您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-05-03 15:43
随着基因诊断技术和对疾病分子机制认识的发展,RNA疗法正逐渐成为一种新的、非常有前途的治疗方法,用于个性化和精准医疗,可治疗罕见病和常见疾病。全球已上市寡核苷酸药物见表1,共14个药物,其中12个均在2016年之后上市。
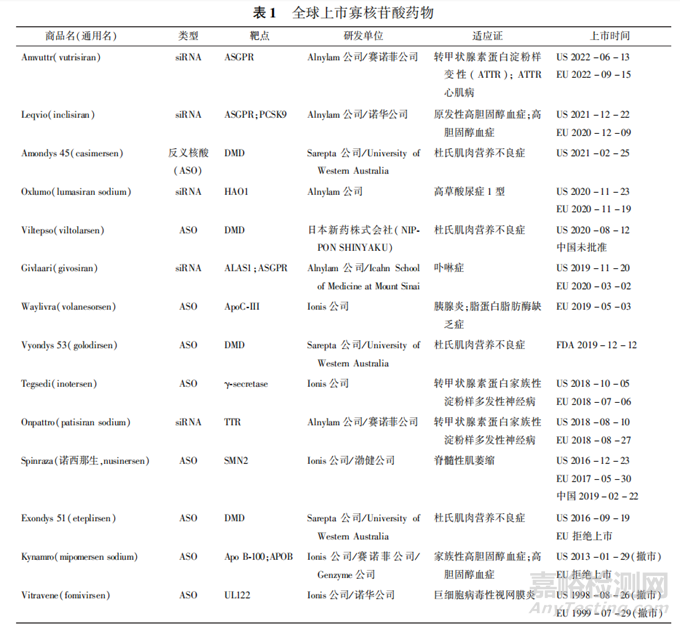
寡核苷酸药物通过与信使RNA(mRNA)互补结合,干扰mRNA转录为蛋白质发挥药效,通常每条链上含有12~30个经化学修饰的核苷酸亚基。关于寡核苷酸药物是按照生物制剂还是化学药品申报注册,目前国内尚无明确规定;美国FDA认为化学合成寡核苷酸与小分子更类似,将其按照化学药由药品评估和研究中心(Center for Drug Evaluation and Research, CDER)监管,而基于载体或启动子驱动的寡核苷酸药物则按照生物制剂由生物制品评价和研究中心(Center for Biologics Evaluation and Research, CBER)监管。由于寡核苷酸药物的分子尺寸介于小分子和生物制剂之间,且制造工艺相比普通小分子更复杂,多个国际人用药品注册技术协调会(ICH)研究指导原则(Q3A,Q3B,Q6)的适用范围明确将寡核苷酸药物排除在外,国内外亦尚无针对寡核苷酸药物药学研究的专门指导原则。
美国FDA曾指出关于寡核苷酸药物的监管存在以下挑战:① 对于质量研究和标准制定方面均无明确指导原则。② 由于寡核苷酸药物的多样性,包括单链反义寡核苷酸、剪接调节剂、适配体和免疫调节剂、双链siRNA(通过RNAi机制发挥作用)等,而这些不同作用机制的药物会有不同的毒理学特征,从而导致不同的问题。③ 对于杂质的鉴定限和质控限尚无明确共识。④ 杂质表征存在困难,由于寡核苷酸杂质与主成分性质非常接近,导致分析方法对于杂质之间及杂质与主成分之间的分离能力存在很大挑战。
本文讨论的范围是化学合成的寡核苷酸药物,不包括通过重组和酶法制备的mRNA等。本文将结合已上市化学合成寡核苷酸药物的审评报告、欧洲制药业成立的寡核苷酸联盟(EPOC)发布的一系列技术白皮书、相关文献等进行分析,对化学合成寡核苷酸原料药(API)所用起始物料的药学研究进行探讨,以期为国内化学合成寡核苷酸药物的研发提供参考。本文中所阐述的观点除明确有官方出处外,其余均为个人观点,不作为药品申报的依据。
1、已上市寡核苷酸药物及其化学结构修饰
天然核苷酸成药性方面存在以下问题:① 体内稳定性差。② 难以被靶细胞摄取。③ 脱靶效应。因此,需对天然核苷酸进行化学修饰,以增加稳定性、提高对靶点的亲和力、促进细胞摄取,并提高体内的生物利用度。
寡核苷酸药物的化学修饰可分为3类:① 核苷酸间链接的修饰:最常见的为硫代磷酸酯修饰,其中磷酸二酯键中的氧被硫取代,由于硫代磷酸酯为手性结构,这也通常会导致API由2n(n为硫代数量)个非对映异构体组成。② 糖环的修饰:由于核糖的2′位为羟基,对其进行修饰还可以防止副反应的发生,常见的修饰包括:2′-OMe, 2′-F,2′-O-MOE(甲氧乙基)、2′-脱氧;此外,还有采用吗啉环代替糖环的修饰方式(如已上市的viltolarsen, golodirsen, eteplirsen)以及2′,4′形成桥环的修饰方式。③ 杂环碱基的修饰:常见的修饰包括嘧啶环上C5位甲基取代。
除了前述的化学修饰外,结构优化的另一个有效方式是与缀合物偶联,以改善寡核苷酸药物在特定组织的分布和细胞摄取,缀合物可以是多肽、蛋白质、碳水化合物、适配体和胆固醇、生育酚或叶酸等小分子,目前已有多个靶向肝脏的N-乙酰半乳糖胺(GalNAc)缀合物偶联寡核苷酸药物获批上市,GalNAc可以降低毒性、提高药效、改善药动学(PK)性质、降低脱靶效应。此外,递送系统也是非常重要和热门的研究及应用领域,可以改善寡核苷酸药物在体内分布、细胞摄取并降低毒性,如已上市药物patisiran采用纳米脂质体(LNP)递送。递送系统属于制剂的范畴,不在本文讨论范围。
经查询欧洲EMA的官方评估报告(EPAR),本文总结了欧盟上市寡核苷酸药物API的结构特点、制备方法、制剂类型及处方,见表2。

可以看出所有寡核苷酸药物均采用固相合成工艺,制剂均为注射液(给药途径包括皮下注射、静脉注射、鞘内注射)且大部分为简单溶液型注射液。这些寡核苷酸药物在磷酸酯、核糖、碱基结构以及链末端(缀合物)均有不同程度的修饰。
2、固相合成工艺
寡核苷酸API采用固相合成工艺(见图1),在装有固相载体(成分为化学修饰的树脂或玻璃)的填充柱上通过计算机编程控制进行自动化合成,整个寡核苷酸树脂的合成是连续进行的。
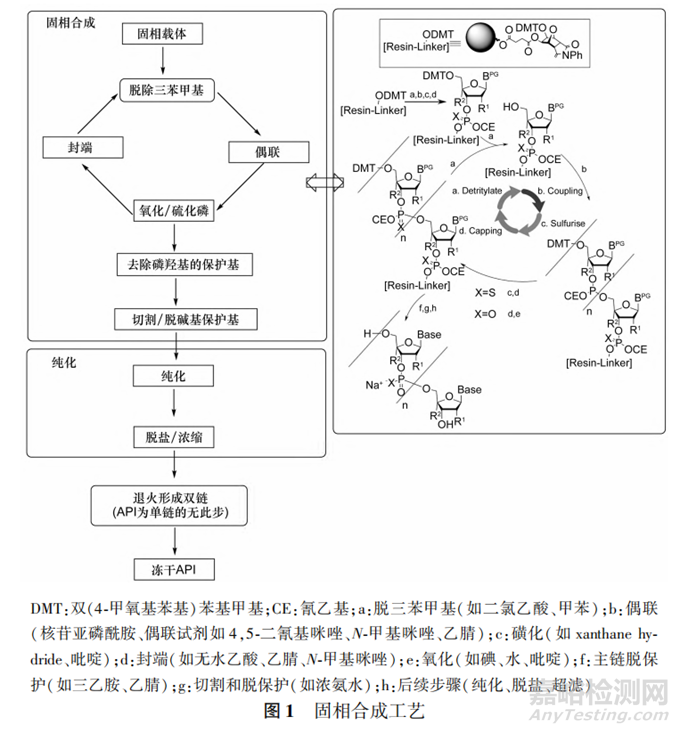
固相合成具有稳定、高产率、高化学选择性以及广泛的洗涤步骤优势,合成结果高度可控及可预测,整个制备工艺包括6步。
① 从3′到5′端在固相载体上逐步偶联核苷酸(通常采用保护的核苷亚磷酰胺进行),得到寡核苷酸树脂,每个循环包括:脱除核糖5′的DMT保护基,暴露核糖的5′-OH连接位点;与下一个核苷亚磷酰胺偶联得到亚磷酸二酯;亚磷酸二酯不稳定,需将Ⅲ价的磷氧化为V价的磷酸酯(P=O)或硫代磷酸酯(P=S);封端/带帽,加入酰化试剂,以封盖由于不完全偶联或脱保护副反应而残留的任何未反应的羟基中心,从而防止此类杂质的传递。
靶向配体可以类似的方式偶联至树脂上,最后一个核苷酸的DMT保护基可在该步或者裂解后进行脱除;在偶联完成后,胺洗可脱除主链保护基(常见为磷羟基的氰乙基保护基),得到碱基被保护的寡核苷酸树脂。
对于20聚体寡核苷酸,这意味着共有80个合成步骤依次进行,过程中没有分离的中间体,因此在以上每一步反应后都要用溶剂对树脂进行多次洗涤,以去除多余的物料,避免残留至后续步骤中生成杂质。
② 用氨水处理可以脱除碱基上氨基的保护基,同时将寡核苷酸从树脂上裂解下来,将寡核苷酸与树脂分离,得到单链寡核苷酸粗品。
③ 粗品经过液相色谱纯化,通常采用强阴离子交换色谱柱(SAX)。与API非密切相关的杂质(如链长度显著不同于API的杂质)在色谱纯化步骤中很容易被分离,但此步骤中不会去除链长度为全长(或接近全长)的寡核苷酸杂质。
④ 脱盐/浓缩:通过超滤/渗滤来交换反离子(如果需要)并浓缩寡核苷酸溶液。可通过配备膜的切向流过滤设备实现,根据膜的孔径截止尺寸去除残留的有机溶剂、盐和低分子量杂质。或者可以进行一系列基于乙醇的寡核苷酸沉淀及随后从水中复溶去除低分子量杂质和浓缩寡核苷酸。
⑤ 单链寡核苷酸通过退火(加热到高温,再缓慢降温)形成双链寡核苷酸,若API为单链,则无需退火。
⑥ 寡核苷酸溶液通过冻干的方式得到固体API。
3、起始物料
3.1 起始物料的选择
由于寡核苷酸药物制造工艺的复杂性,API中存在的寡核苷酸类杂质谱的复杂性,杂质研究、表征和控制的挑战性及局限性,要保证API批间质量的一致性,遵循从源头控制质量的理念和良好的药品生产质量管理规范(GMP)生产是非常重要的,因此起始物料的控制是关键的一环。
ICH Q11为评估起始物料对成品质量的影响程度提供了科学的基于风险的框架,虽然ICH Q11明确指出寡核苷酸不在范围之内,但其中概述的起始物料选择的理念仍然适用。
欧盟上市寡核苷酸药物的审评报告说明申请人参照ICH Q11选择了合理的起始物料,审评报告中披露的起始物料选择策略见表2,除inotersen和nusinersen未提及外,其他所有寡核苷酸药物均选择保护的核苷亚磷酰胺作为起始物料(文中的核苷亚磷酰胺、酰胺、保护的酰胺等措辞均指保护的核苷亚磷酰胺),另外,有2个品种明确将预加载一个亚基的固相载体作为起始物料。
EPOC联盟在其技术白皮书中指出,核苷亚磷酰胺采用标准的化学制造方法,质量良好的核苷亚磷酰胺物料已能从第三方供应商处广泛获得,其作为起始物料已被广泛接受。但是对于缀合物以及预加载亚基的固相载体作为起始物料尚无明确共识,随着商业化的可及性及对起始物料质量认知的深入,可能会逐渐形成共识。总之,应参照ICH Q11对起始物料选择的合理性进行论证。
值得注意的是,多个寡核苷酸药物的欧盟审评报告中均指出,若将来新增起始物料供应商,在变更获得官方批准后才能实施(欧盟根据风险将上市后变更分为一般变更和重大变更,重大变更需经过监管机构批准后才能实施),可见监管机构认为寡核苷酸药物中起始物料供应商变更对产品质量带来的风险较大。这种风险源于起始物料中的关键杂质会通过相似的合成路径衍生至API中,成为与API同样长度的关键杂质,且不易通过纯化去除。对于一种20聚寡核苷酸药物,若每个起始物料核苷亚磷酰胺中含有某一类关键杂质,即使在起始物料中的含量水平仅0.05%,最终会在API中生成1.0%(20×0.05%)的杂质。因此,起始物料应尽可能不存在关键杂质,一方面是为了保证API的质量,另一方面杂质的产生会造成高昂成本浪费。总之,选择能提供良好质量的起始物料供应商是非常重要的,对于起始物料供应商的变更应进行充分的评估和研究。
3.2 起始物料的质量控制
起始物料根据其类型可分为核苷亚磷酰胺(脱氧酰胺、2′修饰酰胺、复杂酰胺)、缀合物酰胺、预加载亚基的固相载体,应根据起始物料的性质及其对API质量的影响建立合理的质量标准。核苷亚磷酰胺和缀合物酰胺的质量控制项目包括性状、鉴别、有关物质(包括异构体)、残留溶剂、31P纯度、水分、含量等。预加载亚基的固相载体质量控制项目包括物理性质(粒度、膨胀度、堆密度等)、加载亚基的量、质量(性状、鉴别、有关物质、残留溶剂、水分)等。起始物料的质量控制中最有难度的项目是有关物质,应对起始物料的杂质谱分布进行分析,了解杂质的来源、衍生、去除情况,评估各杂质对API质量的影响,从而设定合理的特定杂质、单杂、总杂的限度。
在起始物料的杂质研究中,欧盟审评报告及EPOC均提到了起始物料中的杂质根据与主链树脂的反应性和被工艺清除的能力将其分为两大类,关键杂质和非关键杂质:关键杂质是指具有与起始物料相似的反应基团(通常指含有亚磷酰胺及DMT基团的杂质),能与树脂链反应并衍生至API生成全长杂质,这类杂质通常无法通过强阴离子色谱被清除;非关键杂质是指不与树脂链反应或即使反应也易被清除,最终不影响成品纯度。
起始物料的杂质谱与其合成工艺相关,常见类型起始物料的合成工艺及关键、非关键杂质分析如下。
3.2.1 脱氧核苷亚磷酰胺(简称脱氧酰胺)
固相合成通过树脂的5′-OH与下一个核苷酸的磷酰胺反应生成磷酸二酯键,因此脱氧核苷亚磷酰胺(结构式见图2)需要保护5′-OH(通常用三苯甲基DMT保护)、磷羟基(通常用氰乙基CE保护)、碱基上的伯氨(通常用酰基保护)。
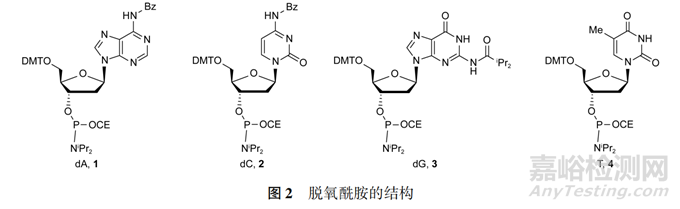
脱氧酰胺以发酵来源的天然脱氧核苷为起始物料(合成路线示例见图3),先对碱基上的伯氨基进行保护(由于胸腺嘧啶无伯氨基无需进行保护),然后5′-OH经DMT保护,再与磷试剂制备得到。
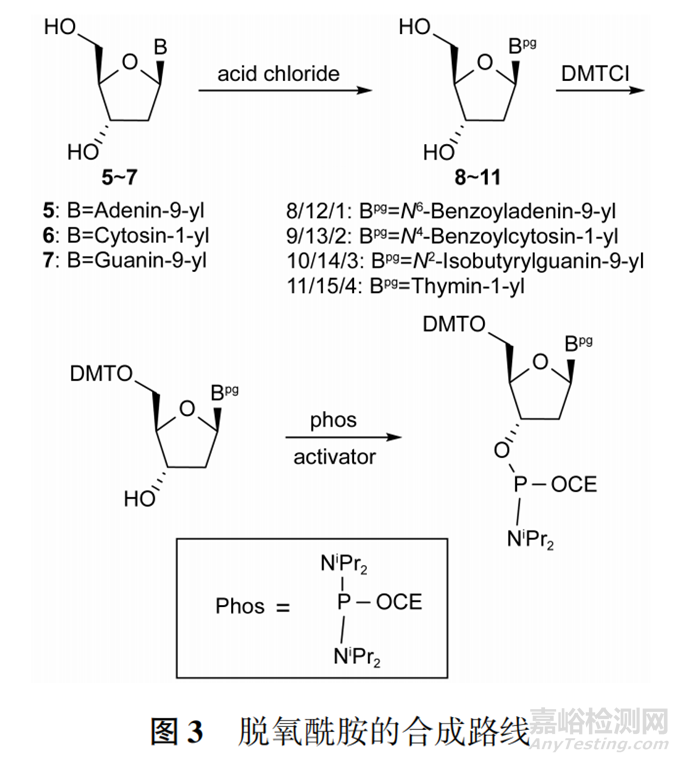
脱氧酰胺的合成过程虽然不会产生新的手性碳,但会产生手性磷中心,导致脱氧酰胺是一对非对映异构体的混合物(在31P-NMR中为双峰),EPOC指出起始物料中磷的绝对构型不会影响API中非对映异构体的分布。API中非对映异构体的分布由偶联反应中的其他因素决定,可能机制为偶联反应中,手性磷被四氮唑活化时会迅速发生消旋,后续硫代反应的立体选择性受磷周围手性基团的影响,最终硫代磷酸酯虽然会存在过剩的磷异构体比例,但通常在40∶60~60∶40之间;美国FDA也曾指出异构体的比例受活化剂影响,不受起始物料构型影响。因此EPOC指出无需控制起始物料中的磷异构体比例。
脱氧酰胺中常见杂质见表3,关键杂质(同时含有磷酰胺基团和DMT保护基团)为3′和5′-OH保护基相反的杂质以及碱基未被保护的杂质,可以通过严格的脱氧酰胺质量标准进行控制。脱氧酰胺的质量标准侧重于控制关键杂质和整体纯度,可以采用HPLC法以及31P NMR法检测杂质和纯度水平。


3.2.2 2′修饰的核苷亚磷酰胺(简称2′修饰酰胺)
对于2′修饰(-OMe、-F、-OMOE)的核苷亚磷酰胺(结构见图4)

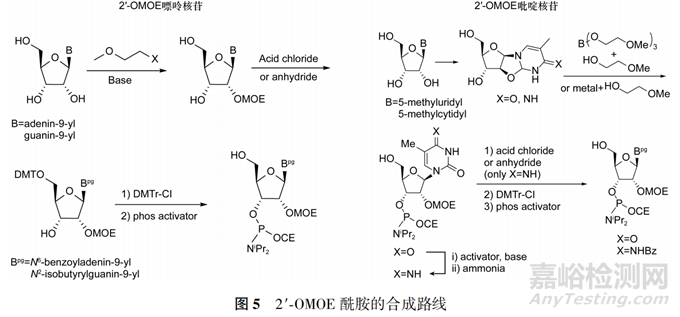
以天然核糖核苷为起始物料,可通过对2′OH进行修饰(修饰后的2′位为惰性反应位点,不再参与反应),后续的上DMT保护基及合成亚磷酰胺步骤与前述脱氧核苷相同。常见的2′-OMOE核苷亚磷酰胺的合成路线见图5。
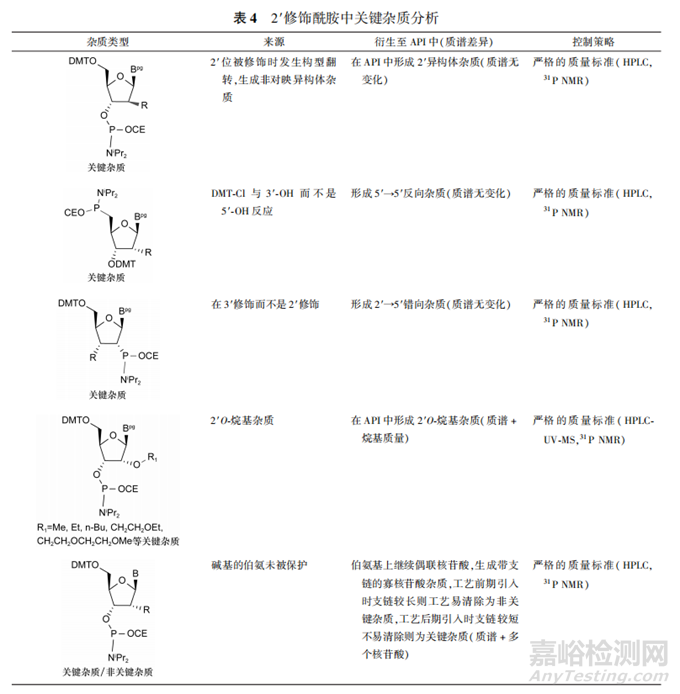
2′修饰酰胺中关键杂质见表4。关键杂质(同时含有磷酰胺基团和DMT保护基团)除了与脱氧酰胺类似的3′和5′-OH保护基相反的杂质和碱基未被保护的杂质外,还包括2′-O烷基修饰的杂质、2′和5′-OH保护基相反的杂质,可以通过严格的脱氧酰胺质量标准进行控制。脱氧酰胺的质量标准侧重于控制关键杂质和整体纯度,可以采用HPLC法(HPLC-UV,HPLC-MS)以及31P NMR来检测杂质和纯度水平。
3.2.3 其他复杂的酰胺
脱氧酰胺和2′修饰酰胺的质量控制要点亦适用于更复杂的酰胺类型,如2′,4′桥环核苷亚磷酰胺(LNAs)、磷酸吗啉寡核苷酸(PMOs),结构见图6。
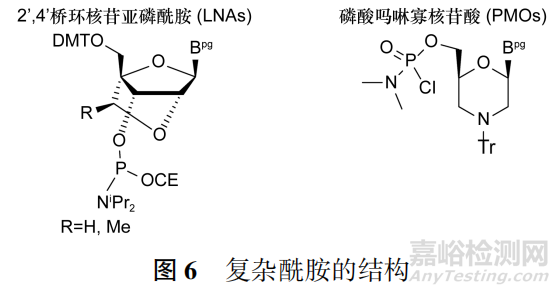
这类更复杂酰胺的供应链可能不如前面所述的脱氧酰胺和2′修饰酰胺完善,而且合成路线更多样,应通过具体合成路线具体分析潜在的关键杂质。有文献提到,LNAs的关键杂质包括桥环上甲基的异构体以及脱甲基杂质。
3.2.4 缀合物
缀合物包括小分子的胆固醇(cholesterol)、生育酚(tocopherol)、茴香胺(anisamide)、叶酸(folic acid)、多肽(peptides)、茴香酰胺(anandamide)、GalNAc、聚乙二醇醚(PEG)和大分子的抗体、适配体等。小分子缀合物通过适当的连接子与寡核苷酸共价连接。
GalNAc能通过与积木蛋白受体(ASGR)结合,将化学修饰的寡核苷酸靶向递送至肝细胞。尽管GalNAc缀合物的化学修饰可以采取多种形式,但它们保留了共同的特征,即几个GalNAc部分(通常为3个,形成三触角结构)通过接头连接到寡核苷酸。GalNAc可在固相合成最后的5′-端引入,也可通过预加载GalNAc的固相载体在3′-端引入。
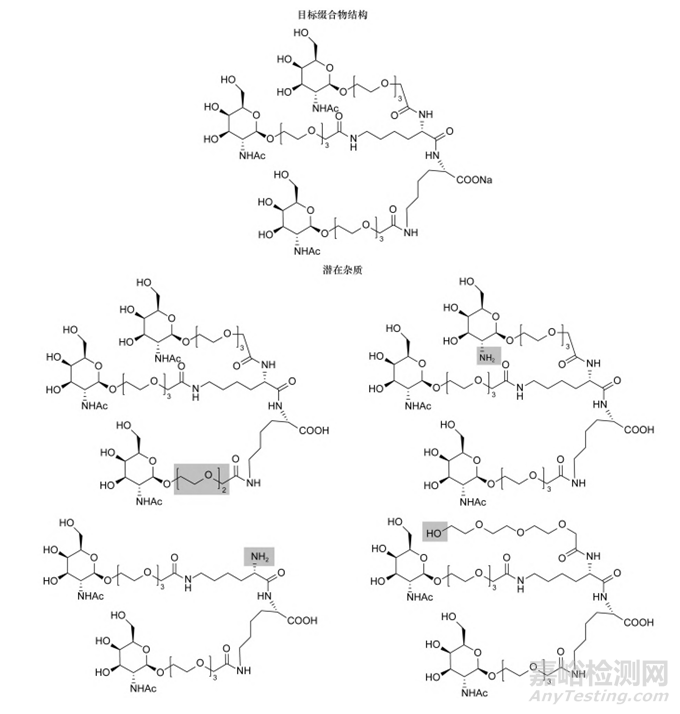
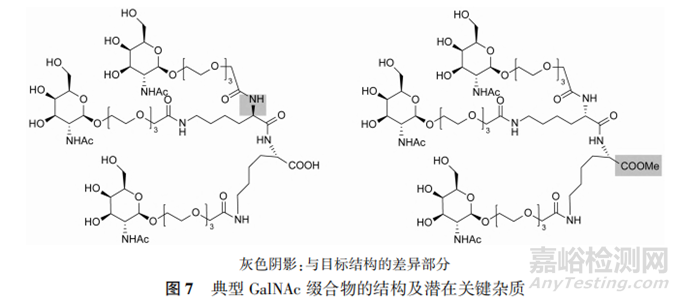
具有双赖氨酸部分的典型GalNAc缀合物结构见图7。通过天然糖和氨基酸反应制备得到单一立体异构体结构,其存在的潜在杂质包括乳糖胺脱乙酰基杂质等。目前,GalNAc缀合物在商业环境中的应用是一个非常不成熟的领域,应根据缀合物的合成工艺及结构特点进行工艺杂质和降解杂质的分析。
3.2.5 固相载体和预加载亚基的树脂
固相载体虽然不是API的组成部分,但是其良好的质量控制有利于API合成工艺的稳健性,其关键质量属性包括:性状、鉴别(IR)、DMT含量(紫外法)、杂质(HPLC法)。
虽然酰胺偶联的产率通常非常高,由于空间位阻或者树脂连接子上仲醇的反应性较低导致第一个亚基的偶联可能较困难,可以采用预加载一个亚基的树脂进行API的制备[已上市药物(如inclisiran, givosiran等)采用预加载GalNAc的固相载体]。预加载亚基的固相载体质量控制项目包括物理性质(粒度、膨胀度、堆密度等)、加载亚基的量、质量(性状、鉴别、有关物质、残留溶剂、水分)等。由于树脂的质量表征方法有限,在论证预加载亚基的树脂作为起始物料时,还应注意从分析方法能否充分控制关键质量属性(尤其是对关键杂质的控制)的角度论证其作为起始物料的必要性和合理性。
4、结语
由于寡核苷酸药物制造工艺的复杂性以及API中存在的寡核苷酸类杂质谱的复杂性,杂质研究、表征和控制的挑战性及局限性,要保证API批间质量的一致性应遵循从源头控制的理念和良好的GMP生产,严格控制起始物料的质量,在申报注册时应参照ICH Q11对起始物料选择的合理性进行论证。相比传统小分子药物,寡核苷酸药物对起始物料的质量要求更为严苛,因此应选择那些能持续提供良好质量起始物料的供应商,而且在变更供应商时应更为慎重。

来源:《中国新药杂志》


