您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-05-06 08:05
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
加科思肺癌新药Ⅱ期临床积极。加科思药业自研KRAS G12C抑制剂戈来雷塞(glecirasib)单药二线治疗非小细胞肺癌患者的的Ⅱ期临床达到主要研究终点。glecirasib的确认客观缓解率(ORR)为47.9%,疾病控制率为86.3%;中位无进展生存期(mPFS)为8.2个月,中位总生存期(mOS)为13.6个月;戈来雷塞总体耐受性良好。详细数据将在ASCO2024会议上公布。
国内药讯
1.罗氏眼科双抗中国获批新适应症。罗氏VEGF-A/ANG-2双抗法瑞西单抗(罗视佳®,Vabysmo®)获国家药监局批准新适应症,用于治疗继发于视网膜分支静脉阻塞(BRVO)的黄斑水肿。在全球Ⅲ期临床BALATON中,法瑞西单抗组患者实现视力改善16.9个字母,中央亚域视网膜厚度(CST)降低311.4μm,实现95.3%患者无黄斑水肿。此前,该新药已获CDE批准用于治疗糖尿病性黄斑水肿(DME)和新生血管性(湿性)年龄相关性黄斑变性(nAMD)。
2.恒瑞减肥新药启动III期临床。恒瑞医药GLP-1R/GIPR激动剂HRS9531在clinicaltrials官网上注册一项III期临床,拟评估用于超重或肥胖患者的疗效和安全性。该项试验预计2025年7月30日结束。HRS9531可通过同时激动GLP-1和GIP受体,发挥葡萄糖依赖性的促胰岛素分泌、抑制食欲和改善胰岛素敏感性等作用,帮助降低血糖和减轻体重。该新药目前正在多项临床研究中评估治疗2型糖尿病的有效性与安全性。
3.普米斯乳腺癌双抗获批Ⅲ期临床。普米斯PD-L1/VEGF双抗PM8002注射液获国家药监局批准开展一项Ⅲ期临床,拟评估PM8002联合注射用白蛋白结合型紫杉醇一线治疗不可手术的局部晚期/复发转移性三阴性乳腺癌患者的有效性与安全性。在Ib/II期临床中,PM8002治疗总缓解率达到78.6%,疾病控制率(DCR)为95.2%。今年3月,PM8002用于上述适应症已被CDE纳入突破性治疗品种。
4.再鼎引进新药拟纳入优先审评。再鼎医药从Argenx公司引进的FcRn拮抗剂艾加莫德注射液(皮下注射)获CDE拟纳入优先审评,用于治疗成人慢性炎性脱髓鞘性多发性神经根神经病(CIDP)患者。该产品可与FcRn结合,使循环IgG水平降低。在Ⅲ期ADHERE试验中,Vyvgart Hytrulo治疗患者的复发风险降低了61%(HR:0.39,95% CI:0.25-0.61,p=0.000039)。
5.维立志博双抗获批Ⅱ期临床。南京维立志博1类新药PD-L1/4-1BB双特异性抗体LBL-024获国家药监局批准开展Ⅱb期临床研究。LBL-024以高亲和力结合PD-L1,阻断PD-L1/PD-1免疫抑制通路,并同时有条件地激活4-1BB通路,能够实现仅在表达PD-L1的肿瘤微环境中限制性地激活T细胞4-1BB信号。在针对晚期恶性肿瘤的Ⅰ/Ⅱ期临床中,LBL-024单药已获得安全性结果和初步疗效数据。
国际药讯
1.强生消化道疾病新药报产。强生IL-23抑制剂古塞奇尤单抗(guselkumab,Tremfya)已向欧洲药品管理局递交两项新适应症上市申请,用于治疗中重度活动性溃疡性结肠炎(UC)和中重度活动性克罗恩病(CD)。这两项适应症的申请分别是基于II/III期QUASAR研究和GALAXI系列研究的积极结果。其中,在Ⅲ期临床(QUASAR)中,guselkumab治疗较安慰剂显著提高UC患者第12周时的临床应答率(61.5%vs27.9%)。
2.K药联合用药胃癌III期临床成功。默沙东PD-1抑制剂帕博利珠单抗(Keytruda)联合曲妥珠单抗、氟尿嘧啶和铂类化疗一线治疗HER2阳性胃癌或胃食管交界处(G/GEJ)腺癌患者的III期KEYNOTE-811研究达到了总生存期(OS)主要终点。与安慰剂组相比,K药联合治疗显著延长患者的OS。2021年5月,FDA基于ORR数据已加速批准K药联合曲妥珠单抗和化疗一线治疗局部晚期且不可切除或转移性HER2阳性G/GEJ腺癌患者。
3.诺华前列腺癌核药Ⅲ期临床积极。诺华靶向放射性配体疗法Pluvicto(177Lu-PSMA-617)在AUA 2024年会上公布用于治疗去势抵抗性前列腺癌(mCRPC)患者的Ⅲ期PSMAfore研究最新结果。数据显示,与使用改变种类的雄激素受体通路抑制剂(ARPI)治疗方案相比,Pluvicto治疗将患者的放射学疾病进展风险降低57%(HR=0.43,95% CI,0.33-0.54),两组中位rPFS分别为12.02个月vs5.59个月。这一结果支持考虑Pluvicto作为治疗这类患者群体的新标准疗法。
4.AZ淋巴瘤新药III期临床积极。阿斯利康BTK抑制剂Calquence(阿可替尼)联合标准化疗免疫疗法(苯达莫司汀和利妥昔单抗)一线治疗套细胞淋巴瘤(MCL)患者的III期ECHO研究结果积极。与苯达莫司汀+利妥昔单抗方案相比,Calquence联合用药显著改善患者的无进展生存期(PFS);次要终点总生存期(OS)方面也观察到有利趋势。Calquence具有良好的耐受性,且副作用较小。
5.精分症创新疗法Ⅱ/Ⅲ期临床积极。Newron公司特异性靶向电压门控钠离子通道阻断剂evenamide,在用于辅助治疗慢性精神分裂症患者的Ⅱ/Ⅲ期临床008A达到主要终点。与安慰剂相比,evenamide辅助治疗患者四周后其PANSS(阳性和阴性综合征量表)总分显著降低(10.2分vs7.6分,p=0.006)。Evenamide耐受性良好,未发现新的安全问题。
6.司美格鲁肽Q1大卖61亿美元。诺和诺德公布2024年第一季度业绩报告,公司总营收653.49亿丹麦克朗(约94.96亿美元),同比增长24%。2024Q1,司美格鲁肽注射用降糖药Ozempic销售额达到278.10亿丹麦克朗(40.41亿美元),增速43%;口服降糖产品Rybelsus销售额为50.13亿丹麦克朗(7.28亿美元),同比增长17%;减肥药Wegovy销售额为93.77亿丹麦克朗(13.63亿美元)。司美格鲁肽3款产品合计创收422亿丹麦克朗(61.32亿美元)。
医药热点
1.湖北将疫苗预防接种异常反应纳入保险补偿。4月28日,据“湖北疾控”消息,湖北省为每一名受种者购买预防接种异常反应基础保险,为接种免疫规划疫苗(一类疫苗)的异常反应提供保障。自2017年起,湖北省在全省范围内免疫规划疫苗预防接种异常反应补偿由“财政补偿”转为“保险补偿”,形成“基础保险”加“补充保险”的预防接种异常反应多层次补偿体系。
2.浙江大学医学院附属第二医院嘉兴医院开工。4月26日上午,浙大二院院长王伟林出席嘉兴医院开工仪式。浙大二院嘉兴医院项目总投资约22.46亿元,建筑面积约20万平方米,拟设置床位1000张(一期实施500床),建设以心血管为专科特色,脑科、骨科、急诊医学为重点的三级甲等医院,建成后将打造集医疗、教学、培训、科研、预防、康复于一体的国家区域医疗中心。
3.美国发现首例通过美容针传播艾滋病毒的病例。据美联社4月29日报道,三名女子在美国新墨西哥州一家无证美容中心接受“吸血鬼面部护理”后被确诊感染了艾滋病毒,这被认为是首例通过使用针头进行美容而感染艾滋病毒的病例。美国疾控中心在《发病率和死亡率报告》中称,从2018年到2023年对这家诊所的调查显示,该诊所显然重复使用了一次性使用设备。
评审动态
1. CDE新药受理情况(05月06日)

2. FDA新药获批情况(北美05月02日)
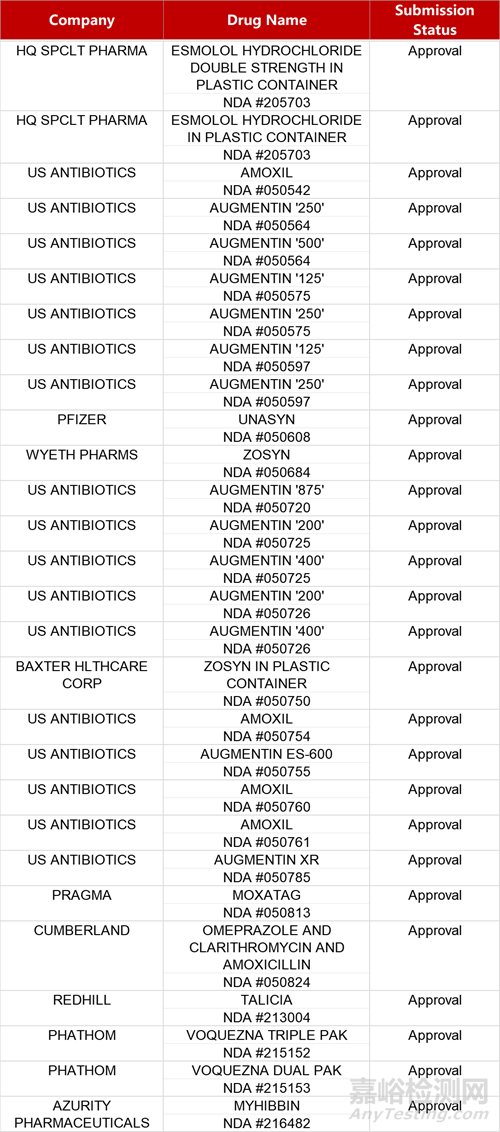

来源:药研发


