您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-06-11 17:10
有机磷类农药(OPs)是目前应用最广泛的农药之一,主要包括对硫磷、乐果、内吸磷、马拉硫磷、敌百虫及敌敌畏等。OPs的应用非常广泛,存在于食物、空气、土壤、水体等中。OPs通过食物链进入人体后,会导致人体健康受损。长期接触低剂量OPs会对人体的心血管系统、生殖系统、神经系统等造成不同程度的影响,甚至导致肿瘤的发生。人体生物监测可精确测量经不同暴露途径进入人体内的环境化合物总量,进而对人体组织和体液内(血、尿、母乳等)环境化学物质及其代谢物进行分析,从而获取个体及群体暴露环境化学物质的类别、数量、负荷水平、变化趋势及早期健康效应等数据。我国于2017年开展了第一轮国家人体生物监测项目,目前第二轮国家人体生物监测项目已开启,OPs是该项目的重要组成部分。以上工作说明,监测人体生物样本中OPs暴露水平具有重大的公共卫生意义。因此,本文综述了检测人体生物样本中 OPs的常用前处理及检测方法,可为监测 OPs及其代谢产物在人体生物样本中含量、了解和综合评价农药的人群暴露剂量及对健康的影响提供方法学参考。
1、OPs理化性质和人体内代谢过程
1.1 理化性质与分类
OPs大多呈油状或结晶状,工业品呈淡黄色至棕色,除敌百虫和敌敌畏之外,大多具有蒜臭味,一般不溶于水,易溶于苯、丙酮、乙醚、三氯甲烷等有机溶剂,对光、热、氧均较稳定,遇碱易分解破坏。敌百虫为白色结晶,能溶于水,遇碱可转变为毒性较大的敌敌畏。市场上销售的OPs剂型主要有乳化剂、可湿性粉剂、颗粒剂和粉剂四大剂型。
1.2 人体内代谢过程
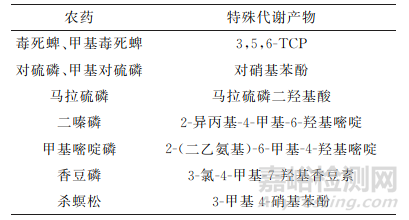
OPs通过消化道、皮肤及呼吸道等途径进入人体内后,可迅速分布于全身脏器并在肝内代谢,代谢方式主要为水解作用和氧化作用。大多OPs结构相似,进入体内后通常被代谢为6种二烷基磷酸盐(DAPs)中的一种或几种,包括磷酸二甲酯(DMP)、磷酸二乙酯(DEP)、二甲基硫代磷酸酯(DMTP)、二乙基硫代磷酸酯(DETP)、二甲基二硫代磷酸酯 (DMDTP)和二乙基二硫代磷酸酯(DEDTP),并在暴露后的6~24h内通过尿液排出。除上述DAPs外,OPs还会产生特殊代谢产物,特殊代谢产物通常对应一种或少数几种OPs,具有特异性。如马拉硫磷二羟基酸是马拉硫磷的特殊代谢产物,3,5,6-三氯-2-吡啶醇(3,5,6-TCP)是毒死蜱、甲基毒死蜱的特殊代谢产物等。文献常报道的一些OPs特殊代谢产物如表1所示。
表1 OPs的特殊代谢产物
2、生物样本的选择
尿液是监测人体OPs暴露最常用的生物样本,优点为样本易于收集,缺点是无法通过尿液中的代谢物推断出特定母体农药的信息。通过检测血液或血液制品可以直接监测血液中的OPs母体化合物,而不是代谢物。但是,血液样本不易收集,样本量有限且血液中农药浓度水平低,对分析技术的灵敏度要求更高。除了常用的尿液、血液样本外,其他样本如胎粪、脐带血、羊水等也在暴露评估中起着重要作用。胎粪可反映妊娠16周到分娩前的污染物长期累计暴露水平,是胎儿宫内暴露评估的良好基质。脐带血可以不用静脉穿刺即可得到相对较大的样本量 (>30mL)。与胎粪只能检测妊娠期第16周到分娩这段时间的婴儿暴露剂量相比,测量羊水(妊娠12~20周期间)可以了解胎儿早期暴露情况。其他可用于暴露评估的生物样本如唾液、头发等在人体OPs生物监测与暴露评估研究中报道较少。
3、生物样本的前处理方法
合适的前处理方法不仅可以有效提取农药,减少或消除生物样本中基质成分的干扰,而且可以提高检测方法灵敏度。生物样本中OPs的前处理技术发展迅速,目前常用的方法有液液萃取法(LLE)、 固相萃取法(SPE)、QuEChERS等。
3.1 液液萃取法
LLE的优点是简单快速、经济易行、技术成熟、应用范围广,不需要复杂的设备,是最经典的前处理方法之一。常用的萃取溶剂主要有乙酸乙酯、二氯甲烷、正己烷、丙酮等。但是,LLE是一种非选择性方法,生物样本中的脂质、糖类等干扰物质也会随OPs被共萃取,需采取进一步措施去除萃取液中的脂质,如冷冻离心、吸附色谱、凝胶渗透色谱等。同时,LLE需要的有机溶剂用量较大,溶剂挥发会对操作者产生一定毒害。
周志荣等在进行LLE 时,比较了乙酸乙酯、二氯甲烷、丙酮3种常见萃取溶剂的提取效率,并选取乙酸乙酯萃取血清中8种OPs。陈雁君等用丙酮、二氯甲烷、三氯甲烷、正己烷、乙酸乙酯等溶剂萃取人血清中的乐果,以气相色谱-质谱法(GC-MS)测定,经比较,丙酮毒性较低,且所得OPs回收率高。DULAURENT等选取乙酸乙酯为萃取溶剂重复提取尿液中6种DAPs。LLE在生物样品OPs检测中的应用如表2所示。
表2 LLE在生物样本OPs检测中的应用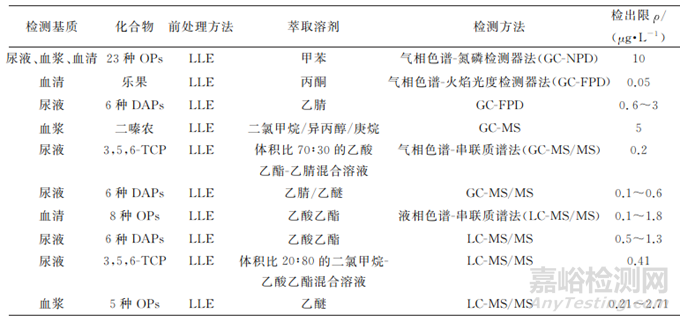
3.2 固相萃取法
SPE具有溶剂用量少、提取效率高、可实现自动化批量处理等的优点,是常用的生物样本前处理方法之一。SPE柱的常见填料有C18、Oasis HLB等。柳洁等以Oasis HLB柱萃取,乙酸乙酯洗脱时,血样净化效果和其中25种OPs的回收率最好。冯翠玲等采用C18 柱萃取,气相色谱法(GC)测定血浆中4种OPs含量。黄梦莹等分别考察了亲水亲油平衡(Waters Oasis HLB)柱、弱阳离子交换(Waters Oasis WCX)柱及弱阴离子交换(Waters Oasis WAX)柱对尿液中4种OPs代谢物的萃取效果以及含体积分数10%,20%,30%甲酸的甲醇溶液和含10%甲酸的乙腈溶液的洗脱效果,并选取Waters Oasis WCX柱和含10%甲酸的甲醇溶液进行试验。DE ALWIS 等以苯乙烯-二乙烯基苯(SDVB)聚合物为吸附剂,建立了全自动、高效率净化尿液的方法,该方法可实现人尿液中的6种DAPs的重复测定。SPE在生物样品OPs检测中的应用如表3所示。
表3 SPE在生物样本OPs检测中的应用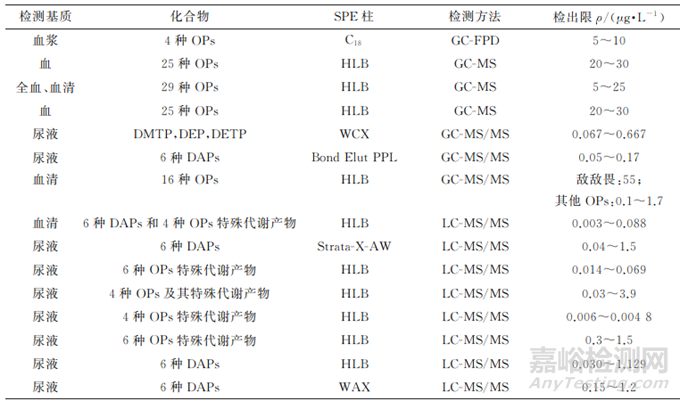
3.3 QuEChERS
QuEChERS是近年来发展起来的一种快速前处理方法,与传统前处理方法相比,该方法具有操作简单、成本低廉等优点。QuEChERS基本包括提取和净化两个步骤,兼具固-液萃取(SLE)和分散固相萃取(d-SPE)的优势。洪萍等建立了一种同时测定中毒者血样中4种 OPs的快速检测方法,在处理血液样品时应用了QuEChERS,取得了满意的结果。QuEChERS在生物样品OPs检测中的应用如表4所示。
表4 QuEChERS在生物样本OPs检测中的应用
3.4 其他前处理方法
除上述常用方法外,还有一些前处理方法,如固相微萃取法(SPME)、液液微萃取法(LLME)、微波萃取法(MAE)、加速溶剂萃取法(ASE)以及 LLE、SPE、QuEChERS的联用方法,亦取得不错效果。
FIŠEROVÁ 等将样品溶液过HLB柱后,收集流出液进行QuEChERS净化,用于提取尿样中5种DAPs和5种特殊代谢产物。其他前处理方法在生物样本OPs检测中的应用如表5所示。
表5 其他前处理方法在生物样本OPs检测中的应用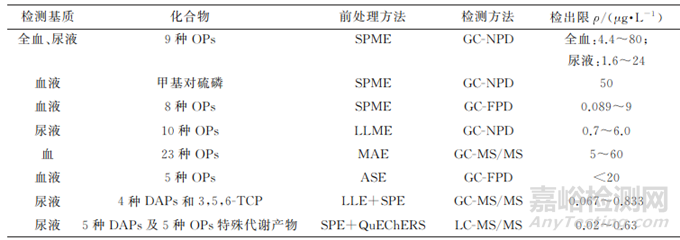
4、生物样本的检测方法
4.1 气相色谱法
GC是目前测定OPs残留量的经典手段之一,常用FPD和NPD来检测OPs。
冯翠玲等采用GC-FPD分析实际中毒病人血浆中4种OPs,检出限为 5~10μg·L-1,该方法操作简便、结果可靠,灵敏度高,可为临床中毒病人的急救提供可靠的依据。WU等采用GC-FPD检测上海地区90名受试者120份尿液样本中的6种DAPs,所得回收率高、检出限低。将该方法用于评估非职业性和职业性人群的OPs暴露水平,获得上 海地区针对OPs项目的首份生物监测报告。TARBAH等采用GC-NPD对尿液、血浆、血清和食物多种样本中23种 OPs进行定量分析。LEE等采用SPME提取人体全血和尿液中的9种OPs,并采用GC-NPD检测。PITARCH等采用GC-NPD同时测定尿液和血清样品中10种常见OPs的含量。
4.2 气相色谱-质谱法
GC只依靠色谱的保留时间进行定性,定性能力有限,而质谱检测器(MS具有定性能力强的优势。GC-MS是定性定量分析痕量化合物的重要手段,广泛应用于复杂多组分的分离鉴定。
柳洁等用SPE-GC-MS建立了一种同时检测中毒血样中25种OPs的方法,检出限为20~30μg·L-1。LACASSIE 等提出了一种高效、特异性强、灵敏度高的同时测定血液和血清中29种OPs含量的方法,检出限为5~25μg·L-1,且方法回收率、精密度和准确度良好。
4.3 气相色谱-串联质谱法
GC-MS/MS可选择特定的母离子进行二次质谱分析,有效地排除了样本中其他物质的干扰,灵敏度更高、抗干扰能力更强,有更强的定性能力,更适合分析生物样本中的痕量农药。周志荣等采用GC-MS/MS测定血清中敌敌畏、对 硫磷、氧化乐果等16种OPs的含量,除敌敌畏外,其他OPs的检出限均低于2μg·L-1。BRAVO等构建了测定约1100份孕妇和儿童尿液样本中6种DAPs含量的GC-MS/MS,检出限为0.1~0.6μg·L-1,该检测方法可用于一般人群研究。
4.4 液相色谱-串联质谱法
LC可以有效的分离和检测热不稳定性、高分子以及高沸点的化合物。但是,采用LC定性未知化合物时,必须通过已知标准物质定性,若无标准对照,则需借助质谱、化学分析、红外光谱等辅助定性。目前,应用于生物样本中OPs检测的方法主要为LC-MS/MS。
DULAURENT等采用LC-MS/MS 同时定量分析6种DAPs,结果显示,LC-MS/MS可用来监测一般人群接触OPs的水平。王贤亲等采用LC-MS/MS检测人血浆中5种OPs,检出限为0.21~2.71μg·L-1。张成龙等采用QuEChERS提取和净化血液样本后,采用超高效液相色谱-四极杆静电场轨道离子阱高分辨质谱法(UPLC-Q Exactive Orbitrap HRMS)同时检测血液中13种OPs代谢产物,13种OPs代谢产物标准曲线线性关系良好,检出限为0.2~10μg·L-1。
5、结语
1)针对生物样本中OPs的分析,如果目的是追溯人体暴露于具体哪种 OPs(如中毒事件原因排查),则应选择血液样本;如果目的是监测正常人群日常生活中暴露于OPs的总负荷,则尿液样本更具优势。
2)在生物样本中OPs检测种类方面,本文涉及的文献累计报道了75种 OPs以及16种OPs代谢产物,单篇文献报道的农药种类最少为1种,最多为29种,其中大部分文献在OPs检测种类的选择上无依据的标准。国家标准GB 2763—2021《食品安全国家标准 食品中农药最大残留限量》规定了564种农药残留限量,包括我国批准登记农药428种、禁限用农药49种以及我国禁用农药以外的尚未登记农药87种。建议相关研究选择检测农药种类时可以参考 GB 2763—2021,比如在分析血液样本时,以49种禁限用农药为待测对象。GBZ/T 300.149—2017《工作场所空气有毒物质测定 第149部分:杀螟松、倍硫磷、亚胺硫磷和甲基对硫磷》、GBZ/T 300.150-2017《工作场所空气有毒物质测定第150部分:敌敌畏、甲拌磷和对硫磷》、GB/T 300.151—2017《工作场所空气有毒物质测定 第151部分:久效磷、氧乐果和异稻瘟净》、GB/T 300.153—2017《工作场所空气有毒物质测定 第153部分:磷胺、内吸磷、甲基内吸磷和马拉硫磷》规定了工作场所空气中14种OPs的测定方法,但没有规定OPs环境暴露时血液样本的分析方法,建议在此后工作中进行补充和完善。
3)高效的样品前处理方法是获得准确检测结果的关键。样品前处理方法主要有LLE、SPE、SPME、QuEChERS等。其中,LLE和SPE都是经典且常用的前处理方法,技术成熟,但LLE缺少净化步骤,且需要使用大量有机溶剂,对人体危害较大;SPE 是一种主流的前处理技术,虽然净化效果较好,但存在时间耗费长等问题;SPME所得OPs的回收率较低;QuEChERS是一种较新的前处理技术,凭借其快速、简单、可靠、安全等特点而发展迅速,GB 23200.113—2018《植物源性食品中208种农药及其代谢物残留量的测定气相色谱-质谱联用法》首次把QuEChERS引入到国家食品安全标准中,该方法是未来监测生物样本农药残留的发展方向及趋势。
4)检测方法主要有GC、GC-MS、GC-MS/MS、LC-MS/MS等。GC在定性定量分析的准确度上存在一定的局限性;GC-MS具有高灵敏、高选择、高抗干扰的优点,但MS定性能力不及MS/MS;GC-MS/MS具有更高的灵敏度,非常适合痕量农药的定性定量检测,且能有效消除假阳性现象;LC-MS/MS的应用范围更广,适用于GC-MS/MS不适用的高沸点农药的检测。
5)检出限可以综合反映方法的灵敏度与精密度。检出限越低,意味着该方法灵敏度越高,精密度越好,是评价仪器性能及分析方法的重要技术指标。OPs代谢快,蓄积性弱,普通人体液内的农药及其代谢产物的含量很小,这要求检出限需达到痕量水平。以乐果为例,LLE所得的平均检出限为5.11μg·L-1,SPE所得的平均检出限为9.57μg·L-1,QuEChERS所得的平均检出限为20μg·L-1;GC 所得的平均检出限为9μg·L-1,GC-MS所得的平均检出限为15μg·L-1,LC-MS/MS所得的平均检出限为0.21μg·L-1,说明不同前处理方法和检测方法等皆会影响OPs检出水平。但是,这些已报道方法存在基质干扰大、试验成本高、部分OPs代谢物检出限偏高等问题,建议后续在构建相关检测方法时应尽可能提高方法的灵敏度。
监测OPs环境暴露与人体健康关系的研究依赖于检测技术的发展,因此开发操作简便、分析快速、灵敏度高、重现性好、多种农药同时检测的前处理与检测方法是相关研究的重要方向。
作者:陈玉婕1,刘华良1,2,张昊2,卢宇剑1
单位:1.南京医科大学 公共卫生学院;
2.江苏省疾病预防与控制中心 理化检验所
来源:《理化检验-化学分册》2024年第4期

来源:理化检验化学分册


