您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-07-05 09:08
本文是印度制药专家在2023年12月发表的一篇综述,内容涉及到亚硝胺的毒理学影响、产生的根本原因,风险评估及解决方式的探讨。
药品中N-亚硝基化合物,特别是N-亚硝胺的存在由于其显著的遗传毒性和诱变作用而引起了全球安全性问题。本文综述研究了它们在活性药物成分(API)、药品和药用辅料中的毒性,以及用于检测的新分析策略、根本原因分析、重新制剂改良策略和亚硝胺的监管指南。强调了N-亚硝基化合物的分子毒性,重点是遗传毒性、致突变性、致癌性和其他生理效应。此外论述了持续的亚硝胺危机、无亚硝胺产品的开发以及灵敏检测方法和精确风险评估的重要性。
1.介绍
亚硝胺杂质,即使是痕量也具有剧毒和诱变性,它能够破坏DNA,并随后增加癌症发病率的风险。监管机构在各种活性药物成分(API)和其他批准的药物中发现了亚硝胺杂质,导致沙坦类药物(缬沙坦)、雷尼替丁(zantac)、尼扎替丁、二甲双胍和伐尼克兰在市场上的被召回。
由于亚硝胺杂质水平不可接受,近年来监管机构已将重点转向一类新型亚硝胺杂质,称为亚硝胺原料药相关杂质(NDSRI),其结构与API相似。最近涉及NDSRIs的事件包括盐酸喹那普利,其中检测到N-亚硝基喹那普利的存在。枸橼酸奥芬那君肠溶释放片显示N-亚硝基奥芬那君为杂质。伐尼克兰中的N亚硝基伐尼克兰(NNV)是通过原料药与辅料中存在的亚硝酸盐反应形成的。
根据国际人用药品技术要求协调委员会(ICH)M7指南,亚硝胺杂质被归类为1类已知致突变杂质。国际癌症研究机构(IARC)根据流行病学数据将这些杂质分为2A组和2B组,N-亚硝基二甲胺(NDMA)和NDEA属于2A组,而其他亚硝胺被归类为2B组人类致癌物。所选亚硝胺和NDSRIs的化学结构如图1所示。
为了解决亚硝胺危机,美国药典(USP)正在托管一个名为“亚硝胺交换”的虚拟平台。该平台汇集了制药公司、合同研究组织(CRO)、API制造商和辅料供应商,以促进与亚硝胺问题相关的实时沟通、更新和风险评估。此外,USP还建立了一个“亚硝胺分析中心”,提供测试亚硝基地雷的新型分析方法的更新。
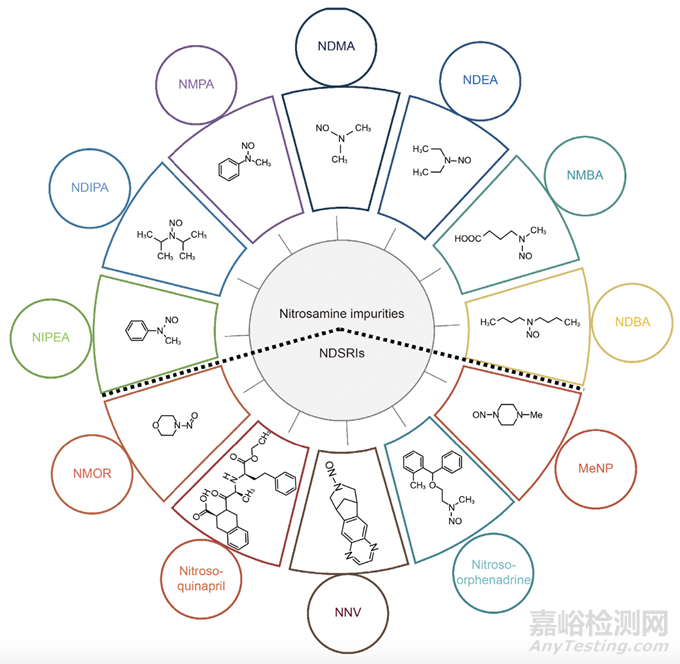
图1:各种亚硝胺杂质和亚硝胺原料药相关杂质(NDSRIs)的化学结构。NDMA:N-亚硝基二甲胺;NDEA:N-亚硝基二乙胺;NMBA:N-亚硝基-N-甲基-4-氨基丁酸;NDBA:N-亚硝基二丁胺;MeNP:1-甲基-4-亚硝基哌嗪;NNV:N-亚硝基-伐尼克兰;NMOR:N亚硝基吗啉;NIPEA:N-亚硝基异丙基乙胺;NDIPA:N-亚硝基二异丙胺;NMPA:N-亚硝基甲基苯胺
药物管制监管机构规定了API和药品中各种亚硝胺杂质和NDSRIs的可接受每日摄入量限值。例如这些限制包括N-亚硝基二甲胺(NMDA)和N-亚硝基-N-甲基-4-氨基丁酸(NMBA)为96 ng/天,N-亚硝基甲基苯胺(NMPA)、N-亚硝基二异丙胺(NDIPA)、N-亚硝基异丙基乙胺(NIPEA)、N-亚硝基二乙胺(NDEA)和1-甲基-4-亚硝基哌嗪(MeNP)为26.5 ng/天,NNV为37 ng/天,N-亚硝基吗啉(NMOR)为127 ng/天,如图2所示。
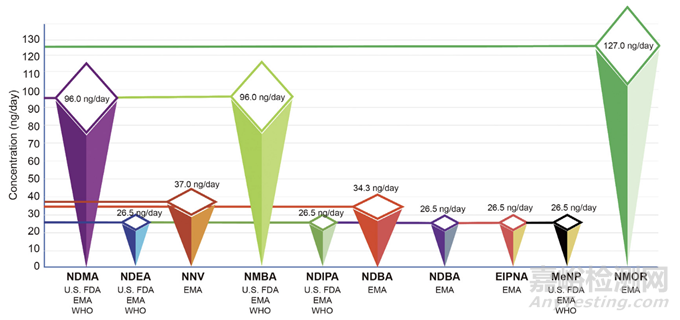
图2: 根据监管机构,药品中选定的亚硝胺杂质和亚硝胺原料药相关杂质(NDSRIs)的每日可接受摄入量限度。NDMA:N-亚硝基二甲胺;美国FDA:美国食品药品监督管理局;EMA:欧洲药品管理局;世卫组织:世界卫生组织;NDEA:N-亚硝基二乙胺;NNV:N-亚硝基-伐尼克兰;NMBA:N-亚硝基-N-甲基-4-氨基丁酸;NDIPA:N-亚硝基二异丙胺;NMPA:N-亚硝基甲基苯胺;NDBA:N-亚硝基二丁胺;EIPNA:N-亚硝基乙基异丙胺;MeNP:1-甲基-4-亚硝基哌嗪;NMOR:N-亚硝基吗啉
促进亚硝胺形成的条件包括易反应性胺的存在,如仲胺和叔胺。这些胺在酸性条件下与亚硝酸反应,导致亚硝胺的形成。亚硝酸本身是不稳定的,在酸性条件下由亚硝酸盐(NO2)形成。亚硝胺杂质也可能来自供应商来源的原材料中的污染,包括含亚硝酸盐的起始材料、中间体以及合成过程中溶剂、反应物、催化剂和试剂的重复使用。在药品生产过程中,应仔细评估几个因素,如添加剂、防腐剂、赋形剂和弹性体成分的选择,因为它们会导致药品中亚硝胺的产生。此外,生产后因素,如水分含量、pH值和产品的储存温度也可能导致亚硝胺的产生。原料药或药品的配方设计师应考虑这些因素,并采取必要措施减少药品中的亚硝胺杂质。此外,如果易受伤害的胺和亚硝酸盐被消耗,亚硝胺也可能在胃肠道中形成。药品中亚硝胺杂质的根本原因和来源在图3中以鱼骨图的形式表示。
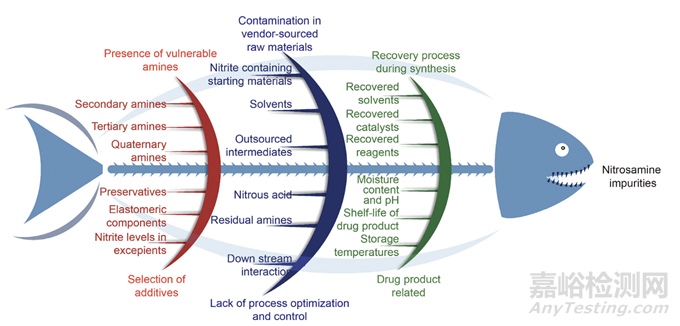
图3: 活性药物成分(API)和医药产品中亚硝胺杂质的根本原因和来源
亚硝胺危机导致的药物召回导致供应链中断和市场上几种药物短缺,引起了全球患者的担忧。它也影响了临床药物开发过程。药物相互作用研究受到二甲双胍、利福平、雷尼替丁、尼扎替丁和普萘洛尔等关键药物召回的影响。实验研究和计算机方法可以方便地从理论上预测许多含有仲胺和叔胺的药物中亚硝胺的形成。
本文综述药品、药用辅料和原料药中N-亚硝基化合物的毒性的重要研究和讨论,主要关注N-亚硝胺。此外,它还涵盖了生理系统中这些杂质的分子毒性特征的最新更新。此外,该综述还研究了用于灵敏检测和定量这些危险杂质的新颖、更新的分析策略。它深入研究了亚硝胺杂质存在的根本原因,并为药品提供了有见地的改良制剂策略。此外它还提供了旨在减少这些亚硝胺杂质发生的法规更新。
2、 文献调研
通过访问公共数据库进行了文献检索,包括PubMed、Medline、eMedicine、国家医学图书馆(NLM)和ReleMed。我们重点关注已发表的文章,包括原创研究、综述文章、病例报告和其他系统综述,有和未有综合荟萃分析,与药用辅料、原料药和药品中的N-亚硝基化合物相关。我们收集与更新的分子毒性含义相关的信息与亚硝胺杂质相关以及多水平方法对灵敏检测的影响。我们对180篇文章的初步筛选产生了本研究的相关数据。本研究收集的所有数据均符合系统综述和荟萃分析首选报告项目(PRISMA)声明中概述的指南。我们对选定的文章进行了自动搜索和手动排序。
2.1 研究选择
在本综述中,纳入了所有已发表或接受的与亚硝胺相关主题相关的文章,特别关注药物中的毒性和分析意义。最初筛选了从1960年至今的总共180篇文章,包括原始研究、综述、病例报告和报告亚硝胺杂质高于监管机构确定的无观察到不良反应水平(NOAEL)的研究。在初步筛选过程中,我们考虑了相关性、出版日期、全文访问和内容等因素。随后,在二次筛选阶段,我们排除了33份报告,包括15份格式不当(如病例报告、信件和简短通信),3份内容不完整,15份全文不可用。这一过程导致选择了147篇文章进行进一步评估。其中,2篇文章被排除在研究之外,2篇文章没有描述亚硝胺诱导的毒性或其药学或分析意义。最终选择143篇文献进行系统综述。通过主要和次要筛选纳入研究的文章的排除和纳入标准的示意图如方案1所示。
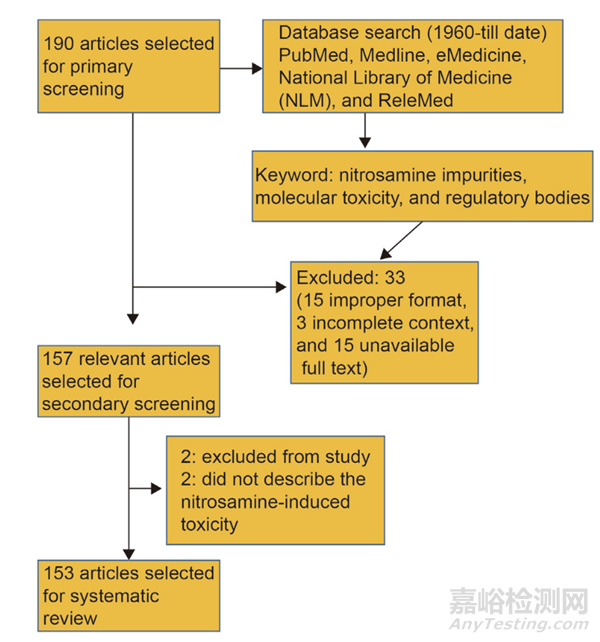
方案1: 通过主要和次要筛选纳入研究的文章的排除和纳入标准的示意图
我们最初的重点是收集有关亚硝胺引起的毒性、副作用或亚硝胺杂质引发的生理毒性的信息。此外,我们旨在探索灵敏检测亚硝胺杂质的分析技术,并提出亚硝胺杂质的监管更新。
2.2数据选择
根据“流行病学观察性研究的系统综述”中概述的国际标准,数据选择和分类遵循特定的标准。这些标准包括讨论亚硝胺诱导的毒性、其他神经系统或全身并发症的文章数量、发表年份和类型,以及描述亚硝胺诱导的毒性相关信号通路的临床前研究,用于毒性管理。为了便于分类,我们将数据分为三个主要组:描述“亚硝胺杂质引发的副作用或生理毒性”的文章、专注于“敏感检测亚硝胺杂质的分析技术”的文章以及旨在“提出亚硝胺杂质监管更新”的文章。分别对这三类的结果进行了审查和分析。这种系统的方法使我们能够解决关键的推论,这可能证明对分子生物学家、分析科学家、研发部门的制剂科学家和参与亚硝胺诱导毒性管理的研究人员。
3.亚硝胺杂质的分子毒性
NDMA、NDEA、N-亚硝基乙基异丙胺(NEIPA)、NDIPA、N-亚硝基二丁胺(NDBA)和NMBA是主要的亚硝胺,它们可以通过生理系统中的遗传毒性或诱变性促进致癌作用。近年来,正如在啮齿动物模型中观察到的那样,很明显,几种药品中的杂质会对人类健康造成重大风险。例如,NMBA和NDEA与NMDA和12种致癌N-亚硝基甲基-N-烷基胺(NMA)具有代谢相似性。在亚硝胺诱导的毒性研究中,通过检查染色体畸变、姐妹染色单体交换和微核形成来评估遗传毒性和致瘤性。
3.1 基因毒性
亚硝胺杂质如NDMA、NDEA等可诱导致突变作用,随后从而导致致癌性。由于体内遗传毒性模型,NDMA已被证明会诱导突变。细胞色素P450(CYP450)酶如CYP2E1和CYP2A6参与N-亚硝胺的代谢并形成N-亚硝基二烷基胺。例如,在啮齿动物模型中,CYP2E1与几种底物的代谢有关,包括有机溶剂、亚硝胺和其他药物分子。此外,CYP3A4在催化更大的N-亚硝胺的活化中发挥作用。CYP2E1的差异表达在不同的体外或体内模型中调节亚硝胺代谢。
4-(甲基亚硝胺基)-1-(3-吡啶基)-1-丁酮(NNK)介导的DNA损伤的遗传毒性包括甲基DNA碱基加合物的形成,例如O6-Me-dGuo和N7-Me-dGuo。由健康细胞中N-亚硝胺活性产生的其他遗传毒性产物包括甲基DNA碱基加合物和吡啶氧代丁基(POB)DNA碱基加合物,包括O6-POB-dGuo和O2-POB-Thd。醛DNA加合物也是由于亚硝胺杂质的存在而形成的显著遗传毒性产物。然而,吡啶基羟基丁基DNA加合物需要进一步广泛的研究来探索亚硝胺的确切性质杂质。表1概述了N-亚硝基化合物在几种体内模型中通过各种给药途径的致癌潜力。
表1: N-亚硝基化合物在几种体内模型中不同给药途径的致癌潜力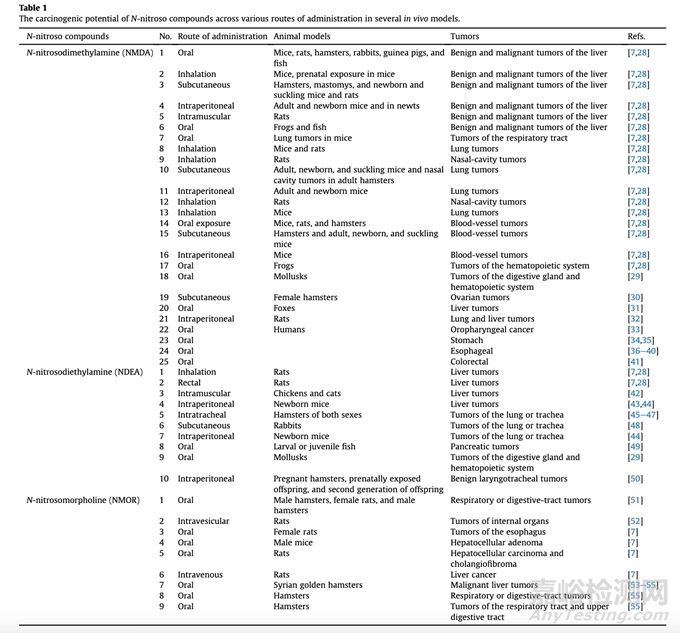
此外,由于药物成分或药物中这些亚硝胺的活性,DNA损伤形成,导致O6-甲基鸟嘌呤或3-甲基腺嘌呤(3MeA)的形成。DNA甲基化主要由NDMA诱导,未修复的3MeA可促进致突变性,随后导致癌症。通常,3MeA诱导的DNA损伤由烷基腺嘌呤糖基化酶修复,烷基腺嘌呤糖基化酶消除甲基化碱基,触发碱基切除修复。因此,烷基腺嘌呤糖基化酶的活性对于最小化亚硝胺杂质如NDMA诱导的致突变性至关重要。
3.2 致癌性
几份流行病学报告描述了亚硝胺对患食道癌、结肠癌、肝细胞癌和其他破坏性癌症的风险的影响。
3.3肺癌
肺癌可以由亚硝胺杂质诱导,因为它们具有通过调节G蛋白信号传导、烟碱乙酰胆碱受体(nAchR)信号传导和表皮生长因子受体(EGFR)信号传导来刺激增殖、迁移和癌细胞存活的能力。例如,亚硝胺对EGFR信号传导的影响可诱导环磷酸腺苷-蛋白激酶A-快速加速纤维肉瘤-丝裂原活化蛋白激酶激酶-细胞外信号调节激酶1/2(cAMP-PKA-RAF-MEK-ERK1/2)轴发生变化,随后促进癌细胞增殖。类似地,EGFR调节可以引起磷酸肌醇-3-激酶-Akt-雷帕霉素哺乳动物靶标(PI3K-AktMtor)信号通路的改变,以促进癌细胞存活。亚硝胺还诱导nAChR信号传导、电压门控钙通道(VGCC)、钙信号传导和蛋白激酶C(PKC)调节的变化,其通过迁移和存活促进癌症进展。当亚硝胺与这些受体相互作用时,HIF1-α信号传导也受β-肾上腺素能信号传导的调节,这些受体随后引起血管生成以向增殖的癌细胞提供营养。
3.2.2.食管癌
食管癌具有较高的发病率和广泛的地理流行,表明环境因素参与了其发展。毒理基因组学过去的报道已经描述了亚硝胺在食管癌发生中的作用。赵等人的一项研究。[64]阐明了亚硝胺在食管上皮中诱导致癌性的潜力。在这项研究中,作者检测了食管鳞状细胞癌(ESCC)、基底细胞增生和癌前病变相关患者的尿亚硝胺水平,并将其与健康个体进行了比较。发现与对照组相比,NMEA、NDBA、亚硝基吡咯烷(NPYR)和NMOR水平升高的ESCC患者的风险更高。根据本报告,危险暴露于N-亚硝基甲基乙胺(NMEA)、NDBA和NPYR的患者发生ESCC的风险较高,表明亚硝胺暴露与食管癌发病率之间存在特定的剂量反应关系。
3.2.3.肝细胞癌和胰腺癌
肝细胞癌是由P450酶参与的亚硝胺代谢引起的致死性癌症之一。生活方式因素,如饮食中暴露于较高水平的亚硝胺或N-亚硝基化合物,与癌症的发展有关。这些化合物特异性地在位于消化器官和肝脏的细胞核中形成DNA加合物,导致亚硝基化合物的致癌性。此外,含有这些化合物的食品加工添加剂是人类接触亚硝胺的重要来源。Zheng等人的一项研究。探讨了特定N-亚硝基化合物、总N-亚硝基化合物的膳食摄入量与肝细胞癌发生之间的关系。作者得出结论,较高的N-亚硝基化合物摄入量可能会增加肝细胞癌发病率的风险,与其他风险因素如乙型肝炎病毒(HBV)或丙型肝炎病毒(HCV)感染或酒精摄入有关。
NDEA和NDMA主要是药物中发现的重要亚硝基化合物,这些被归类为人类2A组致癌物。CYP450酶的代谢激活可以诱导亲电烷基化,导致突变诱导的DNA加合物的形成。肝酶在亚硝胺的代谢中起着重要作用,与其他肝外组织相比,在肝脏中观察到更大的活性。关于亚硝胺的剂量-反应关系表明,NDMA和NDEA在体内模型中诱导肝肿瘤。在体内模型和人类显著暴露于亚硝胺的肝肿瘤中都观察到DNA加合物的形成。N-亚硝胺诱导烷基中α-碳原子的羟基化,在肝细胞中产生羟基亚硝胺,随后促进DNA烷基化。这些连续事件进一步引起基因损伤、突变,并通过触发致癌信号赋予肝细胞恶性转化为癌细胞,如图4所示。此外,暴露于N-亚硝胺通过线粒体DNA、氧化磷酸化(OXPHOS)信号和其他线粒体代谢途径的改变影响肝脏脂质代谢。亚硝胺的另一种机制涉及通过氧化应激、三磷酸腺苷(ATP)耗竭和脂肪酸氧化相关酶的下降诱导肝组织炎症。
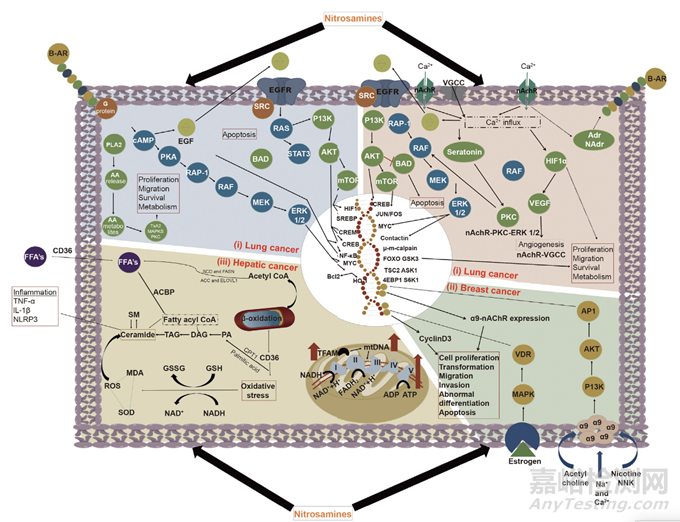
图4:亚硝胺在各种类型癌症中的分子信号通路。(i)肺癌:亚硝胺可通过调节G蛋白信号传导、烟碱乙酰胆碱受体(nAchR)信号传导和表皮生长因子受体(EGFR)信号传导来刺激癌细胞增殖、迁移和存活。(ii)乳腺癌:亚硝胺调节腺苷酸环化酶/环磷酸腺苷(cAMP)/蛋白激酶A(PKA)/cAMP反应元件结合蛋白(CREB)通路,该通路介导EGFR信号通路反式激活。(iii)肝癌:N-亚硝胺暴露通过改变线粒体DNA、OXPHOS信号和其他线粒体代谢途径影响肝脏脂质代谢。I:烟酰胺腺嘌呤二核苷酸(NADH)-泛醌氧化还原酶复合物;II:琥珀酸-泛醌氧化还原酶复合物;III:细胞色素Bc1复合物;IV:细胞色素C氧化酶复合物;和V:三磷酸腺苷合酶复合物;B-AR:B-肾上腺素能受体;Adr:肾上腺素;NAdr:去甲肾上腺素;HIF1a:缺氧诱导因子1a;VEGF:蛋白激酶B;RAF:快速加速纤维肉瘤;PKC:蛋白激酶C;ERK:细胞外信号调节激酶;MEK:丝裂原活化蛋白激酶激酶;RAP-1:Ras相关蛋白1;BAD:细胞死亡蛋白的BCL2相关激动剂;mTor:雷帕霉素的哺乳动物靶标;PI3K:磷酸肌醇3-激酶;VGCC:电压门控钙通道;FOS、JUN和Myc:转录因子;m-m钙蛋白酶:钙蛋白酶的同工酶;FOXO:叉头转录因子;GSK3:糖原合酶激酶3;TSC2:结节性硬化症2;ASK1:凋亡信号调节激酶1;4EBP1:真核翻译起始因子4E(eIF4E)结合蛋白1;S6K1:S6激酶1;PLA2:磷脂酶-A2;TxA2:血栓素A2;SREBP-1:甾醇调节元件结合蛋白1;CREM:cAMP反应元件调节蛋白;NF-kB:核因子κ B;Bcl2:B细胞淋巴瘤2;HO-1:血红素加氧酶-1;AA:花生四烯酸;RAS:大鼠肉瘤蛋白;STAT:信号转导和转录激活因子;AP1:激活蛋白1;PI3K:磷酸肌醇3-激酶;MAPK:丝裂原活化蛋白激酶;VDR:维生素D受体;FASN:脂肪酸合酶;ROS:活性氧;CD36:脂肪酸转位酶;SOD:超氧化物歧化酶;ACC:乙酰辅酶A羧化酶;TNF-a:肿瘤坏死因子α;IL-1b:白介素-1b;SCD:硬脂酰-CoA去饱和酶;ELOVL1:ELOV1脂肪酸延伸酶1;ACBP:酰基辅酶A结合蛋白;标签:三酰甘油;DAG:二酰基甘油;PA:磷脂酸;CPT1:肉碱棕榈酰转移酶1;GSH:谷胱甘肽;GSSG:二硫化谷胱甘肽;MDA:丙二醛;NAD:烟酰胺腺嘌呤二核苷酸;TFAM:线粒体转录因子A。
NDEA和NDMA被认为是胰腺致癌物,这表明摄入某些可诱导N-亚硝基化合物产生的食物呈正相关。这项研究还调查了饮食中吸烟、维生素C、维生素E或红肉等因素与胰腺癌发病率的关系。值得注意的是,维生素C和E的摄入可以被认为是亚硝化抑制剂,而红肉中血红素铁的消耗可能有助于N-亚硝基化合物的内源性产生。
己酮可可碱已在实验啮齿动物模型中证明了改善N-亚硝胺诱导的肝毒性和氧化应激的潜力。N-亚硝胺在损害线粒体脂质代谢中的作用仍需要大量研究来调查药物中这些杂质的确切毒理学。
3.2.4. 乳腺癌
乳腺癌仍然是世界范围内死亡和发病的主要原因,通常归因于不健康的生活方式和饮食习惯。烟草含有多种亚硝胺,NNK是一种已知促进恶性癌细胞的重要致癌物。这些烟草衍生的致癌物与包括乳腺癌在内的各种癌症的发展特别相关。NNK通过与癌细胞中存在的nAChR相互作用,在乳腺癌的发展和进展中起重要作用。值得注意的是,a9nAChR受体与乳腺癌细胞的发展和进展有关。此外,尼古丁和NNK可以与该受体系统相互作用,随后通过调节关键的细胞信号通路如丝裂原活化蛋白激酶(MAPK)和PI3K-Akt通路来影响癌细胞增殖。这些信号通路受到尼古丁和雌激素刺激活性的刺激。NNK和尼古丁对a9nAChR的激活通过PI3K-Akt和MAPK信号形成显著的反馈环,这可以进一步启动激活蛋白1(AP1)和维生素D受体(VDR)转录因子刺激,从而赋予癌症发展。这种现象已经通过使用小干扰RNA(siRNA)对a9nAChR的基因敲除研究得到证实。然而,目前在药物制剂和API中发现的亚硝胺杂质尚未通过体外和体内研究来研究其调节a9nAChR促进乳腺癌的活性的潜力。
此外,β肾上腺素能受体系统(G蛋白偶联受体系统的一部分)及其下游信号在NNK活性上促进癌细胞增殖方面发挥着重要作用。该信号通路随后促进腺苷酰环化酶/cAMP/PKA/cAMP应答元件结合蛋白(CREB)通路的调制,而后者又介导EGFR信号通路的反激活。然而,亚硝胺杂质对这些G蛋白偶联信号通路和EGFR通路的调制作用尚未通过体外和体内研究生动地研究它们在癌症发病率中的潜在作用。
3.3.生理改变:血管紧张素受体阻滞剂中的亚硝胺杂质
NDMA、NDEA、NEIPA、NDIPA、NDBA和NMBA是已知在生理系统中诱导致癌性的主要亚硝胺。此外,在药物中发现的这些杂质可能会导致生理系统的改变。例如,氯沙坦、缬沙坦、奥美沙坦、厄贝沙坦和替米沙坦等血管紧张素受体阻滞剂(ARB)已从美国市场召回,原因是其产品中亚硝胺杂质水平升高,可能会破坏生理稳态。这些亚硝胺的存在ARBs主要归因于生产工艺不当。
NMDA在人类肝微粒体中由P450 2E1代谢[20]。甲基氧化可诱导α-羟基-NDMA的形成,这是致突变性的,可同时分解并产生两种活性物质,包括甲醛和甲基重氮氢氧化物。这两种代谢物可能对生理系统有显著影响[108]。在NDEA的情况下,导致肿瘤发生的代谢激活由P450 2E1和P450 2A6深刻介导。乙基重氮氢氧化物由P-450介导的NDEA羟基化形成,其进一步形成乙基重氮,其可以与DNA相互作用并诱导DNA加合物的形成。DNA的形成会导致人体组织中健康细胞的生理学发生显著改变通过致癌作用转化为肿瘤细胞。与NDEA作用相关的啮齿动物研究描述了几种肝癌、食道癌和鼻咽癌的发病率,因为毒性代谢物诱导了生理改变和致癌性。
当与从人体组织获得的食管细胞培养物孵育时,NDMA诱导的DNA加合物,如O6-甲基鸟嘌呤(O6-Me-Gua)和N7Me-Gua。在人体组织中观察到的甲基化DNA加合物通常会损害健康细胞。在肝细胞DNA的情况下,观察到NDMA中毒受害者、O6-Me-Gua和N7-Me-Gua的形成。在NMEA的情况下,N7-Me-Gua是基本上在肝区和肾区形成的DNA加合物的甲基化形式,然后是食道和肺。这些毒性DNA加合物可能在转录和翻译水平上进一步损害细胞蛋白质的形成,这需要大量的未来研究来揭示这些N-亚硝基化合物诱导的生理改变背后的潜在机制。
4.增强亚硝胺杂质灵敏检测的分析技术
多年来,药品中一直有亚硝胺杂质的报道。然而,仍有许多含有这些杂质的产品尚未被彻底探索。最近药品退出市场的激增引起了全球监管机构的极大关注。作为回应,美国食品药品监督管理局(U.S.FDA)、欧洲药品管理局(EMA)、世界卫生组织(WHO)等监管机构敦促所有相关利益相关者对这些杂质进行严格的识别和报告,并建议API和药品制造商开发高灵敏度的分析方法,特别是能够定量下限(LOQ)水平的亚硝胺的气相色谱和液相色谱方法。这对于有效检测和定量原料药、药物合成中间体和药品成品中痕量水平的这些杂质至关重要,最终确保消费者的药品安全。开发这种新颖而灵敏的方法是一项具有挑战性的任务,需要大量的专业知识和研究经验。分析方法开发中的主要挑战可能来自分析物电离不足和基质干扰等问题。当涉及到NDSRIs时,较低的分子量、结构的复杂性以及缺乏现成的标准可能会给实现灵敏检测带来困难。它还需要使用高成本仪器,包括液相色谱串联质谱(LC-MS/MS)和气相色谱串联质谱(GC-MS/MS)。
LC-MS/MS和GC-MS技术广泛用于亚硝胺检测,因为它们在纳克级亚硝胺检测中具有良好的灵敏度。轨道阱和四极杆飞行时间(Q-TOF)分析仪优选用于这些杂质的痕量水平检测。USP的倡议“亚硝胺交流”为行业专家、研究人员和药品制造商提供了亚硝胺检测色谱技术的最新进展。灵敏的分析方法应能够将某些基质(API或药品)中的特定亚硝胺杂质定量至该特定亚硝胺杂质可接受摄入量限度的10%。
GC-MS/MS是鉴定和定量挥发性和半挥发性分析物的优选分析工具。与电子碰撞电离相比,化学电离为亚硝胺杂质的分析提供了更好的特异性和灵敏度。用于亚硝胺分析的GC-MS/MS中使用的固定相包括聚乙二醇(PEG)涂覆的毛细管柱、氰丙基苯基二甲基聚硅氧烷和苯基甲基聚硅氧烷。用于亚硝胺分析的几种检测器包括火焰离子化检测器、氮磷检测器(NPD)和化学发光检测器。GC-MS/MS分析可能会受到残留溶剂的潜在干扰,这可能会影响分析方法的耐用性和灵敏度,例如,二甲双胍中NDMA分析中的二甲基甲酰胺(DMF)干扰。来自复杂基质的干扰可以通过额外的净化和预处理步骤来克服,如固相萃取(SPE)或液液萃取(LLE),以及使用内标。控制和减轻基质的共洗脱至关重要,因为它会导致假阳性结果,缩短气相色谱柱的寿命,并污染质谱仪。这个问题可以通过使用顶空(HS)注射模式来克服。然而,HS进样模式不适用于二甲双胍和雷尼替丁等不耐热分析物的分析。
GC-MS/MS分析中采用的其他替代方法包括无溶剂HS-GC/MS和全蒸发HS-GC/MS,其灵敏度高于HS-GC/MS。采购昂贵的同位素内标的负担可以通过使用诸如HS-GC/MS、HS-固相微萃取(SPME)-GC/MS、分散液液微萃取(DLLME)-GC/MS和具有氮磷检测的全蒸发静态HS气相色谱法等方法来克服,这些方法不需要使用内标。
LC-MS/MS是鉴定和定量极性、非极性和非挥发性分析物的优选分析工具[135]。李等人。指出,与电喷雾电离(ESI)相比,大气压化学电离(APCI)对亚硝胺分析具有更高的灵敏度。ESI是分析N-亚硝基二丙胺(NDPA)的首选。通过使用大气压光电离(APPI)可以最小化来自基质的干扰。正电离模式适用于大多数亚硝胺,而负电离模式在NMBA的情况下是优选的。由于二甲双胍和雷尼替丁的热不稳定性质,美国FDA建议使用LC-MS/MS分析它们。氘化同位素标准品通常用于LC-MS/MS分析。LC-MS/MS分析还涉及样品制备步骤。LLE比SPE更具成本效益。二氯甲烷是NDMA分析的优选提取溶剂。LC-MS/MS中的基质干扰可以通过在线分流阀来克服,该分流阀绕过样品中存在的基质。
在这篇系统综述中,我们努力总结了分析方法的最新进展,特别是气相色谱和液相色谱方法,用于测试原料药和药品中的亚硝胺。这份全面的总结旨在为有兴趣开发更灵敏的方法来检测各种药物中亚硝胺的研究人员提供有价值的见解。表S1列出了监管机构、独立研究人员和行业专家推荐用于亚硝胺分析的LC-MS/MS、GC-MS/MS和HPLC方法。
5.亚硝胺杂质的监管更新
2018年年中,沙坦类原料药中的NDMA开始首次检测到亚硝胺,这促使从市场。国际监管机构,如美国FDA、EMA、欧洲药品和医疗保健质量管理局(EDQM)、健康科学管理局(HAS,新加坡)、药品和医疗器械局(PMDA,日本)、治疗用品管理局(TGA,澳大利亚)和加拿大卫生部(HC,加拿大)合作向API制造商发出警报。他们提出了几项法规、建议和指南来审查其制造工艺,并启动有关亚硝胺形成的风险评估。主要重点是评估API制造中使用的原材料、中间体、溶剂和试剂是否存在易损胺。2018年,缬沙坦产品被召回市场。2019年,雷尼替丁、尼扎替丁和二甲双胍缓释产品被发现含有亚硝胺,导致其于2020年从市场上召回。雷尼替丁产品中亚硝胺水平升高的根本原因与储存条件有关。随后,注意力转移到检查可能导致药品中亚硝胺形成的关键因素上。
监管机构希望制造商进行根本原因分析,以确定亚硝胺是如何掺入药物和药品中的。美国FDA提出了三步缓解策略,以控制和防止原料药和药品中亚硝胺的形成。第一步,制造商应优先考虑其API和药品组合的风险评估,并且必须在2021年3月31日之前记录并向监管机构报告其调查结果(美国FDA)。EMA给出了2021年3月31日(化学药物)和2021年7月1日(生物药物)的时间表。第2步,在2023年10月1日(美国FDA)、化学药物2022年9月26日和生物药物2023年7月1日之前,必须使用敏感分析技术定量亚硝胺的确证性测试。第3步,制造商必须报告确定的亚硝胺形成的根本原因,并实施对其工艺或方法的改变以消除亚硝胺形成。
2020年,Lhasa有限公司(英国)启动了药品制造中使用的辅料中亚硝酸盐含量数据库的创建。这一举措涉及行业专家和研究人员的代表,因为辅料中的亚硝酸盐含量使药品更容易含有亚硝胺杂质。此外,2020年,由EMA组成的人用药品委员会(CHMP)对整个情况进行了科学审查,并提交了这方面的报告。2021年,欧洲药品监管网络成立了一个名为“亚硝胺实施监督小组”的智囊团,讨论亚硝胺杂质出现的发展和当前情况。EMA要求沙坦类、利福平、雷尼替丁、含二甲双胍和伐尼克兰药物的上市许可持有人只有在严格测试后才能将其产品投放市场。
美国FDA主要建议遵循三步缓解策略的步骤2和3,以应对NDSRI问题的出现。他们还呼吁所有相关利益攸关方审查、讨论、提供信息并更新他们的建议和方法,以便监管机构有效解决这一问题。最近在几种产品中发现的亚硝胺以及随后的召回只是冰山一角。未来几天,市场上已经有许多产品的发病率和风险可能会更高。为了应对这一潜在危机,应与所有全球监管机构合作成立一个联合工作组,旨在制定应对即将到来的危机的战略。
6.亚硝胺风险评估和减少亚硝胺杂质掺入药品的重新改良制剂策略
如果在初始分析中报告了亚硝胺,则必须对亚硝胺掺入来源进行根本原因分析。随后,必须设计重新配制策略,以最大限度地降低药品中亚硝胺杂质形成的风险。研究减少药品中亚硝胺的重新配制策略将非常有利于解决亚硝胺引起的危机。
美国FDA建议加入抗坏血酸和α-生育酚等抗氧化剂,因为它们已显示出抑制人体内亚硝胺产生的潜力。此外,使用碳酸钠等赋形剂在体内创造碱性pH环境,可能是一种有效的缓解策略,因为亚硝胺的产生主要发生在酸性介质中。这种重新配制策略可以设计并建议给各个制药行业的配方设计师,也可以通过配方设计师提交的补充或修正传达给监管机构。
在API多步合成过程以及药品储存和运输过程中,亚硝胺可以通过多种途径掺入药品中。在API合成的背景下,含有易损胺的药物特别容易受到亚硝胺污染。在这种情况下,API制造商在为多步合成过程选择催化剂、试剂和溶剂时应采取细致的方法。
在多步API合成过程中,加入额外的纯化步骤可以有效消除亚硝胺的形成。建议在合成过程中避免使用含有伯胺或仲胺以及亚硝化剂和溶剂的试剂。在评估药品中亚硝胺污染的风险时,需要考虑各种因素,如制剂的pH值、水分含量和粒度分布。还应考虑制剂中使用的药物内包装材料和辅料的材料特性。例如,封盖箔中的起泡材料或底漆(例如硝化纤维素)的选择可能是关键的。当暴露于二甲胺和二乙胺等仲胺时,硝化纤维素可以充当亚硝化剂,所述仲胺可能存在于印刷油墨中。在通常在高温下进行的起泡过程中,任何形成的亚硝胺都可能蒸发并可能进入药品。储存条件也可能影响亚硝胺的形成。例如,雷尼替丁API和成品中NDMA的水平会随着储存温度的升高而增加。为了缓解这一点,Harmon等人提出了除氧包装技术来对抗自氧化,这是盐酸雷尼替丁中NDMA形成的一种可能机制。Harmon等人还提出,各种赋形剂的成分甲醛催化亚硝化反应并导致亚硝胺的形成。制造商在为其配方选择辅料时应谨慎,特别是考虑辅料中的亚硝酸盐含量。当原料药和药品中含有易受攻击的胺时,这一点尤其重要。此外,在药品风险评估中,还应考虑弹性成分。在药品储存的情况下,应仔细评估储存温度。图5描绘了减轻亚硝胺杂质掺入药物产品中的重新配制策略。
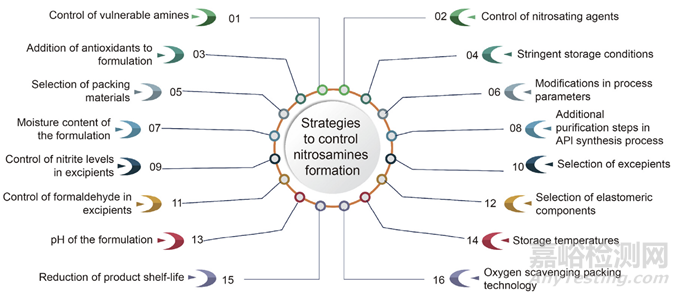
图5:减少亚硝胺杂质掺入药品的重新配制策略。API:活性药物成分
7:结论
该综述提供了与亚硝胺杂质相关的分子毒性的生动精确的风险评估,能够进行有效的根本原因分析和重新配制策略,以减少其在药品中的存在。高灵敏度分析方法的发展简化了这些杂质的检测过程。此外,监管机构和科学界采取积极措施对于解决药品中潜在的亚硝胺杂质相关问题至关重要。这种方法确保了患者的安全,并培养了对各种疾病反复使用药物的信心。
药品、赋形剂和API中N-亚硝基化合物,特别是N-亚硝胺的存在,由于其遗传毒性和诱变作用,对人类健康构成重大风险。强调毒理学数据,设计有效的方法来计算可接受的摄入量限制和探索结构活性关系,可以大大有助于解决亚硝胺的危机。全球相关利益攸关方和专家分享关于亚硝胺的计算机预测、体内研究和分析测试的知识也可以极大地帮助避免重复测试和降低成本。综述展示了亚硝胺杂质对生理系统的有害影响,强调了新型分析策略对灵敏检测和定量的重要性。此外,该综述强调了这样一个假设,即了解根本原因、实施重新改良制剂策略和纳入监管更新可以有效减少药物配方中的亚硝胺杂质,确保开发更安全的产品。

来源:文亮频道


