您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-08-20 08:14
摘 要: 建立液相色谱-串联质谱法测定鸡蛋、虾、鱼等农产品中硝基呋喃代谢物的残留量。样品中的硝基呋喃残留物经盐酸水解后,以2-硝基苯甲醛衍生,采用乙酸乙酯提取,浓缩,净化后再用C18色谱柱分离,以0.1%甲酸水溶液-乙腈溶液作为流动相梯度洗脱,电喷雾离子源(ESI)下以多反应监测(MRM)正离子模式扫描检测,内标法定量分析。呋喃它酮代谢物、呋喃西林代谢物、呋喃妥因代谢物、呋喃唑酮代谢物的质量浓度在0.5~50 ng/mL范围内与色谱峰面积线性关系良好,相关系数均大于0.995,检出限分别为0.13、0.035、0.14、0.017 μg/kg。在鸡蛋、虾、鱼中添加2、5、10 μg/kg硝基呋喃代谢物时,平均回收率为88.71%~105.16 %,测定结果的相对标准偏差为3.12%~9.08%(n=6)。该方法简便、快捷、准确度高,可用于测定鸡蛋、虾、鱼等农副产品中的硝基呋喃代谢物。
关键词: 硝基呋喃代谢物; 液相色谱-串联质谱法; 衍生化; 鸡蛋; 鱼; 虾
硝基呋喃类药物主要包括呋喃它酮、呋喃西林、呋喃妥因、呋喃唑酮等,可抑制或杀灭多种革兰氏菌以及某些真菌和原虫,主要用于预防和治疗肠道细菌感染,在畜牧业和水产养殖中得到广泛应用[1‒2]。由于硝基呋喃类药物及其代谢物属于硝基杂环类化合物,具有细胞诱变性和动物致癌毒性,已引起临床高度重视。欧盟、日本和美国等大部分国家和地区已禁止呋喃西林等4 种硝基呋喃类药物在肉类食品中的残留,我国也在2002年将该类抗生素列为食源性动物禁止使用的药物[3‒4]。由于硝基呋喃类原型药在生物体内代谢迅速,呋喃它酮、呋喃西林、呋喃妥因、呋喃唑酮在体内分别代谢为5甲基吗啉-3-氨基-2-唑烷基酮(AMOZ)、氨基脲(SEM)、1-氨基-2-乙内酰(AHD)、3-氨基-2-恶唑烷酮(AOZ),因此常通过检测代谢物来反映硝基呋喃类药物的残留状况[5‒6]。
硝基呋喃类药物检测标准分类比较复杂,现行有效的国家检测标准就有20个,如GB 31656.13— 2021《食品安全国家标准 水产品中硝基呋喃类代谢物多残留的测定 液相色谱-串联质谱法》、GB/T 21311—2007《动物源性食品中硝基呋喃类药物代谢物残留量检测方法 高效液相色谱/串联质谱法》、GB/T 20752—2006《猪肉、牛肉、鸡肉、猪肝和水产品中硝基呋喃类代谢物残留量的测定 液相色谱-串联质谱法》 等。按照检测仪器分类主要包括高效液相色谱法[7]、液相色谱-质谱法[8‒13]、胶体金免疫层析法[14‒15]、酶联免疫吸附法[16]等,其中液相色谱串联质谱(LC-MS/MS)法检测鸡蛋、水产品等报道最为常见。然而文献报道或国家标准中,液相色谱串联质谱法在检测样品时的分类处理较为复杂,不同类型样品处理方法不一致,衍生化时间较长等问题,笔者尝试建立可同时处理和检测几种不同基质样品的方法,简化样品处理过程,统一检测方法,为鸡蛋、鱼、虾等不同食用农产品的监管与产品质量控制提供了更多的检测方法与思路。
1、 实验部分
1.1 主要仪器与试剂
液相色谱-质谱联用仪:QQQ 4000+型,美国AB SCIEX公司;
超声清洗仪:KQ-250DV型,昆山市超声仪器有限公司。
超纯水机:Milli-Q型,美国密理博公司。
有机系针筒式微孔滤膜:0.45 μm,上海安谱公司。
电子天平:XS205D型,感量为0.01 mg,瑞士梅特勒-托利多公司。
pH计:seven compact型,瑞士梅特勒-托利多公司。
往复式恒温振荡水浴培养摇床:SPH-100×24型,上海世平实验设备有限公司。
高速离心机:Multifuge X pro型,美国赛默飞科技有限公司。
涡旋混合器:XW-80A型,上海驰唐电子有限公司。
高速分散机:T25型,德国艾卡公司。
水浴氮吹仪:JHD-006型,上海极恒实业有限公司。
不同量程移液器:德国艾本德公司。
2-硝基苯甲醛:优级纯,上海阿拉丁生化科技股份有限公司。
盐酸、氢氧化钠、磷酸钾:均为优级纯,国药集团化学试剂有限公司。
乙腈、甲醇、乙酸乙酯、正己烷:均为色谱级,德国默克公司。
甲酸:色谱级,上海易恩化学技术有限公司。
实验用水均为超纯水。
鸡蛋、虾、鱼等样品,市售。
AMOZ、SEM、AHD、AOZ混合标准溶液:各组分质量浓度均为100 mg/L,标准物质编号为S080813,天津阿尔塔科技有限公司。
D5-AMOZ、13C15 N-SEM、13C-AHD、D4-AOZ混合标准溶液:各组分质量浓度均为100 mg/L,标准物质编号为S087591,天津阿尔塔科技有限公司。
1.2 仪器工作条件
1.2.1 色谱仪
色谱柱:Waters ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm,美国沃特世公司);流动相:A相为0.1%甲酸水溶液,B相为乙腈,流量为0.2 mL/min;柱温:30 ℃;进样体积:2 μL;洗脱方式:梯度洗脱;梯度洗脱程序:0~6.0 min,A相由90%降至40%,6.0~6.1 min,A相由40%升至90%,保持3.9 min。
1.2.2 质谱仪
离子源:电喷雾离子源(ESI);扫描方式:正离子扫描;检测方式:多反应监测(MRM);离子源喷雾电压:5 500 V;离子源加热温度:500 ℃;气帘气、雾化气、辅助加热气、喷撞气:均为氮气,硝基呋喃类代谢物质谱参数见表1。
表1 硝基呋喃代谢物的质谱检测参数
Tab. 1 Mass parameters of nitrofuran compounds
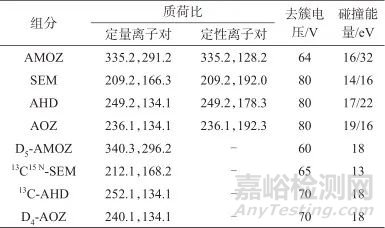
1.3 样品处理
称取鸡蛋、虾、鱼等样品各2 g,置于50 mL离心管中,加入0.2 mol/L盐酸溶液10 mL,用均质器以10 000 r/min均质1 min,加入100 ng/mL混合内标溶液0.05 mL,再加入0.1 mol/L 2-硝基苯甲醛溶液100 μL,涡旋混合30 s后,置于37 ℃恒温箱中反应2 h,取出离心管,冷却至室温,加入0.3 mol/L磷酸钾溶液1 mL,用2.0 mol/L氢氧化钠溶液调节pH为7.2~7.6,再加入10 mL乙酸乙酯振荡10 min提取,再以8 000 r/min离心5 min,取乙酸乙酯层于40 ℃下用氮气吹干,残渣用0.1%甲酸水溶液1 mL 溶解,再用3 mL乙腈饱和的正己烷液液分离去除脂肪,下层水相过0.22 μm滤膜,用液相色谱-串联质谱法测定。
1.4 溶液配制
混合标准储备溶液:量取AMOZ、SEM、AHD、AOZ混合标准溶液0.1 mL,置于100 mL容量瓶中,用甲醇稀释至标线,制成100 ng/mL的混合标准储备溶液。
混合内标溶液:量取D5-AMOZ、13C15 N-SEM、13C-AHD、D4-AOZ混合标准溶液0.1 mL,置于100 mL容量瓶中,用甲醇稀释制成100 ng/mL的混合内标溶液。
系列混合标准工作溶液:分别取混合标准储备溶液0.005、0.01、0.02、0.05、0.1、0.2、0.5 mL,置于50 mL离心管中,加入混合内标溶液0.05 mL,制成质量浓度分别为0.5、1、2、5、10、20、50 ng/mL的系列混合标准工作溶液,质量浓度分别为0.5、1、2、5、10、20、50 ng/mL,内标物质质量浓度均为5 ng/mL。
1.5 实验方法
将样品溶液与系列混合标准工作溶液注入高效液相色谱-串联质谱仪,在1.2仪器工作条件下检测,建立各代谢物的线性方程并以内标法计算样品中的化合物含量。
2、 结果与分析
2.1 样品处理方法的优化
2.1.1 衍生化温度的选择
GB 31656.13—2021《水产品中硝基呋喃类代谢物多残留的测定》、GB/T 21311—2007《动物源性食品中硝基呋喃类药物代谢物残留量检测》、农业部783号公告-1-2006《水产品中硝基呋喃类代谢物残留量的测定》等国家标准中样品制备条件均为37 ℃衍生化16 h,耗时较长。首先考察衍生化16 h不同温度(25、37、60 ℃)对衍生化效率的影响,不同温度条件下硝基呋喃化合物的衍生化的效率如图1所示,从图1可以看出,衍生效率无显著性差异。因此选择37 ℃作为衍生化温度。
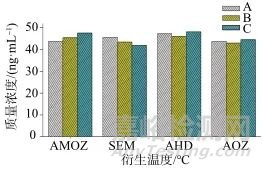
图1 不同温度下硝基呋喃化合物的衍生化的效率
Fig. 1 The efficiency of derivatization of nitrofuran compounds in different temperatures
A—25 ℃;B—37 ℃ C—60 ℃
2.1.2 衍生化时间的选择
考察温度37 ℃时,不同衍生时间(0、0.5、1、2、4、8、12、16、24 h)对衍生化效率的影响,不同时间下硝基呋喃化合物的衍生化效率如图2所示,从图2可以看出,不同时间的衍生效率接近,无显著性差异,为了实验结果可控高效,选取在37 ℃下衍生2 h。
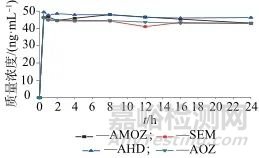
图2 不同时间下硝基呋喃化合物的衍生化的效率
Fig. 2 The efficiency of derivatization of nitrofuran compounds in different long-term
2.2 基质效应
选取鸡蛋、虾、鱼3种阴性基质样品,按照1.4方法配制基质标准曲线溶液,在1.2仪器工作条件下测定,并绘制含基质样品的标准曲线。将3种典型基质匹配的标准曲线的斜率(ki)与不加基质样品配制的标准曲线的斜率(kn)进行比较,斜率的比值见表2,不同基质样品中4种硝基呋喃代谢物的色谱图如图3所示。斜率比值越接近1,说明基质效应越小。由表2、图3可知,斜率比值为0.884~1.033,4种代谢物的测定没有受到基质样品的干扰,说明该方法的基质效应较小,可直接采用不含基质的标准溶液进行定量分析样品。
表2 基质效应结果
Tab. 2 Results of matrix effect

注:ki—含基质的标准曲线的斜率; kn—不加基质的标准曲线的斜率。
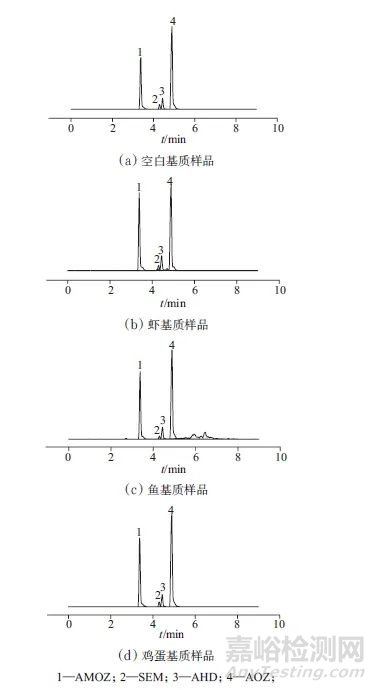
图3 不同基质样品中4种硝基呋喃代谢物的色谱图
Fig. 3 Chromatogram of four nitrofuran metabolites in different samples
1—AMOZ;2—SEM;3—AHD;4—AOZ;
2.3 线性方程、检出限与定量限
按1.3方法配制系列混合标准工作溶液并绘制标准曲线,按照3倍信噪比对应的质量浓度为检出限,10倍信噪比对应的质量浓度为定量限。
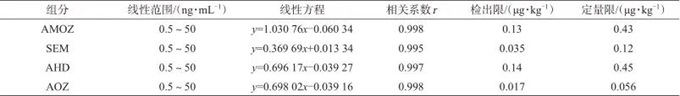
硝基呋喃代谢物的线性范围、线性方程、相关系数、检出限与定量限见表3,由表3可知,AMOZ、SEM、AHD、AOZ在质量浓度在0.5~50 ng/mL范围内与色谱峰面积线性关系良好,相关系数均不小于0.995。
表3 硝基呋喃化合物的线性范围、线性方程、相关系数、检出限与定量限
Tab. 3 Linear range,linear equation,correlation coefficient,detection limit and quantification limit of nitrofuran compounds
2.4 加标回收与精密度试验
称取鸡蛋、鱼、虾等阴性样品各2 g,分别加入100 ng/mL混合标准储备溶液0.02、0.05、0.1 mL (分别相当于2、5、10 μg/kg的硝基呋喃代谢物),加入100 ng/mL混合内标溶液0.05 mL,按照1.3方法处理,在1.2仪器工作条件下测定样品中的残留量,加标回收与精密度试验结果见表4,由表4可知,以上三种基质样品中加标回收率为88.71~105.16 %,测定结果的相对标准偏差(RSD)为3.12~9.08%(n=6),表明该方法准确度良好。
表4 加标回收与精密度试验结果
Tab. 4 Results of spiked recovery and precision test

2.5 稳定性试验
将衍生化后的系列混合标准工作溶液放置2周,分别在第1、2、3、4、5、7、10、14天测定样品。4种代谢物的稳定性试验结果见表5,由表5可知,该方法在14天内稳定性良好,检测样品时可将衍生化对照品放置保存,可减少检验工作量和成本。
表5 稳定性试验结果
Tab. 5 Result of stability test

3、 结语
建立了液相色谱-串联质谱法同时测定不同基质样品中硝基呋喃代谢物残留量的方法,该方法操作简便、快捷、回收率高,可同时测定鸡蛋、虾、鱼等农副产品中的硝基呋喃代谢物。
参考文献:
1 郭添荣,韩世鹤,吴文林,等. UPLC-MS/MS 法快速检测人工养殖淡水鱼中硝基呋喃类代谢物[J].环境化学,2022,41(11):3 534.
GUO Tianrong,HAN Shihe,WU Wenlin,et al. Rapid detection of nitrofuran metabolites in cultured freshwater fish by UPLC-MS/MS[J]. Environmental Chemistry,2022,41(11):3 534.
2 师真,陈俊秀,梁志坚,等.2017-2018年云南省9种新鲜鱼类产品中4种硝基呋喃代谢物的检测[J].食品安全质量检测学报,2020,11(9):2 866.
SHI Zhen,CHEN Junxiu,LIANG Zhijian,et al. Determination of 4 nitrofuran metabolites in 9 fresh fish products in Yunnan province from 2017 to 2018[J]. Journal of Food Safety and Quality,2020, 11(9):2 866.
3 李青青,罗秋水,周强,等.基于信息熵理论的超高效液相色谱-串联质谱法测定淡水鱼肉中4种硝基呋喃类代谢物的残留量[J].理化检验(化学分册). 2023,59(11):1 261.
LI Qingqing,LUO Qiushui,ZHOU Qiang,et al. Determination of residues of 4 nitrofuran metabolitesin fresh water fish by ultra-high performance liquid chromatography-tandem mass spectrometry basedon information entropy theory[J]. Physical Testing and Chemical Analysis(Part B:Chemical Analysis),2023,59(11):1 261.
4 宋军,艾连峰,王敬,等.通过式固相萃取-液相色谱-串联质谱法快速测定中兽药制剂中硝基呋喃类药物[[J].分析科学学报,2021,37(6):807.
SONG Jun,AI Lianfeng,WANG Jing,et al. Rapid determination of nitrofurans in traditional chinese medicine for animals by liquid chromatography-tandem mass spectrometry with a through-type solid-phase extraction[J]. Journal of Analyticals Science,2021,37(6):807.
5 FERANDO R,MUNASINGHE DMS,GUNASENA ARC,et al. Determination of nitrofuran metabolites in shrimp muscle by liquid chromatography-photo diode array detection [J]. Food Control,2017,72:300.
6 李燕,王啸,张祥. QuEChERS-HPLC-MS/MS 测定淡水鱼中硝基呋喃代谢物残留[J].食品与药品,2020,22(5):386.
LI Yan,WANG Xiao,ZHANG Xiang. Determination of nitrofuran metabolites residues in freshwater fishes by QuEChERS combined with HPLC-MS/MS[J]. Food and Drug,2020,22(5):386.
7 唐红梅,曾芳,李成洪.食品中硝基呋喃类药物及其代谢物残留检测的研究进展[J].食品安全质量检测学报,2016,7(10):3 952.
TANG Hongmei,ZENG Fang,LI Chenghong. Progress on the detection of nitrofurans drugs residues and their metabolites in food [J]. Journal of Food Safety & Quality,2016,7(10):3952
8 李艳,徐欣然,吕晓峰,等.液相色谱-串联质谱测定鸡蛋中4种硝基呋喃类代谢物残留[J].安徽农业科学,2019,47(24):199.
LI Yan,XU Xinran,LYU Xiaofeng,et al. Determination of four metabolite residues of nitrofuran antibiotics in eggs by liquid chromatography-tandem mass spectrometry[J]. Jour Anhui Agric Sci,2019,47( 24):199.
9 封腾望,王新新,穆树荷,等.滤过型净化-超高效液相色谱-三重四极杆/复合线性离子阱质谱法测定草鱼肌肉冻干粉中4种硝基呋喃类代谢物[J].食品安全质量检测学报.2022,13(13):4 180.
FENG Tengwang,WANG Xinxin,MU Shuhe,et al. Determination of 4 kinds of nitrofuran metabolites in grass carp muscle lyophilized powder by pass-through cleanup-ultra performance liquid chromatography-triple quadrupole/compound linear ion trap mass spectrometry[J]. Journal of Food Safety and Quality,2022,13(13):4 180.
10 李仲超.液相色谱-质谱同时测定水产品中78种兽药残留[J].食品科学,2014,35(16):217.
LI Zhongchao. Simultaneous determination of veterinary drug residues in aquatic products by liquid chromatography-tandem mass spectrometry(LC-MS-MS)[J]. Food Science,2014,35(16):217.
11 王立丹. QuEChERS结合超高效液相色谱-高分辨质谱法测定畜禽产品中兽药残留的研究[D].广州:华南理工大学,2019.
WANG Lidan. Determination of veterinary drug residues in live stock and poultry products by QuEChERS combined with ultra performance liquid chromatography-high resolution mass spectrometry[D]. Guangzhou:South China University of Technology,2019.
12 吕珍珍,程泷,李昌松,等. UPLC-MS/MS法同时测定不同动物源性食品中硝基呋喃代谢物残留[J].食品工业科技,2020,41(12):245.
LYU Zhenzhen,CHENG Long,LI Changsong,et al. Simultaneous determination of nitrofuran metabolite residues in different animal derived foods by UPLC-MS/MS[J]. Science and Technology of Food Industry,2020,41(12):245.
13 张艺蓓,岳田利,乔海鸥,等.陕西省水产品中4种硝基呋喃代谢物的检测[J].西北农林科技大学学报(自然科学版),2015,43(10):195.
ZHANG Yibei,YUE Tianli,QIAO Haiou,et al. Determination of four nitrofurans metabolites residues in aquatic products in Shanxi Province[J]. Journal of Northwest A & F University (Natural Science Edition),2015,43(10):195.
14 赖年悦,钱继银,方凯,等.基于胶体金免疫层析法快速筛查水产品中的药物残留[J].安徽农业科学,2013,41(26):10 817.
LAI Nianyue,QIAN Jiyin,FANG Kai,et al. Rapid screening of drug residues in aquatic products based on colloidal gold immunochromatographic assay[J]. Journal of Anhui Agricultural Sciences,2013,41(26):10 817.
15 WANG Quan,LIU Yingchun,WANG Mingyan,et al. A multiplex immunochromatographic test using gold nanoparticles for the rapid and simultaneous detection of four nitrofuran metabolites in fish samples [J]. Analytical and Bioanalytical Chemistry. 2018,410 (1):223.
16 XU Z L,SHEN Y D,SUN Y M,et al. Novel hapten synthesis for antibody production and development of an enzymelinked immunosorbent assay for determination of furaltadone metabolite 3-amino-5-morpholinomethyl-2-oxazolidinone[J]. Talanta,2013,103:306.
引用本文: 邢海艳,孙丽,吴旭,等 . 液相色谱-串联质谱法测定不同基质样品中硝基呋喃代谢物残留量[J]. 化学分析计量,2024,33(7):101. (XING Haiyan, SUN Li, WU Xu, et al. Determination of nitrofuran metabolite residues in different samples by liquid chromatography tandem mass spectrometry[J]. Chemical Analysis and Meterage, 2024, 33(7): 101.)

来源:化学分析计量


