您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-08-26 08:38
鼻腔给药既可以实现局部暴露,也可以达到全身系统给药的目的。鼻腔是空气吸入的主要路径,空气中可以携带颗粒、液体或气体。另外,鼻子还有两个额外功能,嗅觉和通过加热、加湿和过滤进入的气流以保护肺部。大的和/或有刺激性的颗粒或飞沫会引发反射性喷嚏,从而被排出,避免肺部沉积或全身吸收。然而,如果有合适的制剂和递送装置,药物可以局部吸收或通过鼻粘膜进入系统循环,从而实现治疗目的。未被鼻子吸收的小颗粒物可被吸入肺部,或在肺局部起作用,或被吸收到系统循环中,或通过粘液纤毛清除和巨噬细胞摄取清除。进入鼻腔的液体,既可以在鼻腔内吸收,也可以被吸入递送至肺部。较大的吸入颗粒物也有机会被胃肠道清除。这些颗粒或液滴附着在鼻子里的粘液上,被纤毛推向鼻子后部,排入鼻咽,最终被吞咽到食道和胃中。除了从鼻子中清除药物外,这种机制还可能导致药物通过胃肠道实现系统暴露。因此,鼻内给药是个局部和全身吸收共存的给药途径,既可以产生预期的药理作用,也可能因为非预期的暴露出现毒性反应。
鼻腔给药有很多优势,给药简单、无创、允许大多数患者(包括恶心或呕吐的患者)自行用药。而且,除了直接递送至鼻内,还可以实现多种靶部位的药物暴露。比如已上市的鲑鱼降钙素和催产素鼻喷可以实现系统治疗的目的,舒马曲坦和唑米曲坦则可以通过鼻腔给药实现入脑治疗偏头痛。鼻粘膜与大脑位置很接近,可以实现大脑和/或脑脊液中药物的快速暴露。还有些在开发的药物则通过鼻内给药实现靶向肺部组织的目的。由于相对较大的血管表面积,分子量<1 kDa的亲脂性药物非常容易被吸收,系统暴露甚至达到与静脉注射(IV)途径相似。言外之意,很多经鼻给药的药物可以实现比经口给药更高的生物利用度、更好的耐受性。毕竟,经鼻给药没有首过消除。
与任何途径一样,经鼻给药也有其局限性。大分子,如许多蛋白质、肽(>1kDa)和亲水性药物往往经鼻吸收很差,主要受限于鼻腔黏膜纤毛快速清除。当然,有企业在开发粘膜粘合剂和渗透增强剂以促进这类药物的吸收。经鼻给药另外一个缺点是虽然无首过效应,但鼻子也是个代谢活跃的器官,有些药物在鼻腔环境中被代谢。此外,鼻腔毕竟是暴露在外部环境的,而且受生理条件影响,吸收变异可能会比较大。
所幸动物在鼻解剖学和生理学方面与人体相似,通过动物药理学和毒理学研究,可以比较容易推断人体情况。因此,可以用动物对制剂、粒径大小、通气量、给药体积和/或暴露位置等进行研究,实现经鼻给药后局部或全身靶组织暴露的目的。
鼻解剖学和生理学
在所有哺乳动物中,鼻中隔将两个鼻腔分开。空气通过鼻腔(鼻孔)流入前庭,到达鼻前房。前庭有起支持和保护功能的角质化的复层鳞状上皮。前庭体积小(人体约0.6 cm3),血管少,渗透性差。在前庭之后,空气流入中庭,气流速率在该区域下降。中庭具有与前庭相似的功能。一旦空气通过中庭进入鼻子的主腔,就会到达一个具有血管丰富、渗透性强和表面积大特点的区域(人体约130 cm2)。鼻呼吸区的主要细胞类型为杯状细胞、假复层纤毛柱状上皮和基底细胞等。杯状细胞产生粘液,而纤毛上皮细胞将粘液推向鼻咽远端(粘液纤毛清除)。基底细胞充当祖细胞。这三种细胞类型位于回旋褶皱,即鼻甲上,限制气体流动,使吸入的空气与呼吸道上皮之间紧密接触。这个区域是大多数药物进入血液的主要入口。
鼻内的血管、淋巴管、神经和腺体对药物递送也很重要。动脉是以与吸入气流相反的方向向前流动,可以达到对吸入空气加温和加湿的作用,其中克氏丛(Kiesselbach’s plexus)区域作用最为明显。该区域鳞状上皮细胞逐渐向呼吸上皮细胞转化,大多数亲脂性药物在此处被吸收。克氏丛是一个高度血管化的区域,包含无瓣静脉、有孔毛细血管和多孔内皮基底膜,这些基底膜会对神经、机械、热、心理或化学刺激做出反应,继而改变血容量,并导致药物吸收速率的快速变化。同样,浆液腺和浆膜粘液腺的分泌物可以在副交感神经的控制下分泌大量液体和粘液,对药物吸收产生重要影响。此外,脂溶性药物可以通过淋巴管吸收。淋巴管排入周围的淋巴结,与鼻腔相关的淋巴组织一起,作为识别和消除病原体的重要部位。淋巴管也可以作为鼻腔吸入疫苗的抗体产生部位。
鼻子主要由嗅觉神经、三叉神经和面部神经三种颅神经的分支支配。面部神经的传出纤维控制着该区域的肌肉,但对于药物递送来说,影响副交感神经纤维比较重要,因为其可以刺激鼻腺粘液分泌和血管舒张,从而显著影响药物吸收。三叉神经是头部和面部的主要神经,其传入分支负责机械疼痛/触摸疼痛和对温度的感觉。三叉神经末梢没有覆盖上皮层,从而允许挥发物和小颗粒直接接触神经元受体。对于药物递送,这一点非常重要,因为这些受体与药物和制剂的耐受性/刺激性有关。最后,嗅觉神经从嗅球通过鼻子最接近颅侧的筛状板进入鼻子。许多药企将该神经作为药物通过鼻子进入大脑的重要路径。
鼻解剖结构的种属差异
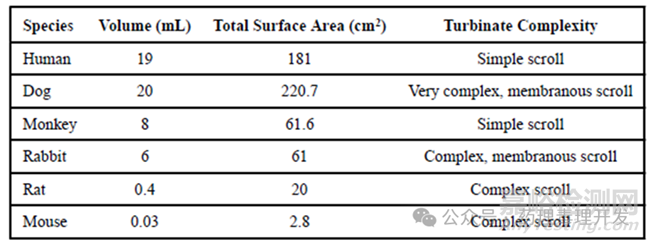
尽管哺乳动物鼻子的解剖和生理在不同物种之间基本相似,但还是存在一些差异。在将药物输送到鼻腔以及解释毒理学研究结果时,需要考虑鼻腔结构和功能的种属间差异。例如,人类和非人类灵长类动物的鼻甲结构简单,而小鼠、大鼠、兔子和犬的鼻甲结构相对复杂。鼻甲的数量和形状会影响气流特征,进而影响药物的沉积。鼻甲结构也可以产生较大的表面积,从而影响药物吸收。下表显示了不同种属鼻子的相对体积、表面积和鼻甲复杂性。表面积值比较关键,用于经鼻毒性研究中的剂量标准化,类似于全身给药的体重或体表面积的使用。
毒理研究中的药物递送和装置
很多种因素包括递送装置、体积、麻醉、给药方法等均会影响药物的经鼻吸收。对于小型啮齿类动物(大鼠和小鼠)药理学和毒理学试验,通常采用移液器滴鼻的方式给药。给药应与吸气相一致,以便通过毛细管作用将溶液吸入鼻孔,同时将动物保持直立。不要将移液器尖端插入鼻孔或离动物太近,以防对动物造成损伤,尤其是重复给药毒性试验,更应注意。这种方式给药尽量保证不同组别间更换移液器的头,预防污染。也可以递送更大剂量,但为了实现最佳全身吸收,总递送剂量应拆分成更小的液滴,少量多次给药,液滴大小如下表所示。每滴给药后,在下一滴给药前暂停约3-5秒,将有助于防止液体积聚和吞咽,从而提高药物的吸收。如果动物在给药时排出或打喷嚏,应记录下来,但通常不会重新给药,尤其是在长期毒理研究中。每次给药完成后,应将动物头部保持向后倾斜的位置约5-10秒,以防止药物从鼻孔中流出。啮齿类动物鼻腔给药通常耐受性很好,但如果给药频率超过每天三次,则可能会出现体重减轻和鼻腔刺激。
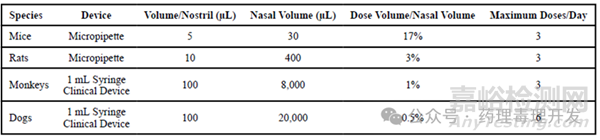
非啮齿类动物鼻腔体积大,可以借助注射器滴入,也可以使用临床装置如液体泵、干粉装置进行鼻内给药。当然,动物试验是不强制要求采用与临床完全一样的装置给药的。犬和灵长类通常是一名技术人员固定动物,另外一名技术人员负责给药。不过,犬比较容易操作,耐受性通常也不错。但灵长类操作起来就会更有挑战一些,而且比较容易产生应激,因此需要限制每天给药体积和给药次数,如上表所示。
影响药物沉积和吸收的因素很多,包括与设备直接接触、给药溶液浓度、极端pH、冷的液体等。这些化学和机械因素可能会引起刺激、分泌物、撕裂、瘙痒、打喷嚏、出血和疼痛,所有这些都会导致药物吸收减少。
如果使用鼻腔喷雾剂降低药物粒径,潜在会促进药物吸收,并可能增加药物在肺部的分布。另外,通过增加给药体积,也能增加药物在肺部的暴露。当然,前文也提到过,经鼻吸入的药物可以通过海绵窦/静脉窦/颈动脉壁/血脑屏障,或淋巴通路/嗅觉神经/三叉神经周围的血管空间进入大脑。
制剂
为实现不同解剖部位(系统循环、肺和大脑)暴露的目的,增强药物在鼻子中的持久性和吸收,制剂的改进也很关键。水溶液和干粉类制剂已经有很多上市产品。但新型聚合微球和纳米颗粒,在改善暴露方面可能更具优势。另外,为了提高水溶液的耐久性和渗透性,已经使用了合成的表面活性剂、胆盐、磷脂和环糊精,同时也探索了胶束、脂质体和各种乳液用于类似目的。对于干粉类制剂,已经在尝试使用生物粘合剂和其他降低药物清除率的制剂。
经鼻给药的毒理设计
目前没有专门针对经鼻给药的非临床研究指导原则,可以参考一些通用型指南比如ICH M3(R2)、ICH S6(R1)和FDA改剂型或给药途径的相关指南。通常来讲,给药途径、给药浓度、给药方案(持续时间和频率)需要与临床拟用方案相似或超出。但是,出于动物福利方面的考虑,经鼻给药非临床研究中达到充分的剂量倍数、或相似的给药频率可能会有些挑战。不过,药物浓度至少要与临床拟用产品相当或更高。除非药物溶解度达不到,给药倍数可以按照鼻内相对表面积换算(参照前文表格),达到临床拟用剂量的10-20倍。可以少量多次给药以达到更高的日给药总量(total daily dose)。 种属选择方面,根据相关动物种属情况,常见组合是大鼠+犬或大鼠+非人灵长类。当然,如果是已上市产品改剂型,通常仅在一种最相关种属中开展经鼻重复给药毒性研究是可以接受的。
动物数量方面并无特殊,与其它系统给药路径相似。对照组设置方面,正常设置一组vehicle对照即可,但如果制剂中含有之前未使用过的新型辅料,则建议增加一组buffer对照。如果药物经鼻给药的目的是实现肺部暴露,建议额外增加每组动物数,原因是为实现药物吸入和肺部充分暴露,往往需要对动物进行深度麻醉,可能会出现动物死亡的情况。当然,对于药物粒径小于5μm的制剂,实现肺组织暴露相对容易,不涉及麻醉,上述风险就低很多。
毒理终点方面,除标准毒理要求的体重、摄食量、临床观察、临床病理学、眼科检查、尸检、器官重量、组织病理学等以外,经鼻途径的药物还需要进行某些特定评估。比如临床观察,需要特别关注给药部位的情况。另外,据报道,鼻内暴露于化合物后,可能会对嗅觉功能产生影响,包括嗅觉缺失,也需要进行评估。简单的嗅觉测试如埋藏食物搜寻测试。也有些更复杂和灵敏的测试,比如嗅觉上皮产生的负电位可以在类似于眼睛视网膜电图的嗅觉电图中测量。
前文已有提及,鼻子中的疼痛受体是没有被鳞状上皮覆盖的,经鼻递送的药物几乎直接进入自由神经末梢,并可能导致上呼吸道刺激。如果药物潜在产生刺激作用,则可以评估刺激效力。三叉神经刺激会导致小鼠呼吸模式的特征性变化,这些变化可以用头外置式体积描记系进行评估,并可参考美国标准测试方法(ASTM 981-04, 2012)。
经鼻给药毒理学研究中特别重要的是鼻腔的组织病理学评估。通常情况下,在对鼻骨进行脱钙后进行四次或多达六次鼻腔切片。这一过程通常会增加一两周的病理处理时间。同样,应该对大脑的嗅觉区域进行额外的评估,特别是药物具备中枢活性。除了通常用于组织病理学的标准三个切片外,建议再增加2-4个切片。由于经鼻给药也会导致药物暴露于口咽、喉、气管、肺、食道和胃,因此在病理学评估中应特别关注这些部位的组织或器官。此外,如果下颌下、支气管和纵隔引流淋巴结肿大,也要进行相应评估。
鼻腔和大脑以及上述其他组织通常用苏木精和伊红染色。如果出现问题,建议对嗅上皮和嗅球进行特殊染色评估。如果存在粘液增生,阿利新蓝(pH 2.4)和周期性酸-希夫染色可以突出粘液产生细胞。嗅觉纤毛中发现的嗅觉受体神经元标记物嗅觉标记蛋白(OMP)和腺苷酸环化酶3(AC3)也可能有用。也可以使用几种嗅觉特异性较低的神经元标记物,例如β-tubulin, fluoro-jade, silver stain和caspase 3.
鼻粘膜中常见的供试品相关或背景发现包括:纤毛缩短(吸收)或缺失、上皮细胞去分化、增生/化生、粘液(杯状细胞)增生/化生、嗜酸性粒细胞包涵体/液滴、炎症、粘膜水肿、变性、萎缩、坏死、鼻甲溃疡和骨质增生。值得注意的是,粘液细胞(杯状细胞)增生和嗜酸性粒细胞包涵体/液滴是啮齿动物毒理学研究中的常见发现,可能与人类病理学无关。

来源:药理毒理开发


