您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-09-03 08:27
摘 要
模型引导的抗菌药物剂量优化在抗菌药物的研发及上市后变更给药方案中具有重要价值。国内抗菌药物在应用模型方法支持剂量优化时,经常出现缺乏充足可靠数据、缺乏对特殊人群给药方案探索等问题。本文根据作者实际工作经验,结合模型引导剂量优化在抗菌药物应用中的具体案例,对模型引导剂量优化在创新抗菌药物研发、特殊人群给药方案选择及上市后给药方案变更中的相关问题进行讨论,以期为国内抗菌药物研发及上市后给药方案的选择提供参考。
抗菌药物是临床应用范围广、品种繁多的一大类药品。随着抗菌药物在临床的大量使用,以及普遍的抗生素滥用,临床上耐药菌株越来越多。根据世界卫生组织(WHO)预测,到2050年,多重耐药菌和泛耐药菌将导致1000万人死亡,超过癌症。
合理的给药方案对预防抗菌药物耐药性的发生至关重要,也是新抗菌药物研发中的重要内容。抗菌药物作用特点是杀灭或抑制入侵到机体内的外来病原菌而发挥药理效应,其疗效取决于抗菌药物、病原菌和机体三者相互作用的结果。药代动力学(PK)/药效学(PD)研究是将药物浓度与时间、抗菌作用结合起来,阐明抗菌药物在特定剂量/浓度和特定给药方案下抑菌或杀菌效果的时间过程。利用抗菌药物的PK/PD特性建模可以支持给药方案的优化,减少药物不良反应和耐药性的出现。随着定量药理学的发展及模型引导的药物研发理念在创新药中的应用,模型引导的剂量优化方法在抗菌药物中的应用越来越普遍。近年来,国内外上市的创新抗菌药物,均在一定程度采用模型引导的剂量优化。
目前在对国内抗菌药物的审评及沟通交流中,发现采用PK/PD模型推测给药方案时,往往存在预测人体目标给药方案考虑不足、缺乏特殊人群给药方案、已上市品种变更给药方案无充足可靠数据支持等问题。本文主要结合国际审评案例、国内审评及沟通交流中的常见问题对抗菌药物给药方案的选择提出几点思考,以期为国内抗菌药物研发及上市后优化给药方案提供参考。
1、国内外监管机构相关要求
国内及欧洲药物管理局(EMA)分别发布了《抗菌药物药代动力学/药效学研究技术指导原则》和《Guideline on the use of pharmacokinetics and pharmacodynamics in the development of antimicrobial medicinal products》指导PK/PD模型在抗菌药物研发中的应用。上述指南中均说明可基于PK/PD研究,通过模型引导的药物研发方法,为抗菌药物各期临床试验给药方案的制定、抗菌药物群体量效关系的探索、特殊患者群体和特定患者个体给药方案的调整等提供支持性数据。
根据国内外发布的抗菌药物PK/PD研究技术指导原则,抗菌药物PK/PD研究策略主要包括如下内容:①根据非临床阶段的体外或/和体内动物PK/PD研究,初步确定PK/PD指数,并通过体外或/和动物PK/PD研究获得抑菌或杀菌效果所需PK/PD靶值;②结合早期临床获得的PK数据、抗菌药物的MIC分布,进一步完善PK/PD靶值,模拟抗菌药物不同给药方案的达标率(PTA),推荐确证性临床试验的给药方案;③结合确证性临床研究数据,进一步分析完善PK/PD关系,或暴露量/效应关系,制定不同亚群的给药方案、完善说明书等。
2、案例分析
近年来,在抗菌药物的研发过程中,依靠模型引导进行剂量优化越来越普遍。但国内同类产品在给药方案选择中,往往存在模型工具应用不足,影响研发效率的情况。以下案例分别结合醋酸来法莫林上市时剂量优化及注射用头孢他啶/阿维巴坦钠外推儿科患者适应证时剂量优化,对模型引导的剂量优化在抗菌药物中的应用进行分析。
醋酸来法莫林
爱尔兰Nabriva公司的醋酸来法莫林于2019年8月在美国食品药品监督管理局(FDA)获批上市,用于治疗成人社区获得性细菌性肺炎(CABP)。该品种在上市时充分利用了PK/PD模型对给药剂量进行优化,体现在饮食影响、肝功能不全患者给药方案优化及最终上市剂量模拟等方面。
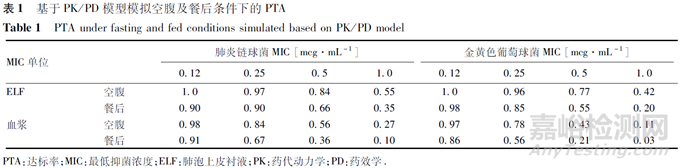
饮食对给药方案的影响 根据片剂食物效应研究的结果,口服本品(空腹与进食对比)的平均峰浓度(Cmax)和药时曲线下面积(AUC0-inf)分别降低22.90%和18.43%,从该数据来看,食物对本品的暴露量影响不大。但基于本品的1次给药间隔的暴露量的差异来算,高脂餐后AUC0-12 h约降低30%。用肺泡上皮衬液(ELF)及血浆PK/PD模型,模拟醋酸来法莫林片在空腹及餐后条件下的PTA,结果如表1所示。按照肺炎链球菌和金黄色葡萄球菌的最低抑菌浓度(MIC)分别为0.50、0.25 mg·mL-1计算,高脂餐后PK/PD的达标率(PTA)小于70%。即食物摄入影响本品的疗效,故本品最终说明书中规定的饮食条件为“在餐前至少1 h或者餐后至少2 h服用”。
肝功能不全对给药方案的影响 根据一项独立的肝功能不全受试者PK研究结果,与肝功能正常的成年人相比,中度和重度肝功能不全受试者成人的总来法莫林的暴露量浓度相似。肝功能不全受试者来法莫林蛋白结合率降低,游离来法莫林的浓度随着肝功能损害程度的增加而增加,与肝功能正常受试者相比,中、重度肝功能不全受试者中游离来法莫林血浆AUC0-inf平均增加2、3倍。因缺乏安全性数据支持3倍以上的游离来法莫林浓度的安全性,对于严重肝功能损害患者需要调整来法莫林注射液的剂量,最终重度肝功能不全患者将XENLETA注射的给药间隔从12 h延长至24 h,该给药方案下,基于PK/PD模拟的PTA大于90%。对于口服给药途径,体内的代谢及转运的影响因素复杂,口服给药后肝损害对来法莫林PK的影响可能大于静脉给药,且无独立研究评价肝功能损害对来法莫林片剂给药分布影响,对于肝功能不全患者未给出剂量调整的建议。
基于PK/PD模型支持上市剂量合理性 关键临床试验完成后,基于来法莫林的群体PK模型,以CFU相对基线减少1个log10相关的中位AUC:MIC比值为目标,采用蒙特卡罗模拟说明书中给药方案的PTA。根据PTA分析,按照拟定给药方案给药后,CABP患者第1天游离血浆及ELF中的药物暴露量均达有效暴露量,达到PK/PD靶值的累积概率约为90%。群体PK/PD模拟结果支持说明书中来法莫林给药方案对感染肺炎链球菌和金黄色葡萄球菌的CABP患者的有效性。
注射用头孢他啶/阿维巴坦钠
EMA于2022年更新发布的《Addendum to the guideline on the evaluation of medicinal products indicated for treatment of bacterial infections to address paediatric-specific clinical data requirements》,说明对于抗菌药物,进行不同年龄段儿科患者的剂量外推时,可通过PK/PD建模和模拟,以及PTA的估计,为儿科患者的给药方案提供额外支持。
美国Pfizer公司的注射用头孢他啶/阿维巴坦钠(CAZ-AVI,Zavicefta)于2016年在EMA获批上市用于治疗成人复杂性腹腔内感染(cIAI)、复杂性尿路感染(cUTI)、医院获得性肺炎和呼吸机相关性肺炎(HAP/VAP)。随后,基于成人患者与儿科患者疾病的相似病理生理学,依靠模型外推方式的方法,外推了3个月~18岁儿科患者的给药方案,外推过程如图1所示。
因不同年龄段患儿的生理条件差异较大,Pfizer在儿科患者研究中,采用逐步递进的研究策略,结合不同年龄段患儿的PK数据不断优化PPK/PD模型,模拟优化儿科患者给药方案。在Ⅱ期研究中,个体模型预测的PTA>94%,但最终试验结果显示,稳态谷浓度(Cmin,ss)相较于模型模拟值,明显降低。基于Ⅱ期研究的Cmin,ss,用模型模拟了CAZ-AVI在MIC为8 mg·L-1时的PTA,模拟结果表明,在各年龄队列中的总体达标率仍能达到90%以上。
值得一提的是,Pfizer在当时申请新增儿科患者适应证时,HAP/VAP儿科患者的PIP试验正在进行。对于HAP/VAP适应证,基于PPK/PD模拟结果获批。

3、讨 论
结合国内外相关指南、国际审评案例、国内沟通交流及审评过程中常见的问题,对抗菌药物给药方案的选择提出以下几点思考。
因只有游离药物才能发挥抗菌作用,药物在组织中的分布、消除取决于游离药物的浓度,故抗菌药物的蛋白结合率有重要的临床意义。PK/PD指数采用游离药物浓度计算。在预测临床给药方案时,需关注非临床动物与人蛋白结合率的种属差异及不同患者人群蛋白结合率的差异;在预测不同患者人群给药方案时,也应关注蛋白结合率的差异。例如:来莫法林在检测不同肝功能人群蛋白结合率时,发现静脉输注本品1 h后,肝功能正常受试者与中、重度肝功能不全患者的蛋白结合率分别为94.8%、89.2%、86.5%,在预测不同肝功能不全患者的给药剂量时,需将该差异考虑在内。
低蛋白血症可使游离抗菌药物浓度升高,从而使抗菌药物的清除率出现不同程度的升高。在估算低蛋白血症等特殊人群的目标剂量时,需考虑到药物蛋白结合率的变异性。对于患有低蛋白血症的危重患者,药物与蛋白结合率的变异性较高,对于该类患者考虑个性化给药更为合理。
抗菌药物要有效地控制感染,必须在感染部位达到有效的抗菌浓度。抗菌药物在不同组织的穿透能力不同,针对不同感染部位使用抗菌药物的目标血药浓度及PK/PD靶值也不同,故检测相应靶组织中的浓度对预测的给药剂量是否合理至关重要。在初步预测临床给药方案时,需关注药物在非临床动物模型与人体中组织穿透力差异。预测不同患者人群的给药剂量时,也应关注靶组织的可能的浓度差异。例如,对于治疗肺部感染和尿路感染的药物,给予相同给药剂量,药物在肺组织及尿路中的暴露量可能存在差异,此时需要结合靶组织中的药物暴露程度,考虑治疗不同部位感染时,给药方案的合理性。
关于儿科患者给药方案,对于具有一定抗菌谱的抗菌药物,基于成人患者与儿科患者疾病的相似病理生理学,可以由成人患者安全有效性数据外推儿科患者的安全有效性。此时,PK/PD模型的可靠性直接影响PTA估算的准确性。采用PK/PD模拟儿科患者剂量时,需关注PPK模型的可靠性。PPK外推时一般按照青少年、小年龄段儿童的顺序逐步进行,即在获得较大年龄段儿童的PK数据后,将数据纳入PPK模型更新后再外推更小年龄段儿童的数据。儿科患者因伦理及现实问题,越小年龄段患儿越难实现密集采血,一般采用机会采血的方法。设计采血点时,需同时关注抗菌药物的PK/PD指数。例如PK/PD指数为%fT>MIC,关注采血点设计能否反映达到最低抑菌浓度的维持时间;PK/PD指数为%fCmax/MIC,关注采血点设计能否反映峰浓度;PK/PD指数为fAUC0-24/MIC时,关注采血点设计能否反映药物在体内的药时曲线下面积。
关于肝、肾功能不全患者的给药方案,肝、肾为人体重要的代谢、排泄器官,肝、肾功能不全会引起主要经肝代谢、肾排泄的药物在体内的蓄积,发生安全性风险。对于主要由肾排泄的试验药物,应明确肾功能不全严重程度和透析对PK的影响。同样,对于主要在肝代谢的试验药物,应考虑在肝功能不全患者中进行PK研究,特别是在肝氧化代谢的试验药物及其代谢物具有药理活性的药物。
由于抗菌素耐药性的增加和新抗生素的短缺,已上市抗生素的给药方案优化对于提高有效性、降低毒性和减少耐药性的出现至关重要。目前已上市抗菌药物申请变更给药方案中,缺乏足够可信的数据支持是审评中最常见的问题。对于采用抗菌药物的PK/PD特性支持给药方案优化提出以下两点思考。
关注PK/PD靶值的可靠性:PK/PD靶值的选择直接影响PTA的估算结果。早期上市的抗菌药物PK/PD靶值通常不明确,例如,对于β -内酰胺类抗生素,使用的靶标在40%~100% fT > MIC和50%~100% fT > 4×MIC之间变化。另外,缺少近年来的临床分离致病菌株的MIC值,也是PK/PD靶值计算时的常见问题。
关注PPK模型的可靠性:患者的PK参数准确可靠,是影响PTA估算结果的另一个重要因素。对于上市较早的药物,往往缺乏充足的患者PK数据,尤其是特殊人群。仅采用文献报道的PK数据建模,缺乏真实数据对模型进行验证,从而影响模拟数据的可信度。此种情况下,可对患者人群进行稀疏PK采血,对模型进行验证,以增加模型可靠性。
模型引导的抗菌药物剂量优化对抗菌药物的开发及使用等具有重要价值。本文结合国际审评案例、国内审评及沟通交流中的常见问题对抗菌药物基于模型研究优化给药方案,提出了以下关注点:关注不同种属及不同患者人群蛋白结合率差异;关注药物在靶组织中的分布情况;关注儿科患者、肝肾功能不全患者与正常患者PK/PD差异;采用PPK模型模拟患者PK数据时,关注PPK模型的可靠性。
本文是基于目前的科学认知、背景调研等提出的相关思考,不代表监管机构的要求。

来源:CJCP临床药理学


