您当前的位置:检测资讯 > 行业研究
嘉峪检测网 2024-09-29 18:05
多肽由氨基酸脱水缩合而成,具有直链或环状结构。迄今为止,已鉴定出7000余种天然多肽,这些多肽在生命活动中不可或缺,扮演着激素、神经递质、生长因子、离子通道配体等至关重要的角色,是维持和调节生物体内各种功能的关键活性物质。
多肽药物的分子量通常介于化学小分子药物(小于500 Da)和蛋白质药物(大于5000 Da)之间,兼具两类药物的优点。就制备方法而言,多肽药物与小分子药物相似,主要通过化学法合成,具有结构精确、质量易于控制、生产成本较低等优点。在药物开发的早期阶段,还可通过化学修饰优化候选药物的亲和力、溶解度、药代动力学特性以及降低毒性;其治疗效果与蛋白质药物类似,具有副作用小、特异性强、疗效好等优势;从适应证上看,多肽药物可用于治疗包括免疫调节、肿瘤和心血管疾病在内的多种疾病。近年来,跨学科和跨领域的融合推动了药物筛选、合成和修饰等关键技术的进步,提高了多肽药物的开发效率与成本效益,并促进其大规模生产和应用。因此,多肽药物已然成为新药研发的重点方向之一。这种趋势预示着一个以肽为核心的新药研发时代的来临。
1、多肽药物开发技术分析
自1922年胰岛素首次在临床应用以来,多肽药物发展已逾百年。20世纪60年代,固相合成技术的诞生引领了该领域的第一次技术革命。80年代后期,重组技术和噬菌体展示技术的出现,进一步推动了更大分子量多肽药物的生产和特定活性多肽的筛选工作。迈入21世纪,天然多肽资源不断丰富,尤其是毒液来源的多肽组学研究以及新化学修饰技术的发展,为新型多肽药物的探索提供了新方向、新动力。此外,多功能肽、偶联肽、口服肽制剂及创新递送系统等先进技术的涌现,促进了多肽药物的多样化发展。目前多肽药物生产已形成化学合成为主、生物合成并重的格局。
1.1 生物合成技术
生物合成是利用生物体内的细胞机制和酶的作用合成多肽,具有定向表达强、成本低的特点,包括天然提取法、酶解法、发酵法、基因重组法等。
1.1.1天然提取法
首个肽药物的分离方法是天然提取法。1921年,Frederick Banting等人首次从动物的胰腺里提取出胰岛素,并用于治疗糖尿病,挽救了数十万人的生命。这一开创性成果显著提升了公众对多肽治疗的关注度。随后,促肾上腺皮质激素和降钙素等其他动物源性多肽药物也成功进入临床应用。此外,毒素和毒液也被视作药物研发的天然资源,具有巨大潜力和前景。其他天然产物,如环状肽和抗菌肽也受到了科学界的关注,目前正在进行更深入的研究与开发。然而,天然产物通常存在成分复杂、活性组分含量少等多重问题,导致天然提取法的产量很低,价格较高。
1.1.2 酶解法
酶解法通过生物酶将大分子蛋白质降解为活性多肽,能有效保留蛋白质原有的营养价值,具有绿色健康的优点。但酶解法所得产物是系列多肽的混合物,难以实现特定序列的精准合成,且伴随产量低、环境负担及产品质量不稳定等难题。因此,酶解法在药物研发领域的应用并不普遍,多被应用于食品、化妆品、饲料等行业。
1.1.3 发酵法
发酵法通过微生物代谢生产天然多肽,其生态友好性已经得到了充分证明。目前,通过发酵法独立合成多肽的产业化案例较少,应用范围较窄,主要包括ε-聚赖氨酸、γ-聚谷氨酸和蓝细菌肽等,其优势在于成本较低,未来可期。
1.1.4 基因重组法
基因重组法是指通过基因工程技术,将编码多肽的基因导入适当的表达系统中,构建重组DNA表达载体,并在原核或真核细胞中进行多肽分子的表达、提取等。基因重组法能够合成具有确定序列的肽,被广泛应用于制备难以通过传统化学合成方法获得的肽类,如具有多个二硫键的长肽或复杂肽。近年来,随着基因工程技术趋于完善,基因工程类多肽药物的研制及临床应用的步伐明显加快。
1.2 化学合成技术
以化学方法为基础的肽合成技术已有百年历史,化学合成法具有研发周期短、生产成本低等优点,可分为液相合成法和固相合成法,两者主要区别于是否使用固相载体。
1.2.1 液相合成法
液相合成法最早由Emily Fischer于1920年开发,她利用此方法成功合成了第一个二肽——甘氨酰甘氨酸。液相合成肽的过程包括以下关键点:(1)基团保护:选择性保护一个氨基酸的氨基端和另外的氨基酸或短肽的羧基端以及不参与反应的侧链基团;(2)基团活化:为提高反应效率,需对参加反应的氨基酸或短肽的羧基进行活化。常用的活化试剂包括活化酯、活化羧酸和活化酮等;(3)缩合反应;(4)分离纯化:将未完全反应的原料、活化剂、副产物等杂质分离除去得到纯化多肽产物。
液相合成肽领域早期的研究核心是寻找温和的氨基酸保护基团,在不断开发新保护方法的同时,羧基活化和偶联领域也持续创新。然而,随着氨基酸残基数量的增加,溶解和纯化技术难度加大,该方法合成长链多肽的效果并不理想。
1.2.2 固相合成法
1963年Bruce Merrifield开发了固相合成法,该方法简化了多肽合成流程,克服了液相合成的局限性,吸引了制药行业的极大关注。固相合成法可简单刻画为:(1)先将多肽序列C端的第一个氨基酸的羧基通过共价键附着在固体聚合物(树脂+连接分子)上;(2)以此氨基酸作为氨基组分,脱除保护基团后与活化后的羧基组分反应缩合;(3)通过重复脱除保护、缩合、洗涤等过程按序添加氨基酸,合成所需长度的肽链;(4)利用化学反应将肽链从树脂上切割下来,同时脱除所有保护基团,经高效液相纯化处理后,即可得到所需的多肽。该过程易于实现自动化处理,降低了提纯难度和时间成本,实现了产品收率和纯度双提高。目前,固相合成法是多肽化学合成的主流方法,其主要问题在于需要大量昂贵的树脂,在一定程度上增加了生产成本。
实际生产中,需综合考虑目标多肽的长度、复杂性、所需纯度和生产规模等选择合适的多肽合成方法。通常,对于10个以下氨基酸缩合成肽,液相合成法成本较低,更为合适;10—50个氨基酸缩合成肽,固相合成法成为首选;合成较长的多肽链(30个以上氨基)采用生物法更佳。经过多年发展,多肽药物合成技术早已趋于多样化、产业化发展,但仍面临一些关键技术难题,需要科研人员不断攻克以构建更加完善的技术体系。
1.3 多肽药物开发的关键技术难点
肽的性质取决于其氨基酸组成、构象、化学基团等。多肽药物开发过程中,往往需调整电荷分布、等电点、制剂pH值及浸润性处理等;此外多肽类药物通常伴有半衰期较短、血浆清除率较高等缺陷,需要增强抗酶解能力以提高其体内稳定性、增加其流体力学半径以减少肾小球的滤过作用。上述结构修饰过程具备较高的技术壁垒和经验壁垒。此外,计算机辅助药物设计是提升研发效率的关键手段,但能够精通此法的企业仍在少数。
合成纯化方面,随着肽链长度的增加、结构及化学修饰复杂程度不断提高,单一的合成方法越来越不能满足生产需求。对于生产商来说,高效整合多种工艺或者开发新技术也是难点。此外,合成步骤的增多会叠加放大各环节产生杂质的种类和量级,为此每个环节需要根据纯度等质量研究情况多次反馈调整,导致其生产经验性强,工艺中技术诀窍多,合成风险骤增,进一步抬高了技术壁垒。
给药途径和新剂型方面,相比传统的皮下、肌肉和静脉注射给药,口服给药更能有效提高患者的依从性,但多肽的口服生物利用度会因系列化学和酶屏障而降低,如肽可在胃的低pH中被化学降解,也可被胃肠道中的消化酶降解,其中肠黏膜层是限制其口服的最大障碍,这对工艺制造有着较高要求,国内厂家目前还处于初级阶段。
综上,复杂的研发流程和技术壁垒导致多肽药物行业竞争缓和,是个极具差异化的潜力赛道。
2、多肽药物市场格局分析
2.1 行业与市场分析
随着合成方法的不断改进,多肽药物的市场规模和经济价值稳步增长,迎来战略机遇期。据弗若斯特沙利文数据,预计2030年全球多肽药物市场规模将达到2108亿美元,其中,中国市场规模占全球比重维持在15%左右(如图1所示)。多肽药物市场中,糖尿病、肿瘤、罕见病是拉动市场扩容的“三驾马车”。
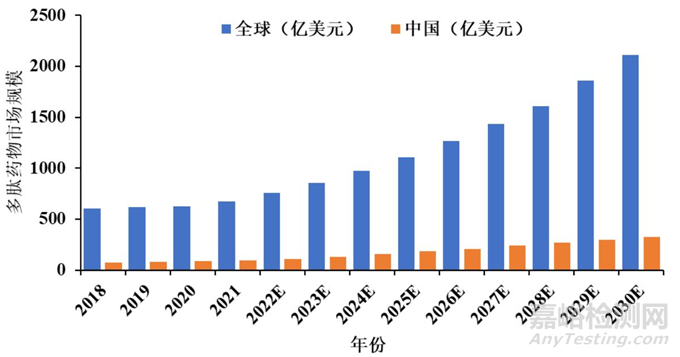
图1 2018—2030年全球多肽药物市场规模及预测
Source: Frost& Sullivan / Insight.
2.1.1 控糖/减肥领域
糖尿病发病率及肥胖率逐年提升,降糖治疗具备长期、刚需属性,但市场对疗效好、安全性高的控糖/减肥药物的需求远未得到满足。
胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂(receptor agonist,RA)在临床试验中显示出卓越的降糖疗效,且低血糖发生风险低;同时通过减少食欲和延缓胃排空等方式帮助患者控制体重,对于肥胖、与肥胖密切相关的非酒精性脂肪性肝炎(Non alcoholic steatohepatitis,NASH)等代谢病的治疗具有重要意义。2021—2022年,全球GLP-1RA市场占比的年复合增长率达到41.5%,其中前两位的明星产品司美格鲁肽(Semaglutide)、度拉糖肽(Dulaglutide)占据全球市场份额82%(如图2);2023年,两者销售额分别达212.01亿美元和71.32亿美元,成为催化多肽药物市场关注度不断提升的主要原因。
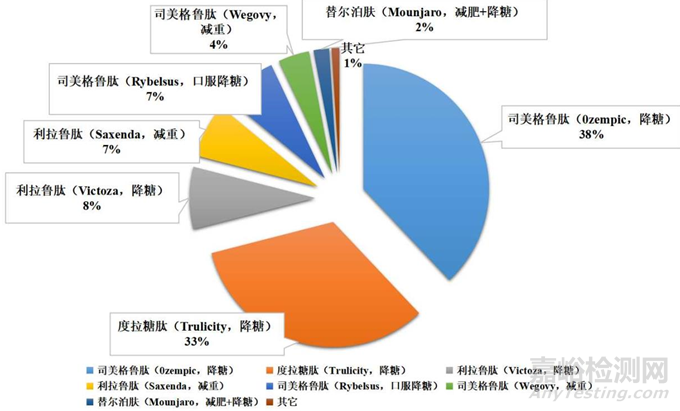
图2 2022年全球GLP-1RA药物的市场份额
Source: Frost& Sullivan /药智网.
截至2023年底,全球已有10款GLP-1RA药物获批上市(表1),主要用于2型糖尿病(Type 2 diabetes,T2DM)的治疗,其中利拉鲁肽(Liraglutide)、司美格鲁肽、贝那鲁肽(Benaglutide)及替尔泊肽(Tirzepatide)获批减重适应证。
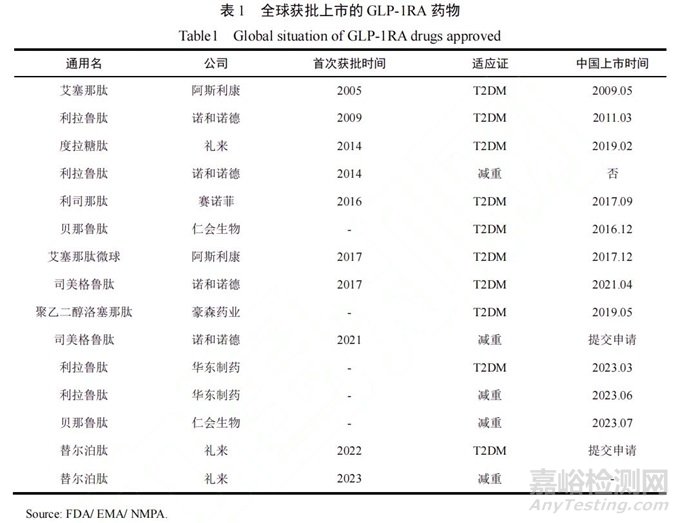
临床数据表明,最新获批的替尔泊肽具有卓越的临床治疗效果,相比于安慰剂,最高能获得20.9%的体重减轻效果。在中国,获批上市的GLP-1RA降糖药物累计有8款,仅贝那鲁肽获批减重适应证,司美格鲁肽已提交减重适应证的新药生产上市申请。目前,我国GLP-1RA药物市场超九成被进口药物占据,仅仁会生物、豪森药业、华东制药三家为本土企业,国产替代道阻且长。
2.1.2 抗肿瘤领域
多肽药物可通过诱导激素去势减缓肿瘤细胞的生长,达到抗肿瘤目的。其中促黄体激素释放激素(Luteinizing hormone-releasing hormone,LHRH)和生长激素抑制素(Somatostatin,SST)类似物是治疗众多癌症的标准疗法。
LHRH类似物是最大的一类抗肿瘤肽,主要包括瑞林类和瑞克类药物。瑞林类药物多通过对天然LHRH的C-端改构或在肽序中增加非天然氨基酸制备,其中戈舍瑞林(Goserelin)、亮丙瑞林(Leuprolide)、曲普瑞林(Triptorelin)占据绝大部分市场份额。由阿斯利康公司开发的戈舍瑞林长期使用可抑制垂体的促黄体生成激素的分泌,从而引起男性血清睾酮或女性血清雌二醇水平下降,停药后可逆,适用于激素治疗的前列腺癌、绝经前期及围绝经期的乳腺癌、子宫内膜异位症,于1987年和1989年分别获欧盟、美国批准上市,2022年全球销售额达到9.27亿美元,位居同类产品第一位。值得一提的是,我国绿叶制药集团基于创新微球技术平台自主研发的2.2类新药——注射用戈舍瑞林微球(百拓维)已于2023年6月底获批,成为全球首个且当前唯一获批上市的戈舍瑞林长效微球制剂,可用于需要雄激素去势治疗的前列腺癌患者;Ⅲ期临床研究数据显示,注射部位不良反应发生率为0,且针头外径仅0.8 mm,相较于植入剂有望降低注射部位疼痛问题,目前已被纳入国家医保药品目录,有望为中国患者带来更显著的临床效益。瑞克类药物主要包括阿巴瑞克(Abarelix)、西曲瑞克(Cetrorelix)、地加瑞克(Degarelix)等,其中地加瑞克是临床上常用的抗前列腺癌药物。但总体而言,瑞克类药物的市场表现不突出。
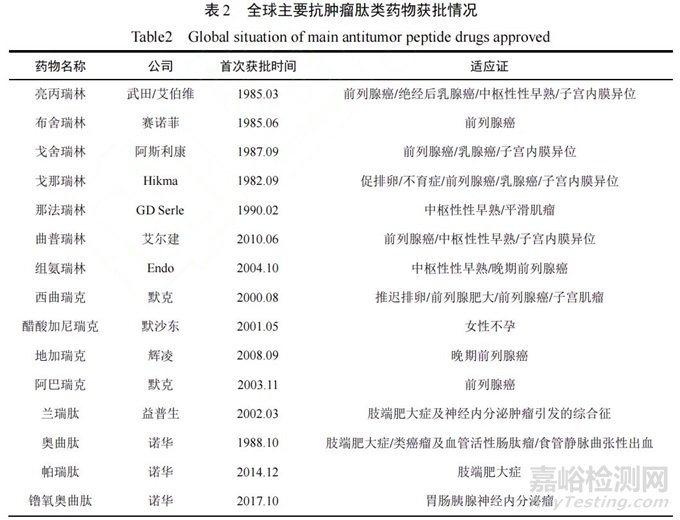
SST几乎对机体所有的生理性内外分泌反应均有抑制作用,能广泛抑制细胞增殖活性。典型药物当属益普生的兰瑞肽(Lanreotide)和诺华的奥曲肽(Octreotide),两者结构类似,均可用于治疗肢端肥大症,2022年销售额均超过10亿美元。2018年,诺华创新性抗癌药镥氧奥曲肽(Lutetium 177Lu dotatate)获美国批准上市,开启了放射性核素治疗肿瘤的新纪元。该药物分子内的奥曲肽可以与肿瘤细胞表面的生长抑素受体结合,同时将放射性镥-177运送到细胞内部,通过发射β射线杀伤肿瘤细胞。全球主要抗肿瘤肽类药物获批情况如表2示。
2.1.3 抗感染和罕见病领域
感染性疾病是当前临床医学面临的重大挑战之一,日益严峻的耐药大环境为抗感染多肽药物的临床开发和应用创造了前所未有的新机遇。
抗菌肽具有杀菌快速、抗菌谱广、毒副作用小、无免疫原性等优点,主要包括脂糖肽、环脂肽等。万古霉素(Vancomycin)是首个问世的糖肽类抗生素,除抑制细菌细胞壁的合成,还可改变细菌细胞膜的通透性,阻碍细菌RNA的合成,对革兰氏阳性菌有强大杀菌效果。据药融云数据库统计,2022年中国注射用盐酸万古霉素医院终端销售额规模近16亿元,其中原研市场占有率近80%。近年来,由于万古霉素系列不良反应、耐药菌等产生,达巴万星(Dalbavancin)、奥利万星(Oritavancin)和替拉凡星(Telavancin)等第二代糖肽类抗生素相继被开发上市。而达托霉素(Daptomycin)作为全球首个获批的环脂肽类抗生素,其抗菌活性高度依赖于钙离子浓度,且在杀灭细菌的同时不会溶解细菌,因此炎症反应相对较轻,是目前治疗革兰氏阳性菌感染的理想药物。值得注意的是,抗菌肽除具有抗微生物作用外,还能通过破坏癌细胞膜上带负电荷分子或线粒体膜诱导肿瘤细胞膜坏死或凋亡。
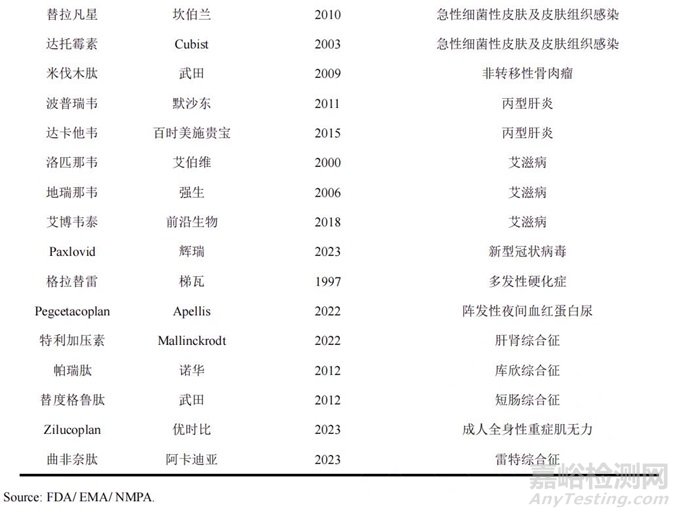
罕见病指发病率非常低的疾病,又被称为“孤儿病”,世界卫生组织将其定义为患病人数占总人口0.65‰~1‰的疾病。罕见病发病率低但种类多,致残率高且可治性低,是危害人类健康特别是儿童健康的重大疾病。多个国家鼓励罕见病治疗药品研发,其中由梯瓦制药研发并于1997年上市的格拉替雷曾是多肽药物中最大的品种,用于治疗多发性硬化症,2016年全球销售额高达42.23亿美元。临床试验证实,醋酸格拉替雷可以降低复发性多发性硬化症患者的复发频率,适用于治疗复发型多发性硬化成人患者,包括临床孤立综合征、复发缓解型多发性硬化和活动性继发进展型多发性硬化。近年来,由于各种多发性硬化症新药和仿制药冲击,格拉替雷市场受到挤压,2022年销售额降至6.91亿美元。同年,阿卡迪亚开发的曲非奈肽(Trofinetide)获得美国批准,主要通过减少神经炎症和支持突触功能,达到治疗雷特综合征核心症状的目的,是全球首个被批准用于治疗该病的药物,具有里程碑意义,在欧洲被授予孤儿药资格认定。全球部分抗感染、罕见病治疗多肽药物获批情况如表3所列。

2.2 研发情况
从学术研究看,总体上多肽药物研究呈现持续性强、热度居高不下的总体态势(如图3所示)。
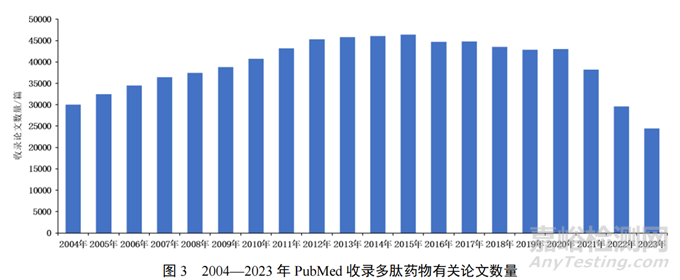
通过“peptide drug”“peptide drugs”“peptide-based drugs”“peptide-based drug”等关键词查询PubMed收录的多肽药物,结果显示:截至2024年3月12日,共计收录多肽药物主题论文达1112962篇,其中近二十年论文数量高达788195篇,占比约70.82%。2004—2013年和2014—2023年两个十年间分别收录384633、343819篇,并在2013—2015三年达到最高峰,其间利拉鲁肽、度拉糖肽、司美格鲁肽先后上市,也引发了一波热潮。近年来,有关研究论文数量有所回落,可能存在两方面原因:一是行业关键技术壁垒已然形成,一定程度上阻碍了科技界的研究热情;二是多肽药物的创新靶点研究基本成型,研究者更多关注产业化、商品化等工程问题,影响了以论文为代表的基础研究成果产出。
2.2.1 GLP-1RA及其多靶点药物
随着全球GLP-1RA多肽药物市场规模、份额快速攀升,国内外企业积极抢占GLP-1RA新赛道,围绕长效化、口服制剂、多靶点协同、适应证拓展以及联合疗法等未来趋势,密集谋划研发布局。例如,为克服GLP-1RA药物容易在胃酸中被降解,诸如微球、微乳、脂质体、纳米粒等给药系统,能快速提高肠道上皮屏障通透性的吸收促进剂,以及细胞穿透肽、水凝胶等多种方法不断被开发,但大多数距离临床试验阶段仍有较大差距。目前,仅诺和诺德突破瓶颈,成功研发全球唯一上市的口服GLP-1RA药物——司美格鲁肽,并连续多年创造了多肽药物的销售神话。
双靶点或多靶点的GLP-1RA药物在疗效上表现出独特优势,成为行业竞相角逐的热门领域。当前,全球有超30家企业密集进军多靶点药物研发(临床试验),大部分集中在GLP-1/GIP(Glucose-dependent insulinotropic polypeptide,葡萄糖依赖性促胰岛素)、GLP-1/GCG(Preproglucagon,前胰高糖素原)、GLP-1/GIP/GCG、GLP-1/GCG/OXM(Oxyntomodulin,胃泌酸调节素)等,具体如表4所示。
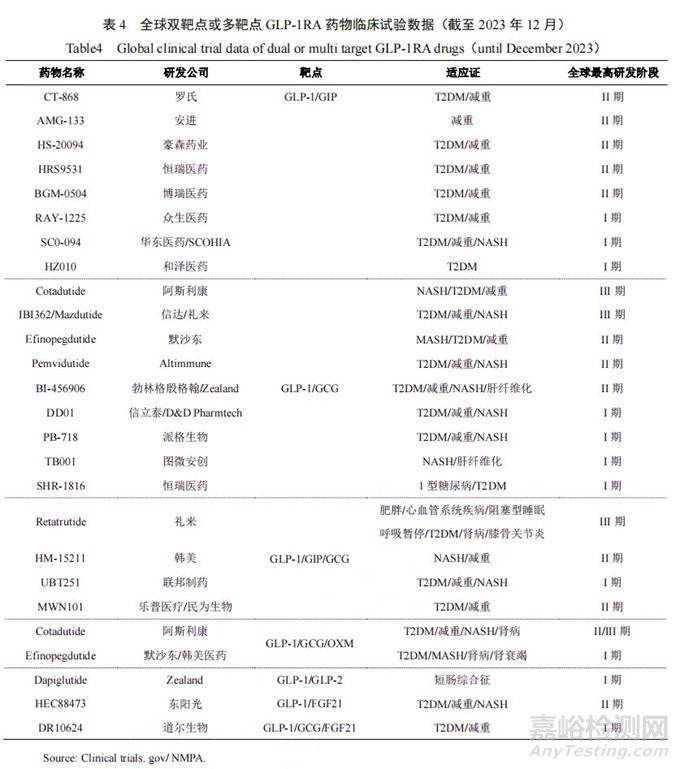
国内多个企业也有所行动,双靶点方面,信达在GLP-1/GCG领域的II期临床减重数据优秀,安全性良好,属于第一梯队,已经进入III期临床;华东医药和东阳光分别在GLP-1/GIP、GLP-1/FGF21(Fibroblast growth factor21,成纤维细胞生长因子21)领域进行研究,处于I期、II期临床;多靶点方面,联邦制药布局GLP-1/GCG/GIP,进入I期临床。双靶点或多靶点药物的结构往往更为复杂,分子量更大,传统类药性规则、经验参数等可能并不适合于判断其安全性。因此,研究者需要在大量的基础及临床实验中寻找规律,建立有针对性的指导原则,这无疑为新药开发增加一定难度。
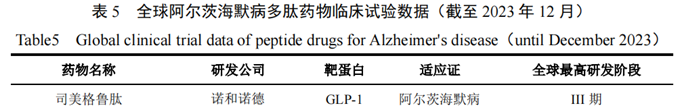
近年来,科研人员发现GLP-1RA药物在阿尔茨海默病的治疗中显示出潜在疗效。2021年,诺和诺德启动了两项III期临床试验EVOKE、EVOKE Plus,围绕3700名早期阿尔茨海默病患者开展司美格鲁肽的临床疗效研究,预计将于2025年9月完成EVOKE试验。此外,国内石药集团/天境生物正联合推进用于阿尔茨海默病治疗的生物类GLP-1受体激动剂TG103的I期临床试验(表5),天士力、Genexine等企业正在提交临床试验申请。作为备受关注的研究领域,基于GLP-1RA开发减缓阿尔茨海默病发展的多肽药物如若开发成功,有望为全球患者带来健康福音。

2.2.2多肽药物偶联物
多肽药物偶联物(Peptide-drug conjugate,PDC)作为一种新兴的前药物策略,不仅保留了多肽的功能和生物活性,还利用连接子的可裂解性响应性释放药物。PDC可显著提高药物在体内的循环稳定性和靶向性,降低药物的毒副作用,有望成为继小分子靶向药、单克隆抗体、抗体偶联药物之后的下一代靶向抗肿瘤药物。
据智慧芽统计,截至2024年3月,全球共有28款PDC药物处于临床研究阶段。目前PDC临床研究仍以国外公司为主,研发较快的有诺华、Bicycle Therapeutics、PeptiDream等企业。其中,Bicycle Therapeutics利用其新型环肽药物技术平台设计了三款PDC在研产品,均处于临床I/II期阶段。目前国内PDC布局者包括盛诺基、同宜医药、复星医药、藤栢医药、博瑞生物等(表6)。
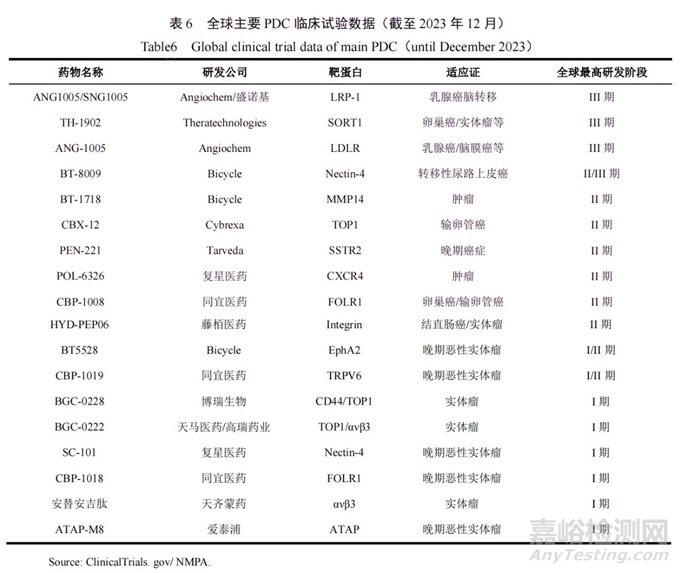
盛诺基与加拿大公司Angiochem合作开发的SNG1005可穿越血脑屏障和血脑脊液屏障,进入颅内发挥抗肿瘤作用,是全球范围尚未上市的全新化合物实体。2024年1月,作为国内第一个批准开展乳腺癌脑转移临床试验的PDC药物,SNG1005成功完成第III期临床桥接试验。如若获批上市,将为国内乳腺癌脑转移患者治疗提供新的选择。虽然PDC具有巨大的应用前景,但该领域的发展仍处于低迷状态。首先,考虑到安全性问题,多肽与药物偶联后是否能保留多肽的生物相容性和生物可降解性尚不清楚;其次是药物的有效性,PDC中的连接子需要特定的环境(温度、pH值、酶等)来断开并释放药物,有时药物无法达到原型药物的有效释放水平,甚至可能完全不释放。此外,目前还没有办法确定药物在靶细胞中的释放率和效率,因此,需要用适当的方法来证明PDC药物的疗效。
2.2.3 抗菌肽及罕见病多肽药物
据Cortellis数据库统计,截至2024年3月,全球临床在研抗菌肽约21款,52%仍处于临床I期(11款),处于临床III期及以上有4款(19%)。其中不乏中国本土企业,正大天晴/普莱医药合作开发的PL-5和益承生物开发的伊匹乌肽均进入临床III期阶段。其中,PL-5作为全新设计的首款非抗生素类抗菌药物,对局部开放性创面感染疗效良好,尤其对耐药菌株有很好的杀伤能力,又不产生新的耐药菌,市场潜力巨大。而伊匹乌肽治疗眼部炎症的研发进展较快,且目前没有同类药物上市,市场前景广阔。
罕见病治疗方面,Zealand开发的长效GLP-2类似物Glepaglutide已被授予治疗短肠综合征的孤儿药资格,并向美国药监局提交上市申请。韩美制药研发的HM15912也处于II期临床试验中,如表7所示。
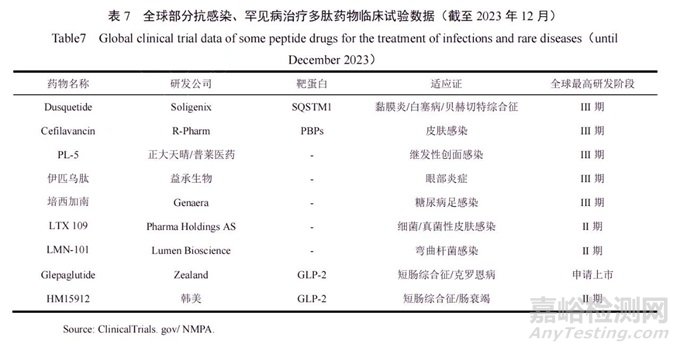
在市场经济中,由于缺乏经济利润和药品开发投资的回报,制药公司投资罕见病新药开发的意愿较低,许多罕见病存在“无药可医”的状态,临床治疗需求缺口巨大。
未来展望及建议
我国高度重视医药业发展,稳步推进多肽药物研发和生产。国家《“十四五”医药工业发展规划》明确将多肽、PDC等前沿核心技术产品列为重点发展对象。2023年3月,国家药监局药品审评中心发布的《化学合成多肽药物药学研究技术指导原则(试行)》,进一步规范了涉及化学合成多肽药物药学研究的原料药制备工艺、结构确证、制剂处方工艺、质量研究与控制、稳定性研究等方面技术要求,为多肽药物开发和产业化奠定了坚实的基础。我国多肽药物研发和生产起步较晚,整体尚处于发展阶段。截至2023年底,37款多肽新药已获国家药监局批准上市,但国产多肽新药数量仅5款。未来一段时期内,我国多肽药物产业仍将以仿制药为主,创新将主要集中于多肽仿制药的研发和生产工艺的改进优化。但差距同时孕育着提升空间,由于我国人口基数大且进口产品产能有限,需求端存在较大缺口,未来我国多肽药物市场发展空间广阔。此外,本土企业等效性研究开展与临床申报数量的双提升证明中国多肽药物产业正蓬勃发展。
为进一步推动我国多肽药物领域的持续健康发展,建议从以下三方面重点发力:技术研发方面,鼓励企业强化与高校、科研院所合作,开展多肽领域原创性研究,包括关键核心技术和前沿技术;鼓励有条件的地方政府设立多肽产业发展专项基金,用于支持多肽药物研发、关键生产技术升级、生产装备自主研发以及引进、消化和吸收国际先进技术等。市场主体方面,建议将多肽产业链纳入国家重点扶持产业,引导行业制定专项行动。对从事多肽药物研制的企业,包括与之配套的新品种、新技术、新装备、新工艺等创新性研究的企业,提供税收减免政策,鼓励自主创新。从合成设备、分离纯化设备、原材料、环保等各环节,对国产配套的企业予以资金支持,鼓励国产配套,对出口创汇型企业予以退税补贴,鼓励参与国际竞争;行业规范方面,制定多肽药物绿色生产指南,明确环保生产技术标准和要求。引导企业采用环保材料和工艺,特别是在减少溶剂使用、废水废气处理技术等方面的创新,给予大力支持,鼓励绿色环保。加大多肽药物知识产权保护力度,确保研发成果得到合法保护,为多肽行业健康发展保驾护航。
文章来源:《中国生物医药工程杂志》作者:窦树珍,周治寰,邹慧,刘少金

来源:Internet


