您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-11-20 08:44
亲脂性和微粒体蛋白孵育浓度是预估化合物与微粒体非特异性结合程度的决定因素。Austin和Hallifax、Houston等分别于2002年及2006年提出了两种预测方程用于评估孵育过程中化合物在微粒体中的游离分数(fraction unbound in the incubation, fuinc)。统计显示,针对不同亲脂性的化合物和微粒体蛋白浓度,仅使用这些预测工具来评估fuinc有一定的局限性,准确度较差,必要时应当通过实验来测定fuinc。那么应当如何选择合适的途径来准确获得fuinc呢?
我们的回答如下:
对于低亲脂性(logP/D<2.5)化合物,可以使用Austin或Hallifax&Houston的预测方程,能够得到准确度较高的fuinc。
对于高亲脂性(logP/D>5)化合物,两种预测方程均无法准确预测fuinc,必须通过实验来测定。
对于中等亲脂性(logP/D 2.5~5)化合物,两种预测方程得到的结果有显著差异,预测准确度一般,建议通过实验来测定fuinc。
如今,利用动物实验及体外实验的数据,人们已经建立了多种预测人体药代动力学和药效动力学的模型。其中化合物在微粒体孵育体系中的蛋白结合率是体外-体内外推(In Vitro-In Vivo Extrapolation,IVIVE)的一个重要参数。化合物与微粒体的非特异性结合可能会导致体内清除率被低估,或者在评价药物相互作用时出现IC50或Ki值被高估等后果。因此准确评估化合物与微粒体蛋白结合的程度十分重要,并且具有一定挑战性。
在药物研发早期,通常使用计算机模型预测的方法来进行一些成药性质的评价。用于评估fuinc的Austin预测方程[1]和Hallifax&Houston预测方程[2]都是基于微粒体蛋白浓度以及所研究化合物的亲脂性所提出的,那么它们的准确度怎么样呢?什么情况下有必要通过实验来确证化合物的fuinc?
表1. Austin预测方程和Hallifax&Houston预测方程

注:aC指微粒体蛋白浓度。
b在应用上述预测方程时,对于碱性及中性化合物使用分配系数logP来计算,酸性化合物使用分布系数logD来计算。
英国曼彻斯特大学曾汇总了127个不同亲脂性化合物的数据,以评估化合物亲脂性和微粒体蛋白浓度对于fuinc预测准确度的影响[3]。由于药物代谢和抑制类实验广泛应用0.1~1.0 mg/mL的微粒体蛋白浓度,因此选定了这一浓度范围。该统计汇总了平衡透析法测定的fuinc或文献报道值(微粒体蛋白浓度:0.1、0.5和1.0mg/mL),并与上述两种方程的预测值进行了统计及比较。
使用Austin和Hallifax&Houston预测方程在0.05~2mg/mL微粒体蛋白浓度范围内生成的模拟数据集(图1)显示,化合物的亲脂性对于预测fuinc的影响大于微粒体蛋白浓度的影响。
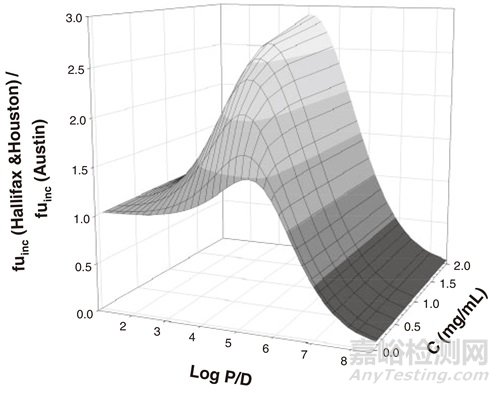
图1. 在亲脂性(logP/D 0~8)和微粒体蛋白浓度(C 0.05-2mg/mL)范围内,Hallifax&Houston和Austin方程fuinc预测值的比值[3]。
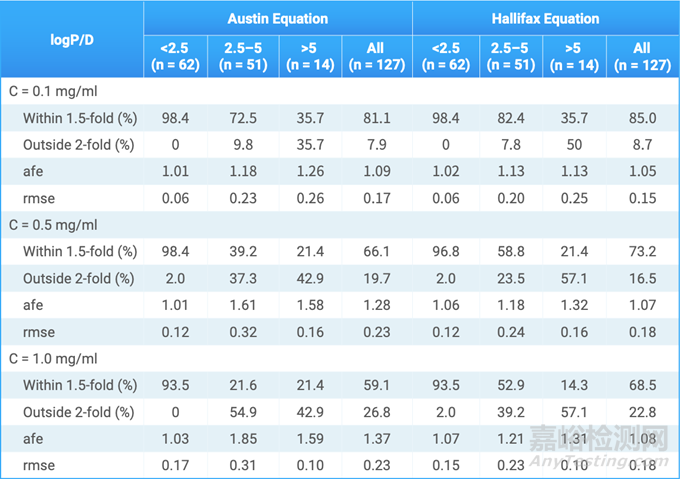
如下表2所示,在微粒体蛋白浓度较低(0.1mg/mL)时,所统计的127个化合物中,Austin预测方程和Hallifax&Houston预测方程的fuinc预测值与实验值差异在1.5倍以内的化合物均占比80%以上,仅有约8%的预测值与实验值差异超过2倍。说明在此微粒体蛋白浓度下,这两种方程均能够准确地预测fuinc。而随着微粒体蛋白浓度的增加,预测值的准确度有所下降。当微粒体蛋白浓度提高到0.5mg/mL时,预测值与实验值差异超过2倍的化合物占比增长至约16%。当微粒体浓度提高到1.0mg/mL时,这一比例增长至22%以上。
表2. 在不同微粒体浓度下,使用Austin方程和Hallifax&Houston方程预测不同亲脂性化合物的fuinc的准确度统计[3]
总体而言,相较于化合物的亲脂性,微粒体蛋白浓度对预测fuinc影响较小,但在较高的微粒体浓度下,该影响仍不可忽视。
对于低亲脂性(logP/D<2.5)化合物,可以使用Austin或Hallifax&Houston预测方程,能够得到准确度较高的fuinc。
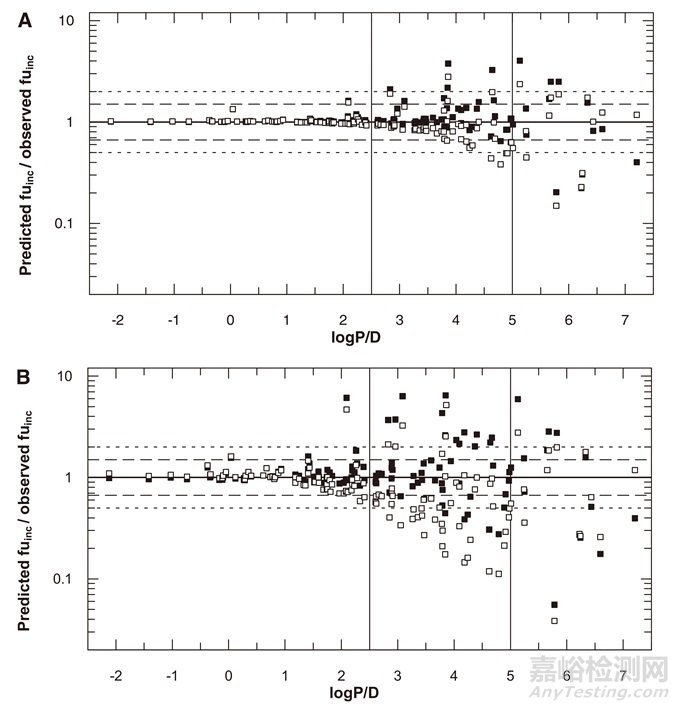
图2. 127个化合物的fuinc预测值/实验值比值(predicted/observed fuinc ratio)与亲脂性(logP/D)的统计[3]。
微粒体蛋白浓度分别为0.1mg/mL(A)和1.0mg/mL(B)。
□为Austin方程预测值。■为Hallifax&Houston方程预测值。
如图2所示,对于选定的62个亲脂性较低(logP/D<2.5)的化合物,在0.1mg/mL和1.0mg/mL微粒体蛋白浓度下Austin或Hallifax&Houston预测方程均能准确地预测fuinc。除两个化合物的预测值均高估50%以外,其余化合物的预测值与实验值差异均在2倍范围内。因此对于亲脂性低(logP/D<2.5)的化合物,尤其是在微粒体蛋白浓度较低时,在高通量筛选阶段,可以使用Austin或Hallifax&Houston两种预测方程,快速、准确地得到fuinc。
对于高亲脂性(logP/D>5)化合物,两种预测方程均无法准确预测fuinc,必须通过实验来测定。
对于选定的14个高亲脂性(logP/D>5)化合物,在0.1mg/mL和1.0mg/mL微粒体蛋白浓度下,两种方程均无法准确预测fuinc。在高微粒体蛋白浓度(1.0mg/mL),Austin和Hallifax&Houston方程将fuinc平均低估了159%和131%(表1,图2)。另外由于亲脂性logP/D>7化合物成药性较低,因此该范围内的化合物并未纳入这一统计中,但可以预期到针对该类化合物,预测方程的准确度较低。
对于中等亲脂性(logP/D 2.5~5)化合物,两种预测方程得到的结果有显著差异,预测准确度一般,建议通过实验来测定fuinc。
对于选定的logP/D在2.5~5范围内的51个化合物,两种方程预测的结果存在显著性差异,并且随着微粒体蛋白浓度的增加,预测的准确度变得非常低(图2)。在0.1和1.0mg/mL微粒体蛋白浓度下,Hallifax&Houston方程预测值与实验值差异在1.5倍内的占比分别为82.4%和52.9%,差异超过2倍的占比分别为7.8%和39.2%。而Austin方程预测值与实验值差异在1.5倍内的占比则分别为72.5%和21.6%,差异超过2倍的占比9.8%和54.9%。在0.1、0.5和1.0mg/mL微粒体蛋白浓度下,两种预测方程预测值与实验值差异超过2倍的平均占比约28.8%,预测准确度一般。
虽然文献中指出当微粒体蛋白浓度高于0.1mg/mL时,对于logP/D≥3的化合物通过实验测定fuinc[3],但我们仍建议,无论微粒体蛋白浓度高低,对于logP/D 2.5~5范围内的化合物也都采取实验手段,以便能够获得准确的结果。
结 语
为了避免化合物与微粒体蛋白的非特异性结合对成药性评价产生影响,通常选择低浓度的微粒体蛋白进行实验,特别是对于具有高酶活性的重组酶。然而,在某些条件下,例如研究Ⅱ相代谢反应或肠道代谢时,仍然需要使用较高浓度的微粒体。值得注意的是,即使是在较低的微粒体蛋白浓度下,高亲脂性化合物也可能显示出较高的微粒体蛋白结合率。因此使用预测方程具有一定的局限性,在药物研发后期,建议通过实验来准确测定fuinc。
综上所述,药物研发早期,使用计算机模型来预测化合物与微粒体的非特异性结合提高了筛选速度。然而针对不同亲脂性质的化合物或微粒体蛋白浓度条件,仅通过预测方法存在一定的局限性,实验手段是必不可少的,需要根据化合物性质及研究目的,选择合适的途径去评估fuinc,以保证结果的准确性和可靠性。
参考文献:
[1] Austin RP, Barton P, Cockroft SL, Wenlock MC, and Riley RJ. The influence of nonspecific microsomal binding on apparent intrinsic clearance, and its prediction from physicochemical properties. Drug Metab Dispos. 2002 30: 1497–1503.
[2] Hallifax D and Houston JB. Binding of drugs to hepatic microsomes: comment and assessment of current prediction methodology with recommendation for improvement. Drug Metab Dispos. 2006 34: 724–726.
[3] Gertz M, Kilford PJ, Houston JB, Galetin A. Drug lipophilicity and microsomal protein concentration as determinants in the prediction of the fraction unbound in microsomal incubations. Drug Metab Dispos. 2008 36(3):535-542.

来源:药明康德DMPK


