您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-01-22 20:08
本文依据 ISPE[1]基于风险的校准管理方法以及中国 GMP 的管理规定,结合生物制药生产过程中的实际计量现状,对计量的基本概念进行简述,并探讨执行计量的必要性及它在企业中的具体实施方法。
1、计量的基本概念
计量是确保单位统一和量值准确可靠的活动。在单位统一方面,计量要求使用标准的量具和仪器,以保障测量结果的准确性。在量值传递和溯源方面,通过检定和校准受检量具和仪器设备,企业能够确保测量结果的可靠性。
检定的定义是查明和确认测量仪器是否符合法定要求的一系列活动,包括检查、加标记或出具检定证书等步骤。而校准则是在规定条件下进行的一组操作,其首要步骤是确定测量标准所提供的量值与仪器相应示值之间的关联,随后利用这一信息来确定如何从示值推导出测量结果。其中,测量标准提供的量值与仪器的示值均存在一定的测量不确定度。
在整个计量过程中,需要使用标准器对计量器具进行检定或校准。标准器是企业内部用作对比或用于建立和维持其他计量器具准确度的标准物品。计量器具是指可以直接或间接测量被测对象量值的装置、仪器、仪表和量具。
计量器具具备准确度、精度、量程、接受标准以及不确定度等多种属性,这些属性是出具计量报告的基础和判断依据。其中,准确度是指在一定实验条件下,多次测量的平均值与真实值之间的接近程度,通常以误差来表示,用于衡量系统误差的大小。精度则是指被测量值之间的一致性以及他们与真实值的接近程度,是精密度与准确度的综合体现。量程是指仪器设备的满刻度指示或输出范围,而不考虑其使用范围或设定值。接受标准是指对于检定(校准)结果,可接受的数值限度或其他适当的测量标准。不确定度则表示由于测量误差的存在,对被测量值不能确切确定的程度,其值即为各项测量值与平均值之间的最大偏差。
特种设备,如锅炉、压力容器(含气瓶)、压力管道、电梯、起重机械、客运索道、大型游乐设施和场(厂)内专用机动车辆等,因涉及生命安全且危险性较大,按照国家规定[3]需进行定期强制检定。
在生物制药计量的生命周期内,还存在一定的特殊性。这主要包括测试和验证,旨在涵盖没有检定和校准规范的情况,通常也是对设备性能的一种测试或验证。测试是按照测试方案进行的数据比对或分析,通常没有特定的接受标准,而是根据工艺、检测或其他要求制定。验证[2]则是按照用户需求标准和验证方案进行的安装、运行和性能确认,针对物理、化学特性进行更为全面和深入的数据分析,并非仅限于单一部件的校准或检定。
2、为什么要执行计量
一家企业,尤其是药企,在生产过程中必须遵循良好的生产规范,确保数据的完整性,这主要是为了保障生产出的药品能够满足临床需求,并最终安全、有效地应用于人类健康领域。执行计量的主要目的包含但不限于:确保数据的准确性、符合法规与标准要求、提升产品质量、减少成本浪费、增强市场竞争力以及促进技术创新。
在生物制药领域,计量的适用范围广泛,涵盖了工艺设备、QC 检测[2]、公用系统、EHS 安全附件以及研发机构等多个方面。简单来说,只要对数据测量和计算有要求,就需要纳入计量管理的范畴。
3、如何执行计量
接下来将从生物制药企业计量的基本流程、方式、可实施性、不确定性和数据准确性等方面进行简要介绍。首先需要了解一下计量的基本流程[1],具体见图1。
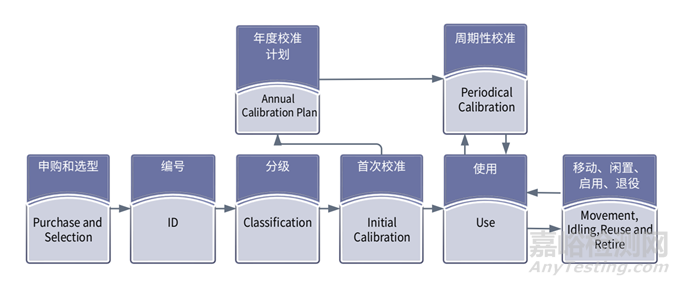
图1 计量的基本流程
通过图1 可以清晰地看到一件计量器具从采购到退役的完整流程。其次,在实际应用中,需要从 3 个维度来关注计量的方式:一是外部与内部,这主要区分了计量的实施方;二是在线与离线,这主要区分了计量的地点;三是多点与单点,这主要区分了计量的数据点。
外部计量通常由有资质的第三方或原厂进行校准。其中,有资质的第三方主要是指法定计量检定机构,而原厂校准则主要涉及专业性和保护性较强的精密仪器或设备,由制造商或授权的厂家进行。内部校准则是按照法定计量规程,选择适用的合格标准器,撰写内部校准规程,并填写校准记录及出具校准报告的一系列活动,这些校准活动仅适用于所在企业,不能用于其他商业用途。
在线计量是指需要计量的器具保持在设备或系统中,包括计量器具至变送器或 HMI 人机界面整个回路的计量;而离线计量则是将需要计量的器具从设备或系统中拆除,接入其他系统或标准实验室中进行计量。
多点与单点是计量过程中用于区分数据点的两种方式。多点计量通常涵盖全量程和覆盖使用范围两种类型,旨在满足不同的使用需求。全量程校准至少应包含 3 个校准点,分别是约5%、50% 和 100% 的量程点;若数据表中有特别说明或根据实际情况无法进行全量程校准,则应确保校准范围覆盖使用范围,并进行两点校准。单点计量则较为特殊,适用于那些固定安装且不可拆卸、或因技术原因无法满足使用范围校准要求的仪器仪表,此时应尽可能进行单点比对校准,或在最大可能范围内进行比对校准。
企业计量通常具有可实施性。当收到计量申请时,无论是复杂的设施设备、精密的仪器,还是相对简单的仪表,都需要从计量的需求出发进行评估,然后制定计量内容。评估主要从属性(包含精度、准确性、量程、使用范围、接受标准、计量频率、计量范围)、标准器(适用于内部校准)、方式(外部计量、内部校准、在线计量、离线计量、多点计量、单点计量)以及来源(中国计量法规如 JJG、TSG、GB/T 等 , 以及制造商专属计量规范如测试报告、验证报告)等多方面进行。
结合需求评估,可以判断计量应该如何实施。但也会遇到无法实施的情况,这时可以通过图2 的可实施性分析来判断并寻找解决方案。
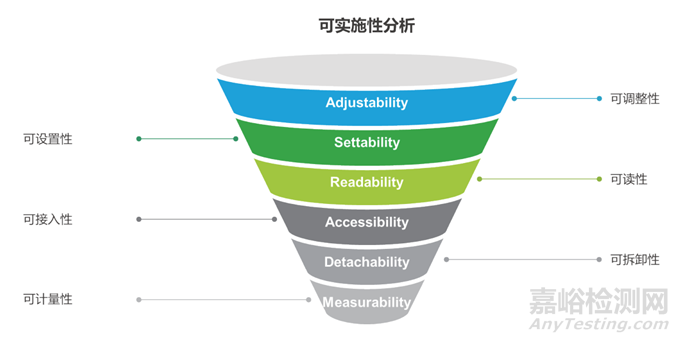
图2 计量可实施性分析
图2 展示了计量可实施性的分析要点,具体包括:
• 可计量性:关乎是否满足法规或原厂校准规范的要求;
• 可拆卸性:影响在线或离线计量方式的选择;
• 可接入性:决定与标准器的连接方式,或是否存在连接障碍;
• 可读性:能否根据计量属性,从被测计量器具中准确读取所需数据及单位;
• 可设置性:能否满足计量范围,并调整不同数据进行计量;
• 可调整性:当计量偏差过大时,是否可以进行调整或补偿。
若以上条件均得到满足,则符合公司计量及数据完整性的要求。反之,则需进一步讨论或咨询同行业做法。计量过程中,可能会受到多种不确定性的影响。接下来,结合前述方式,深入分析不同方式以及各种因素带来的不确定性。
在线与离线计量的不确定性主要体现在连接和读数上。在线计量时,不确定性主要源于现场计量标准器与被测器具的对接过程,这对接口匹配度和密封程度均有要求,因为转接部分可能会无形中增加计量的不确定性。而离线计量的不确定性则主要来自标准实验室的环境条件以及所采用的计量方法,且计量方法可能会随着标准实验室的变化而有所调整。离线计量完成后,还可能面临安装不到位导致原系统读数异常的问题,或者被测部件接入原系统后,经过系统的变送换算,换算后的数据与计量证书上的数据不一致的情况。
多点与单点计量的不确定性主要体现在数据覆盖使用范围上。多点计量包括全量程和覆盖使用范围,无论是哪种方式,都能有效地保证计量的线性度、准确性和稳定性。相比之下,单点计量由于无法覆盖整个使用范围,其带来的不确定性会面临多方面的挑战,如法规遵循和数据完整性等。虽有类似数据评估方法,如用同一台标准器连续监测几年,通过每年的数据统计和分析来确认单点计量的准确性和稳定性,但这种方式仅能证明该特定时间段内单点计量的可行性,无法预测未来几年可能发生的变化。
被测计量器具的材质及它所处的环境同样会带来一定的不确定性因素。对于材质相对稳定、且有护套保护并能进行定期维护的器具,能够持续稳定地工作,从而确保计量数据长期保持准确性和稳定性。若计量器具安装在洁净区内,图2 计量可实施性分析由于能维持良好的温湿度环境,因此受环境因素的影响相对较小。然而,安装在非洁净区内的计量器具,受到外界环境的干扰较大,这不仅会影响其使用寿命,还可能导致计量数据发生偏差。
计量人员的专业性和执行力同样会带来一定的不确定性,这些不确定性可能源于标准器的选型、计量方法的选择以及公式计算的准确性等因素。
最终,数据准确性是计量全生命周期中最为核心的关键要素。对于计量数据的记录,有着严格的规定:测量值不得进行舍入处理;测量结果的平均值、不确定度以及接受标准的小数点有效位数需保持一致;计量数据经过转换后,其有效位数也应与接受标准相吻合,如阻值换算为温度时的处理。在读数间隔方面,通常要求每隔 2 min 记录一次标准温湿度示值与被校准仪器的示值,连续记录 6 次。在进行压力校准时,升压与降压过程需保持平稳,避免冲击与过压现象,读数应在每个点位数值稳定后进行,并无固定间隔要求。
4、结 语
在日常工作中,为了确保计量的完整性和准确性,企业应当积极消除潜在的不确定性因素,采用科学、合理且精确的计量方法,从而为人类的健康事业提供有力保障,贡献绵薄之力。
参考文献
[1] Michael Berkey. ISPE 良好实践指南-设备-2020(中文版):2020,9-15, https://www.doc88.com/p-51573290102861.html
[2] USP1058 分析仪器确认,https://www.doc88.com/p-39997012563.html
[3] 鲁力.中华人民共和国特种设备安全法 [J]. 司法业务文选,2013 (25):20.DOI:10.3969/j.issn.1002-3631.2014.03.024.https://www.gov.cn/flfg/201306/30/content 2437160.htm
本文作者凌琪、王飞来、陈亚斌、李伟敏,无锡药明合联生物技术有限公司,仅供交流学习。

来源:制药工艺与装备


