您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-03-04 11:36
背景 Background
《药物遗传毒性研究技术指导原则》其中描述了遗传毒性试验方法有多种,根据试验检测的遗传终点,可将检测方法分为三大类,即基因突变、染色体畸变、DNA损伤;根据试验系统,又可分为体内试验和体外试验。
目前于没有任何单一试验方法能检测出所有的与肿瘤发生相关的遗传毒性机制,因此,通常采用体外和体内试验组合的方法,以全面评估受试物的遗传毒性风险。[1]
其中推荐的两种标准试验组合,均提及到了细菌回复突变试验,细菌回复突变试验又称Ames试验(Bacterial Reverse Mutation Test),是埃姆斯等人于1975年建立并不断发展完善的用于检测污染物致突变性的试验[2]。
一般利用突变型鼠伤寒沙门氏菌株(TAl535、TAl538、TA98、TAl00、TAl537或TA97或TA97a)或大肠杆菌色氨酸缺陷型菌株(WP2 uvra/uvra[pKM101]/pKM101)并加入哺乳动物肝微粒体进行体外试验,检查其再次发生突变的情况用于检测化合物的致变性和遗传毒性。
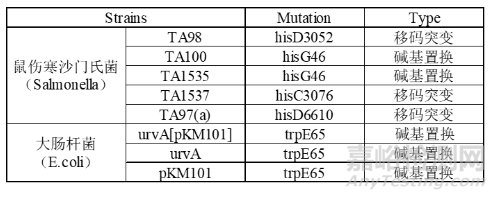
表1.Ames菌株类型表
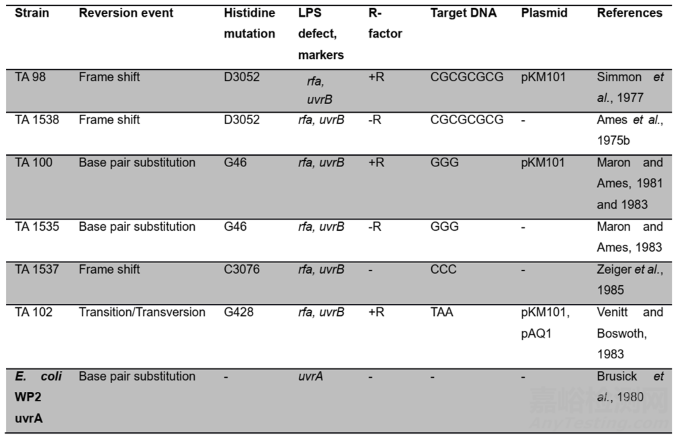
表2.沙门氏菌基因型的突变检测[2]
原理
该试验采用鼠伤寒沙门氏菌组氨酸营养缺陷型菌株或大肠杆菌色氨酸缺陷型菌株,这些突变的菌株自身不能合成组氨酸或色氨酸,必须依赖外源性组氨酸/色氨酸才能生长,而在无组氨酸/色氨酸的选择性培养基上不能存活。
假如有致突变物存在,致突变物可使菌株基因发生回复突变,由营养缺陷型转化为野生型,使它在缺乏组氨酸/色氨酸的培养基上也能生长,据此判断受试物是否为致突变物。原理如下图1所示:
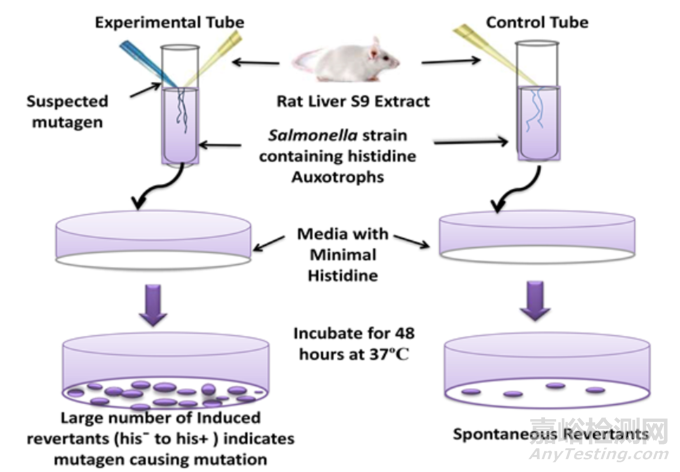
图1.沙门氏菌致突变性的遗传学评价方法[2]
试验一般设计:平板制备
培养基
0.5mmol/L组氨酸-0.5mmol/L生物素溶液(L-组氨酸78mg,D-生物素122mg,加蒸馏水至1000mL)配制:将上述成分加热,以溶解生物素,然后在0.068MPa下高压灭菌20min,4℃保存。
顶层琼脂培养基
取琼脂粉1.2g、氯化钠1.0g,加蒸馏水至200mL。配制:上述成分混合后,于0.103MPa下高压灭菌30min。实验时,加入0.5mmol/L组氨酸—0.5mmol/L生物素溶液20mL。
Vogel-Bonner(V-B)培养基E
一水合枸椽酸100g、磷酸氢二钾500g、四水合磷酸氢铵钠175g、七水合硫酸镁10g加蒸馏水至1000mL。配制:先将前三种成分加热溶解后,再将溶解的硫酸镁缓缓倒入容量瓶中,加蒸馏水至1000mL。于0.103MPa下高压灭菌30min。4℃保存。
20%葡萄糖溶液
葡萄糖200g加蒸馏水至1000mL。配制:加少量蒸馏水加温溶解葡萄糖,再加蒸馏水至1000mL。于0.068MPa下高压灭菌20min。4℃保存
底层琼脂培养基:
琼脂粉7.5g、蒸馏水480mL、V-B培养基E10mL、20%葡萄糖溶液10mL。配制:首先将前两种成分于0.103MPa下高压灭菌30min后,再加入后两种成分,充分混匀倒底层平板。按每皿25mL制备平板,冷凝固化后倒置于37℃培养箱中24h,备用总结就是把一个时间段的工作进行一次全面系统的总检查、总评价、总分析、总研究,并分析成绩的不足,从而得出引以为戒的经验。
营养肉汤培养基
牛肉膏2.5g、胰胨5.0g、磷酸氢二钾1.0g,加蒸馏水至500mL。配制:将上述成分混合后,于0.103MPa下高压灭菌30min。4℃保存。
盐溶液
氯化钾61.5g、六水合氯化镁40.7g,加蒸馏水至500mL配制:在水中溶解上述成分后,于0.103MPa下高压灭菌30min。4℃保存。
0.2mol/L磷酸盐缓冲液(pH7.4)
磷酸二氢钠(NaH2PO4·2H2O)2.965g、磷酸氢二钠(Na2HPO4·12H2O)29.015g,加蒸馏水至500mL。配制:溶解上述成分后,于0.103MPa下高压灭菌30min。储于4℃冰箱。
S9混合液
肝S9100mL、盐溶液20mL、灭菌蒸馏水380mL、0.2mol/L磷酸盐缓冲液500mL、辅酶II(NADP)4mmol、6-磷酸葡萄糖(G-6-P)5mmol。配制:将辅酶II和6-磷酸葡萄糖置于灭菌三角瓶内称重,然后按上述相反的次序加入各种成分,使肝S9加到已有缓冲液的溶液中。该混合液必须临用现配并保存于冰水浴中。
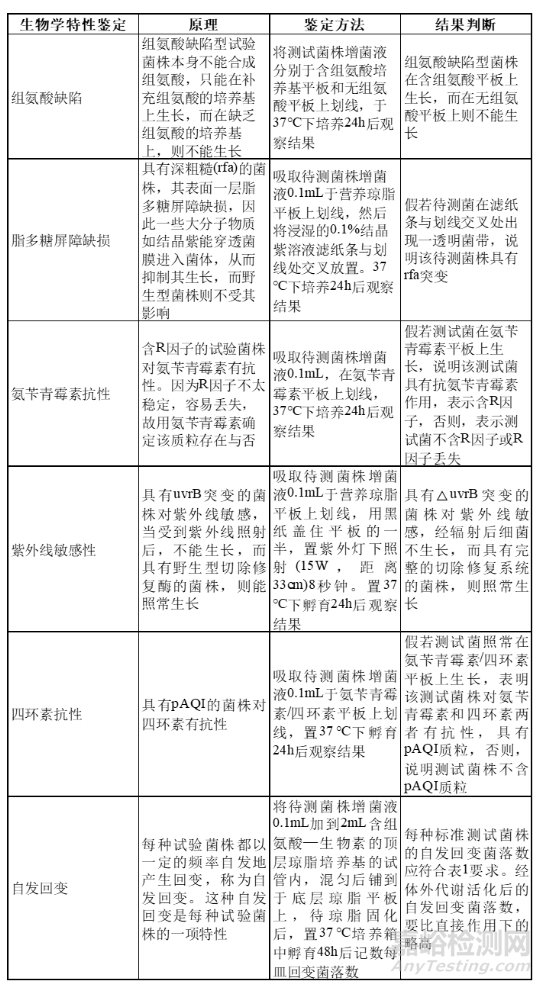
表3.生物学特性鉴定
目前市面上有多种试剂盒用于Ames试验,相比传统的试验,试剂盒在培养基成分准备、诱导S9制备、菌株鉴定、菌株培养等步骤能节约大量时间,试剂盒一般分平板掺入法和预培养平板掺入法,具体操作如下:
平板掺入法
a)准备所需底层培养基平皿若干。
b)融化顶层培养基分装于无菌小试管,每管2mL,在45℃水浴中保温。
c)在保温的顶层培养基中依次加入测试菌株菌液0.1mL,混匀;加受试物0.05mL~0.2mL(一般加入0.1mL。需活化时另外再加入10%S9反应混合液0.5mL),再混匀,然后迅速倾入底层培养基上。转动平皿,使顶层培养基均匀分布在底层上,平放固化,37℃培养48h观察结果。d)另做一阳性对照、溶剂对照和未处理对照。阳性对照不加受试物,只加标准诱变剂(即试剂盒阳性对照试剂,表4);溶剂对照加除受试物和标准诱变剂以外的所有试剂,如溶DMSO等(光谱纯或分析纯);未处理对照只在培养基上加菌液;其他方法同上。
预培养平板掺入法
预培养对于某些受试物可取得较好效果。因此可根据情况确定是否进行预培养。在加入顶层琼脂前,先进行以下预培养步骤:在试验中,将受试物(需活化时另加入10%S9反应混合液)和菌液,在37℃中培养20min,或在30℃中培养30min,然后再加2mL顶层琼脂,其他同上述平板掺入法。
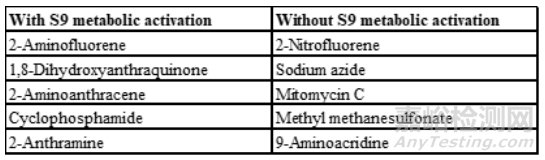
表4.有和没有 S9 代谢激活的阳性对照[2]
参考文献
[1] 《药物遗传毒性研究技术指导原则》,2018
[2] Urvashi Vijay.Microbial Mutagenicity Assay: Ames Test ,Bio-protocol [J]Vol 8, Iss 06, Mar 20, 2018

来源:Internet


