由于海上作业、娱乐和濒海战争等导致的伤口不可避免地暴露在高盐、高渗以及多种致病菌的海水中,从而容易引起严重出血、感染、组织坏死、愈合时间延长甚至高病死率等。然而,目前仅有少量关于海水浸泡伤口治疗的研究报道,且这些研究没有充分考虑海水浸泡伤口的特征以及特殊的海洋环境。构建具有稳定湿粘附的多功能水凝胶敷料有望实现在有渗出物、血液、海水等情况下粘附在伤口组织上,从而达到止血、隔离海水、预防感染、减少炎症、促进愈合等目的。然而,大多数报道的粘附水凝胶对于干燥界面显示出良好的粘附性,但难以实现对润湿界面的有效粘附。因为润湿界面的水化覆盖层阻碍了水凝胶和基底之间的相互作用。此外,水凝胶的溶胀性能降低了粘合界面粘附基团的密度,并降低了耗散基质的机械性能。受海洋生物湿粘附机制启发制备的仿生水凝胶可以通过儿茶酚基团与不同基底表面的相互作用实现湿粘附。然而,仅仅依靠儿茶酚基团仍然难以实现对湿润组织的稳定粘附。因此,制备在潮湿甚至水下环境中具有快速、稳定、持久粘附力的水凝胶敷料仍然是一个挑战。
近日,福州大学生物科学与工程学院石贤爱教授和杨建民副教授课题组,将儿茶酚改性的氧化透明质酸(OD)、ε-聚赖氨酸(EPL)和Fe3+通过希夫碱反应、金属螯合、阳离子-π和静电相互作用等制备了多功能水凝胶(OD/EPL@Fe)。通过结合仿贻贝策略、脱水效应和增强内聚力,使得所制备水凝胶具有高湿粘附强度(78 kPa),且粘附效果高于商业纤维蛋白胶和氰基丙烯酸酯胶。同时,该水凝胶可以有效清除海洋特定致病菌(创伤弧菌和铜绿假单胞菌)并抑制其生物膜的形成。此外,所制备水凝胶具有可注射性、自愈合、清除活性氧、光热效应、隔离海水、按需移除和止血等特性。体内实验结果表明,在大鼠颈部全层皮肤伤口模型中,该水凝胶对动态伤口有良好的粘附效果。特别是在大鼠海水浸泡感染的伤口模型中,该水凝胶表现出抗菌、抗炎和抗氧化的特性,并能够加速皮肤结构和功能的重建。
图1. (A) OD/EPL@Fe水凝胶制备示意图;(B) 潮湿环境下水凝胶的多种粘附机制;(C) 多交联结构赋予水凝胶优异的机械弹性和能量耗散;(D) 水凝胶促海水浸泡伤口愈合示意图。
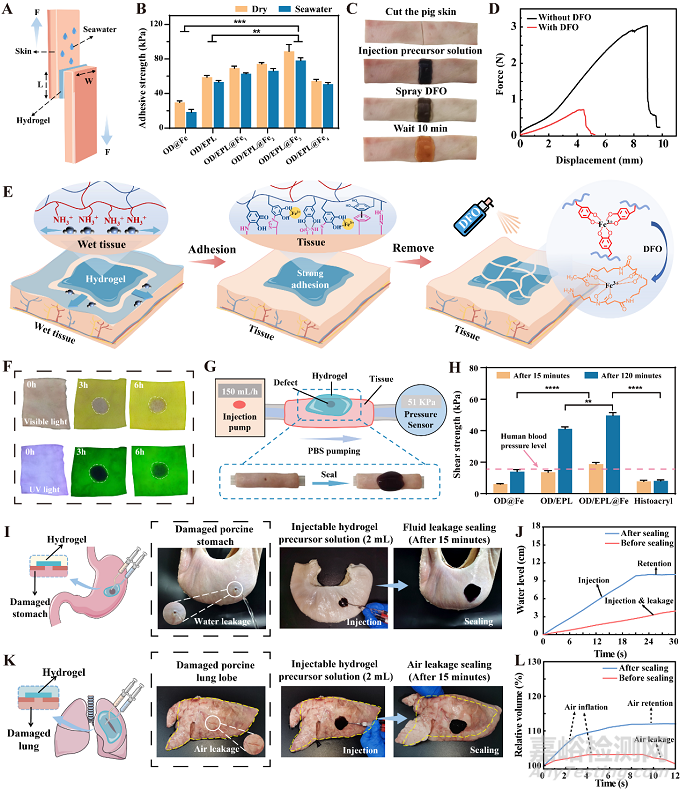
将猪皮浸泡在海水中,研究水凝胶在海水环境下的湿粘附效果。结果显示,OD/EPL@Fe3水凝胶在干燥和海水条件下粘附强度分别为89 kPa和78 kPa。值得注意的是,其湿粘附强度约为商用纤维蛋白胶的8倍,为氰基丙烯酸酯胶的1.5倍。去铁胺(DFO)作为一种医用螯合剂,通过快速解离儿茶酚-Fe金属螯合键来去除或更换水凝胶敷料。同时,水凝胶具有隔离海水的效果,防止处理伤口处再次受到海水浸泡。水凝胶的爆裂压力明显高于商用氰基丙烯酸酯胶和人体正常血压。此外,水凝胶还可以粘附在具有较低表面能的器官表面。结果表明,该水凝胶具有良好的湿粘附性能,且在止血和器官密封方面具有应用潜力。
图2. 水凝胶的湿粘附性能。(A) 搭接剪切试验示意图;(B) 水凝胶的搭接剪切强度;(C) 水凝胶按需移除过程;(D) 喷洒DFO前后,粘附力-位移曲线;(E) 水凝胶的湿粘附和按需去除机理示意图;(F) 隔离海水浸泡试验;(G) 爆裂压力装置示意图;(H) 水凝胶平均爆破压力;(I) 水凝胶对漏水的猪胃进行密封;(J) 密封过程中胃部水位的变化;(K) 水凝胶对漏气的猪肺进行密封;(L) 密封过程中肺部体积的变化。
海水中存在许多致病菌,如创伤弧菌和铜绿假单胞菌,可引起严重的伤口感染,从而影响伤口愈合甚至引发致命危险。试验结果表明,水凝胶对海水中致病菌具有优异杀菌效果。其中,OD/EPL@Fe+NIR组的细菌表面严重皱缩,并呈现出大量的孔洞,表明细胞膜被破坏。同时,抗菌试验结果表明该水凝胶具有光谱抗菌效果。此外,生物膜提高了细菌的耐药性,并加剧了伤口部位的感染。通过结晶紫染色和STYO 9荧光染色结果,证明了该水凝胶能够抑制生物膜形成。

图3. 水凝胶的抗菌和抑制生物膜形成效果。(A) 与水凝胶共培养后创伤弧菌和铜绿假单胞菌的菌落照片;(B) 细菌存活率;(C) 细菌形态学变化;(D) 水凝胶抗菌机理示意图;(E) 结晶紫染色后生物膜照片;(F) 结晶紫染色后生物膜的OD 570;(G) STYO 9染色后生物膜的共聚焦三维图像。
为评估OD/EPL@Fe水凝胶促海水浸泡伤口愈合的能力,从福州长乐东海岸(台湾海峡区域)采集了海水并添加创伤弧菌和铜绿假单胞菌构建了大鼠海水浸泡伤口模型。结果显示,多功能OD/EPL@Fe水凝胶同时发挥了抗菌、抗氧化、抗炎和促进血管生成的效果;加速了皮肤组织的再上皮化和胶原蛋白的沉积;并明显促进了海水浸泡感染伤口的愈合。其主要原因是水凝胶具有良好的抗菌效果,杀死了伤口处的细菌并抑制生物膜形成。同时,光热效应可以加速微循环血流,消除细菌,减少炎症。此外,所含的透明质酸具有诱导血管生成和促进成纤维细胞的增殖和迁移的能力,有利于促进氧气和营养物质向伤口部位的运输和产生更多胶原蛋白。

图4. 水凝胶对海水浸泡伤口的抗菌和促愈合效果。(A) 海水浸泡感染伤口模型和治疗示意图;(B) 伤口愈合照片;(C) 伤口处的细菌菌落照片;(D) 细菌菌落数计数;(E) 伤口面积变化;(F) H&E、Masson和Giemsa染色;(G) 胶原蛋白沉积情况;(H) 真皮层厚度。
虽然目前已经开发了各种新型功能敷料,但这些敷料主要用于处理在陆地环境中产生的伤口或者在具有良好医疗条件的场景中使用。然而,海洋环境中的伤口护理不仅需考虑敷料对伤口的湿性粘附,还要关注海洋特异性病原体的感染,并能防止处理伤口再次被海水浸泡。此外,快速止血、长期稳定粘附、减少氧化应激、抗物理应力破坏也是海水浸泡伤口愈合的迫切要求。该研究结果表明,所制备的OD/EPL@Fe水凝胶在海水浸泡伤口愈合方面具有应用潜力,且对于湿粘附和多网络水凝胶研究具有参考价值。该项成果以“Multi-crosslinked hydrogels with strong wet adhesion, self-healing, antibacterial property, reactive oxygen species scavenging activity, and on-demand removability for seawater-immersed wound healing”为题发表在Acta Biomaterialia期刊上。课题组硕士生吕奕成为本论文第一作者,通讯作者为杨建民副教授和石贤爱教授。本研究工作得到了国家自然科学基金(31800796)和福建省自然科学基金(2022J01095)的资助。