您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2021-04-21 08:41
为使人类免于使用医疗器械所产生的潜在生物学风险,国际标准、国家标准和指南都对各种医疗器械总体评价和开发过程的生物学评价提供了指导意见。而体外细胞毒性评价作为生物学评价中至关重要的一部分,常常为如何进行下一步的生物学评价提供重要的指导作用。国际标准化组织(ISO)、美国药典(USP)等均为细胞毒性检测建立了专门的评价方法(ISO 10993-5,ISO 7405,USP通则87)。本文与大家讨论一下如何进行产品的体外细胞毒性评价。
一、细胞毒性试验的目的?
细胞毒性试验的目的是为了评价产品或产品浸提液是否具有潜在的细胞毒性。
在进行产品的体外细胞毒性评价时,需要满足相应标准规定的进行体外细胞毒性评价的要求,以保证评价结果的充分性和有效性。
二、哪些产品需要进行体外细胞毒性评价?
在了解如何进行产品的体外细胞毒性评价前,我们需要先了解哪些产品需要进行体外细胞毒性评价。
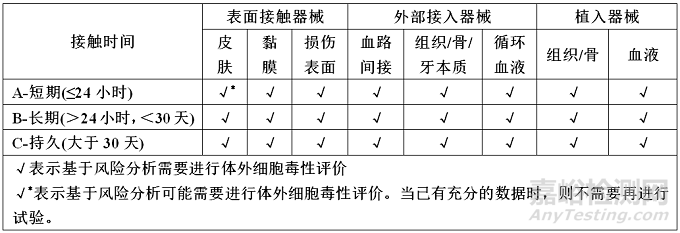
ISO 10993-1 按照器械的人体接触性质和接触时间给出生物学评价的框架,我们来具体地了解一下需要进行体外细胞毒性评价的器械有哪些。
三、如何选择试验方法?
既然几乎所有的产品都需要进行体外细胞毒性评价,而标准中提供的评价方法是多种多样的,我们应当如何从多种方法中选择适宜产品的试验方法呢?要了解如何选择试验方法,我们需要先了解试验方法有哪些。
a) 浸提液试验:浸提液试验是使用浸提介质浸提样品,然后通过浸提液与细胞接触来评价细胞毒性的方法,本试验用于细胞毒性定性和定量评定。
b) 直接接触试验:直接接触试验是通过样品直接与细胞接触来评价细胞毒性的方法。固体样品可直接置于细胞层与细胞接触,液体样品可直接放置;或放置到生物惰性吸水性的基质上与细胞接触。本试验用于细胞毒性定性和定量评定。
c) 间接接触试验:间接接触试验包括琼脂扩散试验和滤膜扩散试验。琼脂扩散试验是将样品置于琼脂层上,通过琼脂层与细胞间接接触来评价细胞毒性的方法,滤膜扩散是将样品置于无表面活性剂的滤膜,通过滤膜与细胞间接接触来评价细胞毒性的方法。间接接触试验用于细胞毒性的定性评定。
在了解了不同的试验方法后,接下来让我们继续了解一下不同的产品在选择评价方法时有哪些原则。
a) 可采用定性或定量的方法测定细胞毒性反应。但细胞毒性的定量评价更好一些,定性方法适合筛选用途。因此在进行成品医疗器械的生物学评价时,我们推荐使用定性的评价方法。
b) 在直接接触试验中,各种形状、尺寸或物理状态(如液体、凝胶、固体等)的材料未经修正即可进行测试,固体材料首选样品宜至少有一个平面,如无平面则应修整出平面,该平面需确保覆盖细胞层表面约十分之一。
c) 琼脂扩散试验不适用于不能通过琼脂层扩散或可能与琼脂相互作用的可沥滤物,使用琼脂扩散试验进行细胞毒性评定时,委托人需要有充分的理由来证明可沥滤物能通过琼脂层扩散,且与琼脂不会发生相互作用。
d) 对于口腔医疗器械的细胞毒性评价,ISO建立了专门的标准(ISO 7405),其中给出了琼脂扩散和滤膜扩散两种指导方法。
四、怎么样判定产品或产品的浸提液是否存在潜在的细胞毒性呢?
前边我们介绍了不同试验方法,不同的试验方法结果判定的准则也是不同的,下面我们就为大家逐一列举一下。
▷定量评价是测定细胞的死亡、生长抑制、细胞增殖或集落形成。可以用客观的方法对细胞数量、蛋白总量、酶的释放、活体染料的释放、还原等可测定的参数进行定量测试。细胞活性下降大于30%被认为是有细胞毒性反应的。以MTT法为例,当100%浸提液的存活率下降到小于空白的70%,则认为产品浸提液是具有潜在细胞毒性的。
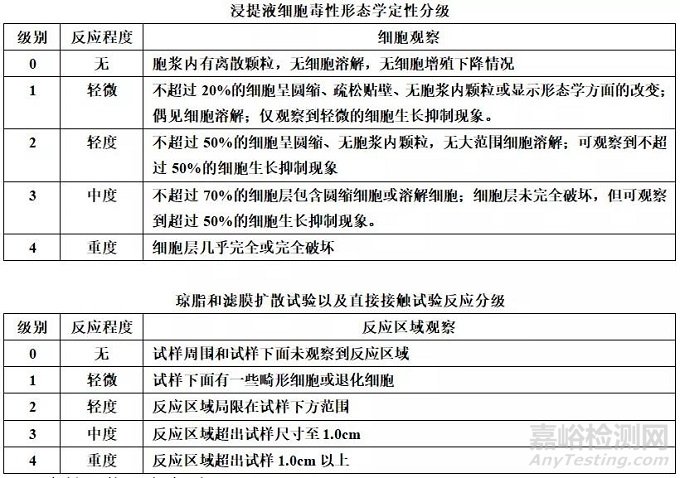
▷定性评价是使用显微镜检查细胞,评价细胞在一般形态、空泡形成、脱落、细胞溶解和胞膜完整性等方面的改变,并描述性地或以数字分级,来记录正常的形态变化。下面列举了两种细胞毒性分级的方法,当分级大于2级时被认为有细胞毒性作用。
五、细胞毒性评价注意事项
在进行体外细胞毒性评价的过程中有各种各样的注意事项,我们进行了总结分类,并分享给大家。
▷试验样品的注意事项:
a) 应考虑试验样品的无菌性,试验样品如取自非无菌供应但在使用前灭菌的器械,应规定适宜的灭菌方式对样品灭菌后进行试验,规定的灭菌方式宜考虑灭菌方法或灭菌剂对产品的影响。
b) 如取自不需要灭菌的器械,则应在供应状态下使用。为了避免细胞培养的微生物污染,对试验材料进行灭菌或许是合理的,但灭菌过程不应改变材料的性能。
c) 对吸水性试验样品,如果适宜,试验前应用培养基将其浸透,以防止其吸收试验器皿中的培养基。
▷测试过程的注意事项:
a) 当浸提介质采用水等非生理浸提介质时,浸提液用培养基稀释后应在最高生理相容性浓度下进行实验。推荐使用高浓度的(如2倍、5倍)培养基稀释非生理浸提液。
b) 使用浸提液试验和直接接触试验进行细胞毒性评价,浸提液与细胞接触的时间应不少于24小时。使用琼脂扩散试验进行细胞毒性评价,样品与细胞间接接触的时间应在24~72小时。
▷标准变更带来的浸提时间的改变
ISO 10993-12标准升版之后,长期(>24小时,<30天)和持久(>30天)接触的样品在进行细胞毒性评价时,推荐的浸提时间是72小时,因为浸提24小时可能不足以使那些使用超过24小时的器械上的化学物质充分释放。

来源:海河生物


