2022年,深圳发改委连续发布《深圳市促进生物医药产业集群高质量发展的若干措施》和《深圳市促进高端医疗器械产业集群高质量发展的若干措施》,重点促进生物医药产业的协同发展和重大技术的攻关,接下来,我们重点比较福田区、龙岗区、龙华区、坪山区、光明区五个区的生物医药产业发展情况。
一、产业指标
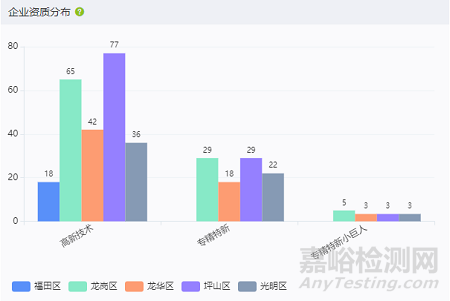
从企业资质分布看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的高新技术企业分别有18、65、42、77、36家,专精特新企业分别有0、29、18、29、22家,专精特新小巨人企业分别有0、5、3、3、3家。
图 深圳市生物医药产业资质分布情况
资料来源:药智数据区域产业分析系统
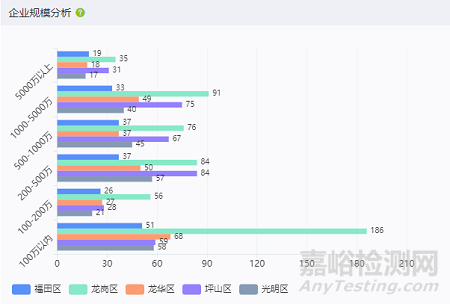
从企业规模看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的生物医药产业企业,注册资金在5000万以上的分别有19、35、18、31、17家,1000-5000万的分别有33、91、49、75、40家,500-1000万的分别有37、76、37、67、45家,200-500万的分别有37、84、50、84、57家,100-200万的分别有26、56、27、28、21家,100万以内的分别有51、186、68、59、58家。
图 深圳市生物医药企业规模分布情况
资料来源:药智数据区域产业分析系统
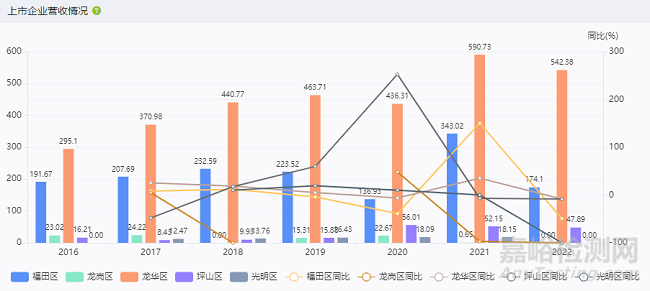
从上市企业的营收情况看,从2016年至2022年,福田区、龙岗区、龙华区、坪山区、光明区的生物医药上市企业累计营收分别为1509.53亿、85.87亿、3139.99亿、206.51亿、78.90亿。对2016年-2023年数据求和,在全国所有区县中,福田区排 29 名,龙岗区排 169 名,龙华区排 15 名,坪山区排 114 名,光明区排 172 名。
图 深圳市生物医药企业营收情况
资料来源:药智数据区域产业分析系统
从企业参保人数分析看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的生物医药产业企业,参保人数在100-499人的分别有1、3、0、2、1家,20-99人的分别有5、8、6、12、4家。20人以下的分别有197、517、243、330、233家。
图 深圳市生物医药企业参保人数分析
资料来源:药智数据区域产业分析系统
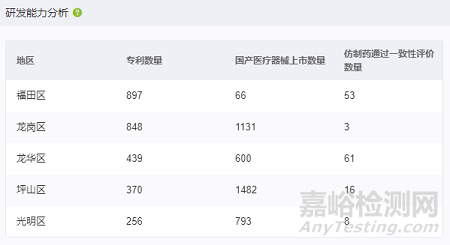
从研发能力看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区生物医药产业专利数量分别为897、848、439、370、256个,国产医疗器械上市数量分别为66、1131、600、1482、793个。仿制药一致性评价数量分别为53、3、61、16、8个。
图 深圳市生物医药产业研发情况
资料来源:药智数据区域产业分析系统
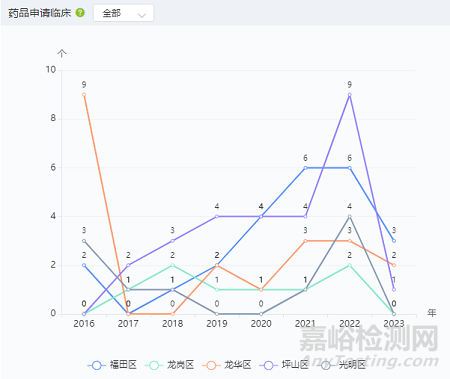
从药品申请临床看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的药品申请临床数量总数分别为24个、8个、20个、27个、10个。对2016年-2023年数据求和,在全国所有区县中,福田区排 48 名,龙岗区排 112 名,龙华区排 52 名,坪山区排 45 名,光明区排 96 名。
图 深圳市生物医药产业药品申请临床情况
资料来源:药智数据区域产业分析系统
从药品批准临床看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的药品批准临床总数分别为36个、8个、77个、34个、13个。对2016年-2023年数据求和,在全国所有区县中,福田区排 54 名,龙岗区排 176 名,龙华区排 28 名,坪山区排 57 名,光明区排 121 名。
图 深圳市生物医药产业药品批准临床情况
资料来源:药智数据区域产业分析系统
从仿制药通过一致性评价看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的仿制药通过一致性评价总数分别为53个、3个、104个、16个、8个。对2016年-2023年数据求和,在全国所有区县中,福田区排 29 名,龙岗区排 301 名,龙华区排 10 名,坪山区排 109 名,光明区排 174 名。
图 深圳市生物医药产业仿制药通过一致性评价情况
资料来源:药智数据区域产业分析系统
从医疗器械上市数量看,从2016年至2022年,福田区、龙岗区、龙华区、坪山区、光明区的医疗器械上市总数分别为66个、1131个、692个、1482个、793个。对2016年-2023年数据求和,在全国所有区县中,福田区排 226 名,龙岗区排 10 名,龙华区排 25 名,坪山区排 7 名,光明区排 20 名。
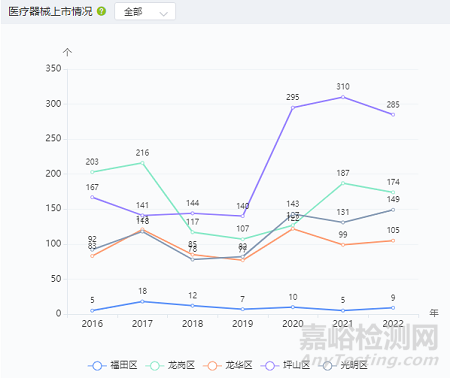
图 深圳市医疗器械上市数量情况
资料来源:药智数据区域产业分析系统
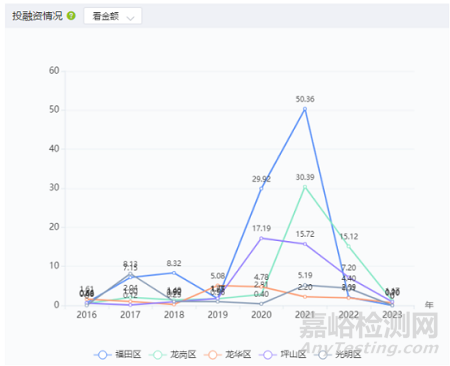
从投融资看,从2016年至2023年,福田区、龙岗区、龙华区、坪山区、光明区的累计投融资金额分别为100.24亿、55.08亿、17.52亿、44.41亿、20.09亿。对2016年-2023年数据求和,在全国所有区县中,福田区排 24 名,龙岗区排 41 名,龙华区排 102 名,坪山区排 51 名,光明区排 92 名。
图 深圳市生物医药产业投融资分布情况
资料来源:药智数据区域产业分析系统
从市场竞争力看,从2016年至2021年,福田区、龙岗区、龙华区、坪山区、光明区的医院销售市场金额分别为382.31亿、31.85亿、359.20亿、114.76亿、78.59亿。对2016年-2023年数据求和,在全国所有区县中,福田区排 29 名,龙岗区排 274 名,龙华区排 36 名,坪山区排 103 名,光明区排 148 名。
图 深圳市生物医药产业企业分布情况
资料来源:药智数据区域产业分析系统
二、产业发展现状
(一)深圳市生物医药产业发展展望
1、重点支持的生物医药领域:
重点支持化学创新药、包括细胞治疗药物、基因治疗药物、基因检测设备、生物安全防护、新型血液制剂和新型疫苗等在内的高端生物制品、全新结构蛋白及多肽药物、儿童用药、罕见病药物、个性化治疗技术、生物酶技术、全新剂型及高端制剂技术、现代中药、古代经典名方中药制剂、先进制药设备以及数字化医疗等领域。对技术含量高、应用前景好、示范带动作用强的产品和平台项目,以及在应急处置和抗击新冠肺炎疫情中发挥示范引领作用的企业,在资金扶持、用地用房、人才奖励、注册审批、政府服务等方面予以优先支持。
2、重点鼓励的生物医药产业发展方向:
1)建设国家级药物科技和产业创新平台。主动承担新药研发等国家重大发展战略任务,主动承担国家级重大核心技术攻关和科技转化任务。支持建设落地深圳的国家重点实验室、国家工程研究中心等国家级创新载体;支持建设落地深圳的国家企业技术中心,围绕新靶标、新位点、新机制、新分子实体,加强前沿领域高水平基础研究,争取若干国家重大科技基础设施和高级别生物安全实验室落地,争取生物医药领域国家产业创新中心、国家技术创新中心和国家制造业创新中心落地。
2)布局和提升市级药物产业服务平台。加快建设合同研发机构(CRO)、合同定制研发生产机构(CDMO)、药物非临床安全性评价机构(GLP)、药物发现平台、动物实验平台、检验计量检测平台、生物医药审评审批公共服务平台和小试中试平台、生物医药关键人才实训平台、生物医药产业孵化加速平台、项目管理服务平台、生物医药产业人才信息平台、制药工程技术服务平台、生物医药供应链平台、MAH综合服务平台等市级重大产业公共服务平台。
3)谋划市级药物基础研究和核心技术攻关。支持相关单位整合优势研究力量,建设若干具有重要影响力的创新研究机构。继续布局若干批市级科技和产业重大专项,对有望解决重大临床需求与市场需求,进行新靶标、新位点、新机制、新原理等生物医药前沿领域高水平基础研究的,给予最高不超过3000万元的全额资助;对新靶点化学药、抗体药物、基因药物、细胞产品、微生物治疗、细菌治疗、多肽药物、噬菌体药物及酶工程等“卡脖子”核心技术攻关和重大产业项目,按照项目总投资40%分阶段给予资助,最高不超过3亿元。
4)加大药物临床研究激励力度。对经认定的临床研究床位不纳入医疗机构床位数管理,不做病床效益、周转率、使用率考核。大力引进、培育临床研究人才,支持三级公立医院加快实施临床研究“大PI”计划。优化临床研究人才评价体系,药物临床试验项目按不同来源和级别视同相应级别的科研项目,纳入主要研究者和直接参加研究者的绩效工资、职称晋升、岗位聘用等管理。
5)探索成立专业药物临床研究联盟和生物医药产业联盟。探索成立专业药物临床研究联盟,为临床研究提供试验设计、伦理审查、GCP核查、药物警戒等全方位服务,并实现统一的医学伦理审查、业务资源分配、质控标准建设和数据交换使用;成立联合产业链上下游的生物医药产业联盟,推动生物医药产业集群高质量发展。
6)探索临床评价中推广真实世界数据应用加快产品上市。持续推进“港澳药械通”政策扩展实施,推动更多临床急需且已在港澳上市的药品在我市符合要求的医疗机构使用。探索“港澳药械通”药品临床评价中推广真实世界数据应用,加快新产品上市进程。
(二)深圳市高端医疗器械产业发展展望
1、重点支持的高端医疗器械领域:
重点支持高端医学影像、体外诊断、生命监测与生命支持、高端植介入、应急救治、肿瘤放疗、医学腔镜、基因检测、光学设备、DNA合成仪、智能康复辅具及健康管理等仪器设备,疾病筛查、精准用药分析所需的各类试剂和产品,支架瓣膜、心室辅助装置、人工晶体、骨科器件等高端植介入产品,可降解材料、组织器官诱导再生和修复材料、新型口腔材料、高值国产替代耗材等生物医用材料,手术机器人、智能软件及其它人工智能信息技术在医疗装备场景的应用等领域。
2、重点鼓励的高端医疗器械产业发展方向:
1)聚焦医疗器械原始创新与融合发展。依托国家高性能医疗器械创新中心等现有国家级重点平台,主动承担国家级基础研究、重大科技转化和产业化落地任务,围绕关键零部件与新型材料领域,加强前沿高水平基础研究和核心技术攻关,补齐我市高端医疗器械科技创新和产业融合环节。
2)推动国家、省市级医疗器械重点平台建设。主动承担高端医疗器械研制等国家重大发展战略任务,主动承担国家级重大核心技术攻关和科技转化任务。推动国家高性能医疗器械创新中心加快建设;支持建设落地深圳的国家重点实验室、国家工程研究中心等国家级创新载体。加快市级医疗器械重点平台建设,谋划布局合同研发机构(CRO)、合同定制研发生产机构(CDMO)、检验计量检测平台、医疗器械审评审批公共服务平台和小试中试平台等市级重大产业服务平台。
3)布局市级医疗器械重大科技产业专项。支持相关单位整合优势研究力量,建设若干具有重要影响力的创新研究机构。继续布局若干批市级科技和产业重大专项;对聚焦高端影像系统、手术机器人、新型体外诊断设备、高端植介入产品、高性能医用芯片、高通量基因测序仪等重大装备、关键零部件、关键原材料研制的“卡脖子”技术攻关和重大产业化项目,对国内率先实现量产的重大装备,或成功应用于医疗器械产品的关键零部件或原材料企业进行资助。
4)构建全链条产业服务体系。推动市药品检验研究院(市医疗器械检测中心)光明分院等重点项目建设,逐步打造集医疗器械注册检测、生物安评、产品改进、法规咨询、质量体系建立及跟踪验证于一体的全链条公共服务体系。
5)支持二、三类医疗器械研发与生产。对在本市完成研制且进行产业转化的重点支持领域内医疗器械产品给予资助。对首次获批二类医疗器械注册证并在本市生产的、首次获批三类医疗器械注册证并在本市生产的、通过国家、省级创新医疗器械特别审批程序首次获得二、三类医疗器械注册证书且在本市生产的,均予以资助。
6)注重医疗器械研发、申报环节特色服务能力提升。强化专利信息资源的开发和利用,提升企业研发高端医疗器械的能力和水平。充分发挥国家药品监督管理局医疗器械技术审评检查大湾区分中心作用,建立针对医疗器械注册申报关键环节的辅导沟通机制,为本地医疗器械企业提供医疗器械注册申报全流程的咨询服务。鼓励医疗器械企业积极委托经认定的市级CDMO服务平台或总部在深圳的CRO服务平台(与企业无投资关系)提供服务。