您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-06-01 08:38
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:16条资讯,阅读时长约:3分钟 」
今日头条
扬子江抗感染新药获批上市。扬子江药业1类新药「注射用磷酸左奥硝唑酯二钠」获国家药监局批准上市。磷酸左奥硝唑酯二钠属于硝基咪唑类抗生素,是奥硝唑左旋异构体磷酸酯衍生物的钠盐,为已上市左奥硝唑的前药。这是该公司首个创新药品种,针对的适应症有:用于治疗由多种敏感厌氧菌所引起的多种感染性疾病;手术前预防感染和手术后厌氧菌感染的治疗;阿米巴病。
国内药讯
1.加科思KRAS抑制剂国内获批临床。加科思KRAS G12C抑制剂1 类新药JAB-21822获国家药监局临床许可,拟用于治疗KRAS G12C突变的晚期实体瘤。在临床前研究中,JAB-21822显示出良好的口服生物利用度和系统药物暴露,以及良好的药代动力学特征和耐受性。JAB-21822目前已在美国获临床许可,加科思今年下半年将在中美同步展开针对非小细胞肺癌、结直肠癌和其他实体瘤的临床试验。据悉,加科思药业还计划进一步开发KRAS G12D和KRAS G12V两个全球尚无IND申请的靶点疗法。
2.泽璟「甲苯磺酸多纳非尼片」即将获批。泽璟制药1类新药甲苯磺酸多纳非尼片新药上市申请已处于“在审批”阶段,有望近期获批上市,用于治疗晚期(无法手术或转移性)肝细胞癌。甲苯磺酸多纳非尼片是一种口服多靶点、多激酶抑制剂类小分子抗肿瘤药物。在一项II/III期临床(试验代号ZGDH3)中,多纳非尼治疗组中位总生存期(mOS)显著优于索拉非尼对照组,达到统计学和临床意义的显著延长。
3.信迪利单抗治疗NSCLC即将获批。信达生物和礼来开发的PD-1抑制剂达伯舒®(信迪利单抗注射液)用于鳞状非小细胞肺癌(NSCLC)一线治疗的新适应症申请(sNDA)已处于“在审批”阶段,预计即将获批。据悉,这将会是该产品获批的第3项适应症。值得一提的是,信迪利单抗用于一线治疗非鳞状NSCLC的适应症已于今年2月获批,1 月还申报了二线治疗鳞状NSCLC适应症,目前在NSCLC领域布局全面。
4.罗氏奥妥珠单抗国内即将获批。罗氏第二代CD20单抗Obinutuzumab(奥妥珠单抗,商品名Gazyva®)的上市申请已进入行政审批阶段,预计即将在中国获批。Gazyva是罗氏利妥昔单抗的升级产品,已于2013年获FDA批准上市,目前已获批与苯丁酸氮芥联用一线治疗慢性淋巴细胞白血病(CLL);与化药联用治疗滤泡型淋巴瘤(FL)和晚期FL;并与Imbruvica 联用治疗CLL/小淋巴细胞淋巴瘤(SLL)。2020年该药销售额已达6.77亿美元。
5.江苏晨泰创新EGFR-TKI报IND。晨泰医药1类新药Zorifertinib片(ADZ3759)的临床试验申请获CDE受理。ADZ3759是新一代以表皮生长因子受体为作用靶点的小分子酪氨酸激酶抑制剂(EGFR-TKI),可以100%透过血脑屏障,达到药物在血液、脑组织和脑脊液的浓度一致,拟用于治疗EGFR基因突变阳性的非小细胞肺癌(NSCLC)伴中枢神经系统(CNS)转移患者。
国际药讯
1.胆管癌靶向新药获FDA批准上市。FDA加速批准BridgeBio公司与Helsinn集团联合开发的口服FGFR抑制剂Truseltiq(infigratinib)上市,用于治疗经治、携带FGFR2融合或重排的局部晚期或转移性胆管癌(CCA)患者。在一项Ⅱ期临床中,Truseltiq在这类患者中的客观缓解率(ORR)为23%(95%CI:16-32%),中位缓解持续时间(DoR)5.0个月(95%CI:3.7-9.3个月)。联拓生物拥有该新药在大中华区的开发和商业化权益。
2.FDA批准创新PET显像剂上市。Lantheus Holdings正电子发射断层扫描(PET)显像剂Pylarify(piflufolastat F18)获FDA批准上市,用于识别前列腺癌的疑似转移或复发。Pylarify是一款靶向前列腺特异性膜抗原(PSMA)的放射性氟化小分子显像剂。Pylarify PET结合了PET成像的准确性、靶向PSMA的精确性和F18放射性同位素的清晰度,相比传统成像检测,Pylarify PET成像技术能够让医生更早、更准确地在身体任何部位发现疑似转移性或复发性前列腺癌。
3.偏头痛靶向疗法获批扩展适应症。FDA批准Biohaven Pharmaceuticals小分子CGRP抑制剂Nurtec口服崩解片(rimegepant 75 mg)扩展适应症,用于发作性偏头痛(每月偏头痛发作次数小于15次)的预防性治疗。在一项Ⅲ期临床中,与安慰剂相比,Nurtec治疗组3个月后患者每月偏头痛天数减少了4.3天,患者偏头痛天数减少30%;而且Nurtec的耐受性普遍良好。Nurtec是唯一获批既可用于急性治疗偏头痛发作,又可作为预防性治疗的偏头痛药物。
4.司美格鲁肽在美提交标签扩展申请。诺和诺德重新向FDA提交一份标签扩展申请,在降糖药Ozempic(诺和泰®,semaglutide,司美格鲁肽)的现有上市许可中,引入2.0mg的新剂量。Ozempic是一款每周一次、皮下注射的GLP-1类似物,目前在美国已批准0.5mg和1.0mg剂量,用于作为饮食调整和运动的辅助手段,以改善2型糖尿病成人患者的血糖控制;以及用于存在心血管疾病(CVD)的2型糖尿病成人患者,降低发生主要不良心血管事件的风险。
5.益普生治疗FOP新药进入优先审查。FDA受理益普生RARγ激动剂palovarotene的新药申请(NDA)并授予了优先审查,适应症为用于治疗进行性骨化性纤维发育不良症(FOP,也被称为“石人综合征”)。FDA将在2021年11月30日前作出审查决定。如果获批,palovarotene将成为全球首个用于治疗“石人综合征”的药物。在欧洲,欧洲药品管理局(EMA)和瑞士医药管理局(Swissmedic)也已受理palovarotene的营销授权申请(MAA),并授予了优先审查。
6.新冠疫苗引发血栓原因或被查明。来自法兰克福大学的研究人员初步发现COVID-19重组载体疫苗(如阿斯利康的Vaxzevria和杨森COVID-19疫苗)报告的罕见凝血事件可能是由“疫苗诱导的Covid-19拟态”综合征(VIC19M综合征)引起的。科学家发现,人类细胞中S蛋白转录后发生的不良剪接事件可能导致蛋白质C端被截断(缩短),导致可溶性S蛋白被释放到血液中,与表达ACE2受体的组织相互作用。与这些组织,特别是血管内皮细胞的相互作用可能导致凝血的不良副作用,与在严重COVID-19患者中观察到的情况类似。
医药热点
1.吴浩获2021年世川卫生奖。在第74届世界卫生大会颁奖仪式上,北京市丰台区方庄社区卫生服务中心主任吴浩因在全科医学、初级卫生保健、社区防控等方面作出的贡献,荣获2021年世川卫生奖。中国基层卫生工作者代表吴浩表示,将2万美元奖金全额转赠给北京昊康公益基金会,以帮助建立中国西部边远地区乡村卫生事业发展种子基金,更好地推进中国基层卫生健康事业协同发展。
2.北京市拟每个村卫生室至少配1名村医。北京市卫健委日前发布关于加快补充乡村医生岗位人员的通知,要求今年年底前,在完成村卫生室标准化建设的同时,村卫生室乡村医生岗位人员也要补充到位,实现每个村卫生室至少有1名乡村医生岗位人员的目标。各区可结合实际,对偏远山村或条件艰苦等难以吸引人员的乡村医生岗位,可适当突破现有政府购买服务水平,确保人员补充到位。
3.越南发现变异毒株混合体。越南卫生部日前宣布,发现一种新型新冠变种病毒,它是此前在印度和英国发现的两种变种病毒的混合体,能在空气中快速传播。据悉,越南新一波疫情与传播力更强的变种病毒有关,病毒能快速自我复制,是造成多个地方在短时间内感染病例急升的原因。目前,这一新发现的毒株混合体尚未命名。
4.全球共88个新冠疫苗进入临床。中国疾控中心主任高福目前透露,全球共有7条新冠疫苗研发技术路线,共有272个候选疫苗,其中88个已进入临床试验。在全球新冠疫苗研发中,中国目前已有3款灭活疫苗、1款腺病毒载体疫苗获附条件上市,1款重组蛋白疫苗获批应急使用。这几款疫苗均表现出良好的免疫原性和安全性。
审评动向
1. CDE新药受理情况(05月31日)
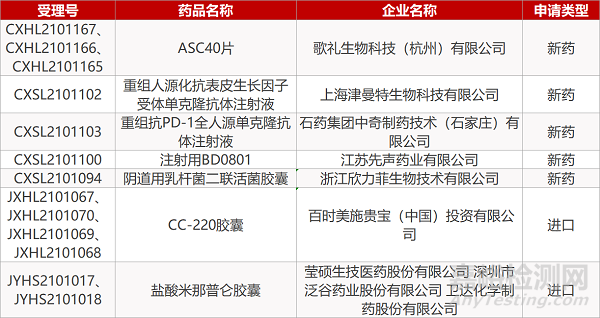
申请临床:
歌礼的ASC40片(3个规格)、上海津曼特的重组人源化抗表皮生长因子受体单克隆抗体注射液、石药集团中奇的重组抗PD-1全人源单克隆抗体注射液、江苏先声的注射用BD0801、浙江欣力菲的阴道用乳杆菌二联活菌胶囊、百时美施贵宝的CC-220胶囊(4个规格)。
申请生产:
莹硕生技/深圳市泛谷药业/卫达化学制药的盐酸米那普仑胶囊(2个规格)。
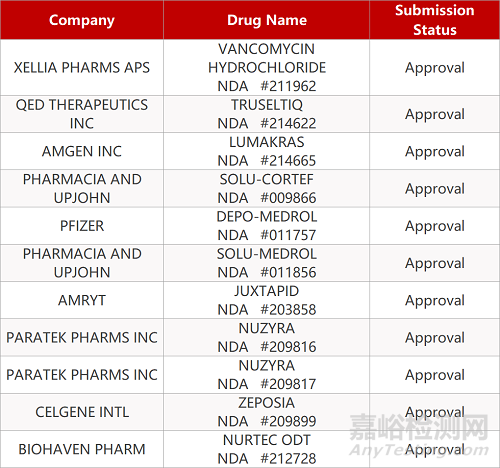
2. FDA新药获批情况(北美05月28日)

来源:药研发


