您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-17 11:22
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
先为达小分子GLP-1新药获批临床。杭州先为达GLP-1受体激动剂XW014获FDA临床许可。XW014是一款口服小分子GLP-1受体激动剂,拟开发适应症包括2型糖尿病、肥胖患者的体重管理、非酒精性脂肪性肝炎及其他代谢性疾病等。与大分子GLP-1受体激动剂相比,XW014口服给药,能提高患者的依从性,比口服多肽类药物更能提高生物利用度,受饮食、合并用药影响较小。
国内药讯
1.罗氏「恩曲替尼」在华获批用于NSCLC。罗氏旗下NTRK/ROS1酪氨酸激酶抑制剂抗癌药恩曲替尼(entrectinib)获国家药监局批准新适应症,用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)。今年7月29日,恩曲替尼胶囊刚刚获国家药监局首次批准上市,用于治疗NTRK融合阳性局部晚期或转移性实体瘤患者。在ROS1阳性NSCLC患者的一线治疗中,恩曲替尼总体客观缓解率(ORR)达68.7%。
2.绿叶戈舍瑞林微球报乳腺癌NDA。绿叶制药注射用醋酸戈舍瑞林缓释微球(LY01005)用于治疗乳腺癌的上市申请获CDE受理。LY01005是绿叶基于微球技术平台自主研发,通过创新微球技术,以肌肉注射的方式每月给药一次。在Ⅲ期临床中,LY01005(3.6mg)每28天肌肉注射一次治疗可有效控制血清雌二醇至绝经后水平,临床疗效与对照药物相比达到非劣效标准。此前,该新药用于治疗前列腺癌的上市申请正接受CDE的新药审评。
3.国药奥密克戎mRNA疫苗报IND。在15日举行的国药集团媒体通气会上,国药集团中国生物宣布,中国生物研发的奥密克戎灭活疫苗、第二代重组蛋白新冠疫苗均获得临床批件,奥密克戎mRNA疫苗也已提交临床申请。目前,中国生物已独立自主在灭活疫苗、基因重组疫苗、mRNA疫苗三条技术路线上研发4款新冠疫苗。其新冠疫苗总体年产能达到100亿剂,为全球最大新冠疫苗研发生产基地和最大供应商。
4.赛诺菲庞贝病新药在华拟优先审评。赛诺菲注射用艾夫糖苷酶α(avalglucosidase alfa)获CDE拟纳入优先审评,用于庞贝病(酸性α葡萄糖苷酶[GAA]缺乏症)患者的长期酶替代治疗。艾夫糖苷酶α可以靶向6-磷酸甘露糖(M6P)受体,从而改善GAA向肌肉细胞的递送。FDA 已于去年8月批准该产品上市,用于1岁及以上患者治疗晚发型庞贝氏症。avalglucosidase alfa治疗费用为33万美元/年(儿童)、75.8万美元/年(成人)。
5.默沙东NASH新药国内启动临床。默沙东GLP-1R/GCGR双重激动剂MK-6024注射液在国内登记启动一项I期临床(登记号:NCT04944992),在中国健康受试者中评价MK-6024的安全性、耐受性和药代动力学特征。该项试验主要研究者由复旦大学附属中山医院主任医师李雪宁担任。去年7月,默沙东在ClinicalTrials.gov上登记了一项该新药vs司美格鲁肽治疗非酒精性脂肪肝(NAFLD)的头对头IIa期临床试验(NCT04944992)。
6.华东医药完成Heidelberg Pharma收购。华东医药宣布已完成对Heidelberg Pharma股权投资方案所需的中德两国有关部门的批准或核准。今年2月,华东医药与Heidelberg Pharma签署《股权投资协议》及《产品独家许可协议》,以1.05亿欧元购进这家肿瘤ADC药物研发公司35%的股权,并获得其在研产品HDP-101、HDP-103在20个亚洲国家和地区的独家开发及商业化权益,在研产品HDP-102、HDP-104的独家选择权,以及另外2款后续在研产品的优先谈判权(ROFN)。
国际药讯
1.Moderna新冠mRNA二价疫苗获批上市。8月15日,英国药品监管机构(MHRA)批准Moderna生产的一款同时针对奥密克戎和新冠原始毒株的mRNA二价疫苗上市。临床数据显示,这款疫苗作为加强剂接种,能够针对奥密克戎BA.1变异株和新冠原始毒株产生强烈的免疫反应。根据Moderna今年6月发表递交的一项数据,这种二价疫苗可将针对奥密克戎的中和抗体水平提升8倍。
2.“渐冻症”干细胞疗法拟在美报BLA。BrainStorm Cell公司宣布基于研究的整体结果,该公司决定向FDA递交其间充质干细胞疗法NurOwn的生物制品许可申请(BLA),用于治疗肌萎缩侧索硬化(ALS)。在Ⅲ期临床中,NurOwn与安慰剂相比,达到临床缓解的患者比例(31%vs28%)不具有统计学意义的显著改善;但在症状较轻的患者亚群中,NurOwn显著改善患者评估ALS症状的ALSFRS-R评分(p=0.050)。此外,NurOwn显著增加患者的神经营养因子水平,减少神经退行性和神经炎症生物标志物。
3.吉利德TROP2-ADC治疗乳腺癌Ⅲ期临床成功。吉利德TROP2-ADC新药Trodelvy(sacituzumab govitecan)在治疗接受过多种前期治疗的HR+/HER2-转移性乳腺癌的Ⅲ期临床(TROPiCS-02)最新结果积极。该研究此前已达到无进展生存期(PFS)主要终点。此次中期分析显示,Trodelvy较化疗显著改善患者的总生存期;药物的安全性亦与之前研究一致。目前,吉利德已向FDA递交Trodelvy用于上述适应症的补充生物制品许可申请。
4.HER2-ADC乳腺癌临床再获新进展。阿斯利康与第一三共开发的HER2-ADC新药Enhertu(trastuzumab deruxtecan),在治疗HER2阳性、无法切除或转移性乳腺癌经治患者的Ⅲ期临床(DESTINY-Breast02)达到主要临床终点与关键次要终点。数据显示,Enhertu显著提高患者的无进展生存期和总存期。药物的安全性与已知研究一致。值得一提的是,FDA近期已加速批准Enhertu用于治疗HER2低表达的乳腺癌患者和携带HER2突变的非小细胞肺癌患者。
5.IGF-1R单抗甲状腺眼病早期临床积极。Viridian公司胰岛素样生长因子-1受体(IGF-1R)单抗药物VRDN-001治疗甲状腺眼病的I/II期临床数据积极。结果显示所有接受VRDN-001(10mg/kg)治疗的患者耐受性良好。截至2022年8月9日,未报告严重不良事件,未出现患者停药,也未发生高血糖或输液反应,2例发生不需要干预的轻度肌肉痉挛,1例发生耳鸣,并在未干预的情况下两周内得到改善。泽纳仕生物拥有VRDN-001(ZB001)的大中华区权益。
6.诺华IL-1β抑制剂NSCLC临床再次失败。诺华IL-1β抑制剂canakinumab (卡那奴单抗,ACZ885)辅助治疗II-IIIA和IIIB期完全切除的非小细胞肺癌(NSCLC)成年患者的III期CANOPY-A研究没有达到无病生存期(DFS)的主要终点。此前,卡那奴单抗联合多西他赛用于治疗既往接受PD1/PDL1抑制剂和铂类化疗的NSCLC患者的III期临床(CANOPY-2),以及卡那奴单抗联合帕博利珠单抗加铂类双药化疗一线治疗局部晚期或转移性NSCLC的III期研究(CANOPY-1)均未达到主要终点指标。
医药热点
1.《“十四五”卫生健康人才发展规划》出台。国家卫健委印发《“十四五”卫生健康人才发展规划》提出,力争到2025年,我国卫生健康人员总量达到1600万人,每千人口执业(助理)医师数达到3.20人(其中中医类别0.62人)、每千人口注册护士数达到3.80人、每千人口药师(士)数达到0.54人,每万人口全科医生数达到3.93人,专业公共卫生机构人员数增长到120万人,其中疾病预防控制机构人员数达到25万人。
2.北京绘出康复医疗路线图。北京市卫健委等8部门联合印发《北京市加快推进康复医疗工作实施方案》,要求到2025年,逐步建立一支数量合理、素质优良的康复医疗专业队伍,各区应至少设有1家二级及以上康复医院或1~2家康复转型医疗机构,每10万常住人口康复医师数达到8人、康复治疗师数达到12人,每千常住人口康复医疗服务床位数达到0.5张。
3.河南试点医防融合型慢病管理。河南省日前召开医防融合型慢病患者健康管理试点工作会议。河南省卫健委强调,试点地区要以签约服务团队为基本考核单元,评价内容包含基本医疗服务、基本公共卫生服务和慢病患者健康管理服务等;评价维度包含工作质量、工作数量和群众满意度;以绩效评价结果为依据,实行多劳多得、优绩优酬,同时评价结果与薪酬分配、评先评优、职称(职务)晋升等挂钩。
4.上海疾控:目前未接到猴痘病例报告。日前,网传“上海前滩出现猴痘疫情”。16日,在上海发布评论区,有网友留言询问:网传上海有猴痘确诊病例了,是真的吗?对此,上海发布回应称:经询市疾控部门,目前上海没有接到猴痘病例的报告,疾控部门持续关注国际疫情发展,并加强本地监测。
评审动态
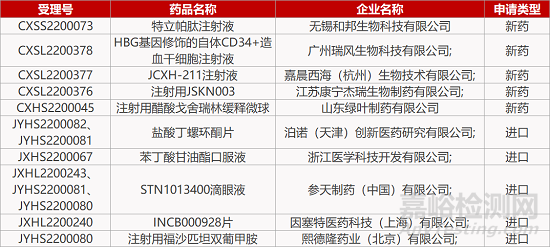
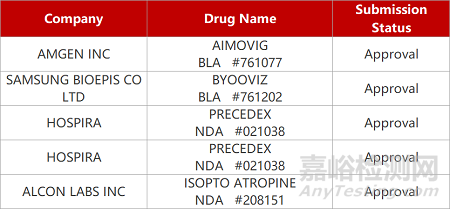

来源:药研发