FDA是食品药品监督管理局(Food and Drug Administration)的简称,是美国政府在健康与人类服务部 (DHHS) 下属的公共卫生部(PHS) 中设立的执行机构之一。根据医疗用途和对人体可能的伤害, FDA将医疗器械分为Ⅰ、Ⅱ、Ⅲ类,越高类别监督越多。
FDA医疗器械法规包括器械上市前和上市后两大部分,其中上市前部分的核心是“上市前批准(PMA)”和“上市前通告(PMN,也即510(k))”。
上市后部门的核心为“医疗器械质量体系法规(QSR820)”和“医疗器械报(MDR)”。510(k)为医疗器械在美国上市的主要途径之一,绝大多数的II 类医疗器械和部分I 类、III 类医疗器械通过此途径清关上市。
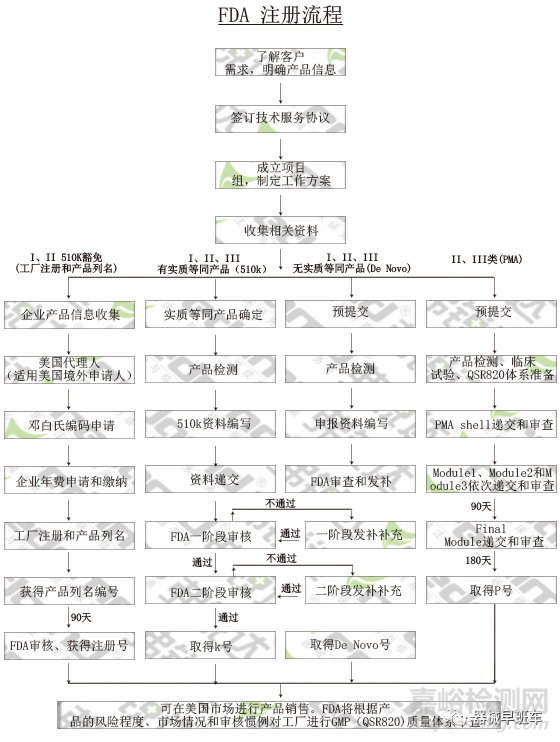
相关法规:
1、CFR-Code of Federal Regulations Title 21
2、21 CFR 812-Investigational Device Exemptions
3、21 CFR 814-PREMARKET APPROVAL OF MEDICAL DEVICES
4、21CFR 830-Unique device identification
5、21CFR 801-Subpart B-Labeling requirements for unique device identificatio





