您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2023-08-29 10:22
口咽/鼻咽通气道在《医疗器械分类目录》中分类编码为08-06-06的口咽/鼻咽通气道,该产品的管理类别为Ⅱ类。
一、口咽/鼻咽通气道的结构组成和工作原理
维持上呼吸道通畅:对于麻醉病人或昏迷病人,支持舌维持上呼吸道通畅的口底和咽部肌肉松弛,舌向后坠入咽后壁,从而导致上呼吸道梗阻。当经口腔或单侧鼻腔插入口咽/鼻咽通气道后,其前端支撑咽后壁,可快速解除或缓解患者上呼吸道通气不畅或梗阻,达到上呼吸道通气目的。
产品为带有凸缘端的通气道,通常由高分子材料聚氯乙烯(PVC)、丙烯腈-丁二烯-苯乙烯共聚物(ABS)、硅橡胶等材质制成。应明确产品的结构及组成,包括附件,并提供相应的结构图示。在图示中标识各部件的名称、重要尺寸信息及测量位置。常见产品如图1、图2。


图1 口咽通气道 图2 鼻咽通气道
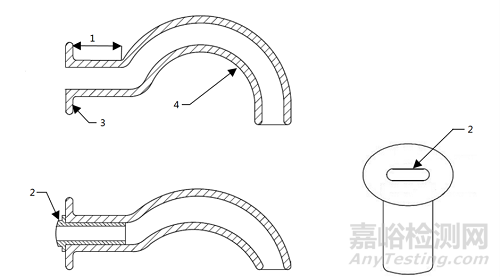
1-口颊部分;2-加强插入物,若提供;3-法兰盘端;4-通气道
图3 口咽通气道结构示意图

1-翼缘;2-接头;3-加强筋,若提供;4-通气道
图4 鼻咽通气道结构示意图
二、口咽/鼻咽通气道的主要风险
可参照GB/T 42062《医疗器械风险管理对医疗器械的应用》,充分识别产品的设计、原材料、制造过程、产品包装、灭菌、运输、贮存、使用等产品生命周期内各个环节的安全特征,从生物学危险(源)、环境危险(源)、有关插入过程的危险(源)、由功能失效等所引起的危险等方面,对产品进行全面的风险分析。
风险管理需包括生产和生产后信息,具体内容参考GB/T 42062第9章和《医疗器械安全和性能的基本原则》的2.1.2e)f)。
三、口咽/鼻咽通气道性能研究实验要求
口咽通气道产品宜符合YY/T 0977《麻醉和呼吸设备口咽通气道》等相关标准,鼻咽通气道产品可参考YY/T 0977《麻醉和呼吸设备口咽通气道》,结合产品设计特征及临床应用来制订,同时还需符合《医疗器械产品技术要求编写指导原则》的要求。
口咽通气道产品性能指标至少应包含外观、设计、尺寸(长度、内径)、规格标识、颜色编码(如适用)、抗扁瘪、内腔畅通性、微生物限度(如适用)、无菌、耐腐蚀性(如适用)、化学性能(重金属、酸碱度等)、环氧乙烷残留量(如适用)等。
鼻咽通气道产品性能指标至少应包含外观、设计、尺寸(长度、内径)、规格标识、接头要求(如适用)、病人端斜面角(如适用)、颜色编码(如适用)、内腔畅通性、抗扁瘪(如预期连接负压设备)、X射线不透性(如适用)、耐腐蚀性(如适用)、微生物限度(如适用)、无菌、化学性能(重金属、酸碱度等)、环氧乙烷残留量(如适用)等。
1.产品性能研究
产品性能指标可参考YY/T 0977《麻醉和呼吸设备口咽通气道》、YY/T 1040.1《麻醉和呼吸设备圆锥接头第1部分:锥头与锥套》标准制定,性能研究项目包括但不限于YY/T 0977《麻醉和呼吸设备口咽通气道》标准所列项目。
2.生物学特性研究
终产品中预期与人体直接或间接接触的部分,均需要进行生物相容性评价。
按照GB/T 16886《医疗器械生物学评价》系列标准、《医疗器械生物学评价和审查指南》要求开展生物相容性评价,应当包括:
(1)明确产品所用材料及与人体接触性质,设计和生产过程中可能引入的污染物和残留物,设计和生产过程中可能产生的析出物(包括可沥滤物和/或蒸发物)、加工残留物,与医疗器械直接接触的包装材料等相关信息。
(2)明确产品的物理和/或化学信息并考虑材料表征(如适用),如器械的物理作用可能产生生物学风险,应当进行评价。
(3)明确生物学评价的策略、依据和方法。
(4)已有数据和结果的评价。
(5)明确选择或豁免生物学试验的理由和论证。
(6)完成生物学评价所需的其他数据。
口咽/鼻咽通气道属于与黏膜短期接触的表面接触器械,若开展生物学评价试验,至少应进行细胞毒性试验、致敏反应试验、刺激试验。
3.灭菌工艺研究
参照GB 18279.1《保健产品灭菌环氧乙烷第1 部分:医疗器械灭菌过程的开发、确认和常规控制的要求》、GB 18280《医疗保健产品灭菌辐射》系列和GB/T 16886.7《医疗器械生物学评价第7部分环氧乙烷灭菌残留量》等标准的要求,明确产品包装及灭菌方法选择的依据,经过确认并进行常规控制,并应开展以下方面的确认:
(1)产品与灭菌过程的适应性:应考察灭菌方式、灭菌工艺过程对于口咽/鼻咽通气道产品的影响。
(2)包装与灭菌过程的适应性。
(3)应明确灭菌工艺(方法和参数)和无菌保证水平(SAL),并开展灭菌确认研究。无菌保证水平(SAL)应达到1×10-6。
(4)残留毒性:若灭菌使用的方法容易出现残留,如环氧乙烷灭菌,应当开展环氧乙烷解析的研究明确残留物信息及采取的处理方法。
4.产品货架有效期和包装研究
(1)货架有效期
货架有效期包括产品有效期和包装有效期。产品有效期验证可采用实时老化或加速老化的研究。加速老化研究试验的具体要求可参考YY/T 0681系列标准。有效期验证方案中应设定验证项目、验证方法及判定标准。验证项目包括产品自身性能验证和包装系统性能验证两方面。
(2)包装及包装完整性
在宣称的有效期内以及运输(例如:震动、振动、温度和湿度的波动)储存条件下,明确保持包装完整性的依据。企业需开展产品包装验证和运输验证研究。
包装研究应包括封口试验以及包装材料对灭菌的适应性研究。可依据GB/T 19633、GB/T 4857系列标准对包装进行分析研究和评价。直接接触产品的包装材料的选择应至少考虑以下因素:包装材料的物理化学性能;包装材料与产品的适应性;包装材料与成型和密封过程的适应性;包装材料与灭菌或洁净控制过程的适应性;包装材料所能提供的物理、化学和微生物屏障保护;包装材料与使用者使用时的要求无菌开启的适应性;包装材料与标签系统的适应性。
需开展运输稳定性验证,可依据有关适用的国内、国际标准和验证方案进行,如:产品包装的跌落试验、振荡试验等,开展运输稳定性验证研究,证明在规定的运输条件下,运输过程中环境条件不会对医疗器械的特性和性能造成不利影响。
5.其他
口咽/鼻咽通气道已列入《免于临床评价医疗器械目录》(以下简称目录),开发人需将产品相关信息与《目录》所述内容进行对比以及将产品与已获准境内注册的《目录》中医疗器械进行对比。具体可按照《列入免于临床评价医疗器械目录产品对比说明技术指导原则》要求进行。

来源:嘉峪检测网


