今日头条
星联肽Nectin-4靶向PDC获批临床。天津星联肽生物1类化药注射用SC-101获国家药监局临床默示许可,拟开发用于治疗Nectin-4表达的晚期恶性实体瘤。SC-101是一款多肽偶联药物(PDC),由靶向Nectin-4蛋白的多肽和微管蛋白抑制剂经连接子偶联而成。此前,苏州天马PDC产品BGC0222已在国内获批新药研究,用于治疗结肠癌、胰腺癌、乳腺癌、小细胞肺癌、胃癌及脑胶质瘤等实体瘤。
国内药讯
1.MSD九价HPV疫苗中国获批二剂次接种。默沙东九价人乳头瘤病毒(HPV)疫苗(酿酒酵母)(商品名:佳达修9)获国家药监局批准,用于年龄在9-14岁的女孩选择在第0、6月分别接种1剂次疫苗完成免疫程序。9-14岁女孩接种HPV疫苗容易激发更好的免疫反应。此前,佳达修9已在国内获批用于9-45岁的三剂次接种程序,用于帮助她们远离HPV感染相关的宫颈癌和宫颈病变。
2.诺华IL-17A单抗中国获批新适应症。诺华IL-17A抑制剂司库奇尤单抗(可善挺®)获国家药监局批准新适应症,用于治疗活动性银屑病关节炎。可善挺可特异性中和多种来源的IL-17A,抑制其促炎作用。此前,该新药已在中国获批用于治疗“符合系统治疗或光疗指征、6岁及以上儿童和成人中重度斑块状银屑病患者”和“强直性脊柱炎成年患者”。
3.信达GLP-1R/GCGR激动剂减重Ⅲ期临床成功。信达生物GLP-1R/GCGR双重激动剂玛仕度肽 (IBI362) 用于中国超重或肥胖成人减重的的Ⅲ期临床(GLORY-1)达成主要和所有关键次要终点。玛仕度肽(4mg和6mg)治疗32周后受试者体重较基线显著下降,体重相对基线下降≥5%的受试者比例显著优于安慰剂组;玛仕度肽总体耐受性良好,未发现新的安全性信号。信达生物计划尽快向NMPA递交其上市申请。
4.艾力斯EGFR-TKI拟纳入突破性疗法。艾力斯医药第三代EGFR-TKI创新药甲磺酸伏美替尼片(艾弗沙)获CDE拟纳入突破性治疗品种,用于一线治疗具有表皮生长因子受体(EGFR)20外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)。此前,该新药已获批用于治疗EGFR T790M突变阳性的局部晚期或转移性NSCLC,以及用于一线治疗EGFR外显子19缺失或外显子21(L858R)置换突变的局部晚期或转移性NSCLC。
5.泽德曼改良型皮炎新药拟纳入优先审评。泽德曼医药改良型创新药TAP-1503乳膏获CDE以“符合儿童生理特征的儿童用药品新品种、剂型和规格”拟纳入优先审评,用于2岁及以上特应性皮炎(AD)患者的局部外用治疗。TAP-1503活性成分是一种全新作用机制的非激素类小分子。去年3月,泽德曼医药宣布完成由佰诺资本领投的亿元A轮融资,以加速AhR靶点多个相关自免炎症性疾病药物的开发。
6.旺山旺水抗新冠新药启动RSV临床。苏州旺山旺水生物氢溴酸氘瑞米德韦干混悬剂(VV116)治疗呼吸道合胞病毒(RSV)感染的II/III期研究启动受试者招募工作。该项研究评估VV116用于治疗婴幼儿RSV感染的安全性、有效性、药代动力学特性及抗病毒活性。VV116是一款新型口服核苷类抗病毒药物,其片剂已于去年1月获国家药监局附条件批准上市,用于治疗轻中度新冠病毒感染,商品名为民得维。
7.和誉CSF-1R抑制剂获孤儿药认定。和誉医药新一代CSF-1R抑制剂Pimicotinib(ABSK021)获欧洲药品管理局(EMA)授予的孤儿药资格,用于治疗不可手术的腱鞘巨细胞瘤(TGCT)。在Ⅰb期试验中,Pimicotinib(50mgQD)队列的ORR达到87.5%。此前,该新药已分别被FDA授予用于治疗TGCT的突破性疗法认定和快速通道资格,以及EMA授予的优先药物资格(PRIME)。
国际药讯
1.司美格鲁肽复方周制剂IIIa期临床积极。诺和诺德评估每周1次司美格鲁肽固定比例联合制剂IcoSema治疗2型糖尿病的IIIa期试验(COMBINE 3)达到主要终点。与每日注射1次甘精胰岛素U100和门冬胰岛素(每日餐时注射2-4次)相比,IcoSema降低HbA1c的效果达到非劣效标准(-1.47%vs-1.40%);患者的体重显著减轻(-3.6kgvs-3.2kg);而且IcoSema组低血糖的发生率更低。
2.FDA拒批安斯泰来CLDN18.2单抗上市。安斯泰来CLDN18.2单抗zolbetuximab用于一线治疗CLDN18.2阳性、HER2阴性的局部晚期不可切除或转移性胃或胃食管交界处 (G/GEJ) 腺癌的上市申请收到FDA的完整回复函。这是由于第三方生产工厂存在未解决缺陷,FDA并未要求额外的临床数据。在Ⅲ期临床GLOW中,与安慰剂联合CAPOX化疗相比,zolbetuximab与CAPOX联合治疗显著改善患者的无进展生存期(8.21个月vs6.80个月)和总生存期(中位OS:14.39个月vs12.16个月)。
3.GSK以14亿美元收购Aiolos公司。葛兰素史克宣布与Aiolos公司达成收购协议,并获得该公司临床期、TSLP单抗候选药物AIO-001(SHR-1905)。SHR-1905是恒瑞针对免疫疾病(如慢性阻塞性肺病和慢性自发性荨麻疹)开发的抗体药物,Aiolos公司于去年8月获得该产品除大中华区外的全球独家权益。根据收购协议,Aiolos将获得10亿美元的预付款和高达4亿美元的成功监管里程碑付款。
4.Arrivent公司申请纳斯达克IPO。Arrivent Biopharma公司宣布已递交纳斯达克IPO申请。Arrivent Biopharma成立于2021年,创始人为姚正彬博士。Arrivent Biopharma的核心产品为2021年从艾力斯引进的第三代EGFR-TKI伏美替尼,以及与Aarvik合作开发的ADC新药ARR-002。Arrivent目前正在开展评估伏美替尼用于治疗携带其他EGFR突变的非小细胞肺癌(NSCLC)的Ⅲ期临床,预计2025年获得顶线数据。
5.基因药物公司Vico融资推进ASO药物开发。Vico Therapeutics宣布完成6000万美元B轮融资,用于支持其反义寡核苷酸(ASO)候选产品VO659开展Ⅰ/Ⅱa期临床,评估VO659鞘内注射多次递增剂量在轻中度脊髓小脑共济失调3型(SCA3)、1型(SCA1)和早期亨廷顿病(HD)患者中的安全性和耐受性,以及初步有效性。此次融资还将进一步拓展该公司在其他遗传性神经疾病领域的产品管线。
医药热点
1.陆骊工任广州市第一人民医院院长。1月5日,广州市人民政府网站公布市政府任免工作人员,其中,任命陆骊工同志为广州市第一人民医院院长,试用期一年。根据公开信息,陆骊工,教授,主任医师,博士生导师,兼任中国医师协会介入医师分会副会长,中国医师协会智慧医疗专委会副主委,清华大学智慧医疗研究院副院长、暨南大学介入与智能医学工程研究院院长、广东省肿瘤介入诊治重点实验室主任、广东省放射介入医疗质控中心主任。
2.上海第九人民医院国际医疗部启用。1月10日,位于浦东新区高科西路上的上海交通大学医学院附属第九人民医院国际医疗部、特需诊疗部正式揭幕启用。九院整形、口腔、耳鼻咽喉头颈外科、眼科等四大特色学科全部引入,并对接商业医保、采取预约制,探索国际旅游医疗新模式。目前医院已与10多家商保合作单位签约,开展国际医疗服务,为优质医疗资源发展提供新空间。
3.港中大团队发现“渐冻症”新发病机制。香港中文大学8日公布,港中大研究团队与英国牛津大学最近一项合作研究项目,揭示了肌萎缩性脊髓侧索硬化症(“渐冻症”)的一种新发病机制。目前,研究团队正筛选新的候选药物并测试它们在细胞和果蝇模型中抑制神经细胞死亡的功效。随后,团队计划在鼠类和灵长类模型上测试有潜力的候选药物,以进一步评估其有效性。
评审动态
1. CDE新药受理情况(01月10日)
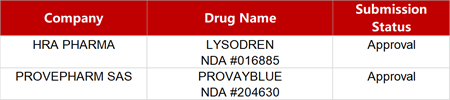
2. FDA新药获批情况(北美01月09日)