您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-07-04 09:19
摘 要: 建立高效液相色谱法测定化妆品中19种非甾体抗炎药含量。化妆品样品经体积比为1∶1的乙腈-乙酸铵溶液超声提取,用C18色谱柱(250 mm×4.6 mm,5 µm)分离,以不同体积比的乙腈-乙酸铵溶液为流动相梯度洗脱,采用二极管阵列检测器检测。布洛芬的检测波长为230 nm,醋氯芬酸、双氯芬酸钠检测波长为278 nm,其余16种非甾体的检测波长均为245 nm。19种非甾体的质量浓度在5~200 μg/mL范围内与其对应的色谱峰面积线性关系良好,相关系数均大于0.999 5,检出限为0.2~8 mg/kg。空白样品的水剂和凝胶基质的加标平均回收率分别为93.1%~110.9%和91.3%~108.1%,测定结果的相对标准偏差分别为0.2%~3.5%和0.6%~4.2%(n=6)。该方法适用于化妆品中19种非甾体抗炎药的测定。
关键词: 高效液相色谱法; 非甾体抗炎药; 化妆品
非甾体抗炎药物(NSAIDs)是目前临床应用最多、最广的处方药之一[1]。其药理作用机制主要是通过抑制环氧化酶,减少炎性介质前列腺素的合成,从而产生解热、镇痛、抗炎的作用。非甾体抗炎药物种类繁多,在临床应用过程中,出现了越来越多的不良反应,如肝损伤[2]、胃肠道[3]及皮肤损害[4]等。某不良反应监测中心对2008~2019年5597例有效自发报告患者NSAIDs相关不良反应(ADRs)数据进行统计,5597例ADRs报告中,累及多个系统/器官,共计6915例次,其中皮肤及皮肤附件损害1594例次(占23.05%),仅次于胃肠系统损害1799例次(占26.02%)[5]。另有统计评估显示,口服NSAIDs治疗比外用NSAIDs治疗的患者,胃肠道反应更常见,而外用NSAIDs组的皮肤反应发生率是口服NSAIDs组的5倍[6],且双氯芬酸通过颈后、颈椎透皮贴剂进行脊柱给药,药物可从贴片通过椎间隙扩散,穿透硬脑膜进入脑脊液,到达大脑[7]。上述研究揭示了NSAIDs有经皮肤吸收进而影响人体健康的风险。
近年来,在部分宣称祛痘、止痒、修护类化妆品的监督抽检中筛查出某些含有NSAIDs的化妆品。根据《已使用化妆品原料目录名称(2021年版)》[8]和《化妆品禁用原料目录》[9]规定:“对乙酰氨基酚在淋洗类产品中最高历史使用量为0.05%,但未提供驻留类产品最高历史使用量”“非那西丁、辛可芬、异丙安替比林和保泰松为禁用成分”,其他非甾体暂未作规定。化妆品中非甾体大致有以下来源:一是人为添加,非甾体抗炎药具有较好的抗炎、止痛和退红肿作用,特别是祛痘修护类化妆品中少量添加可缓解炎症及减少产品成分的刺激,从而达到较好的效果;二是原料带入污染。由于非甾体能引起诸多不良反应,为保证人民用妆安全和满足监管需求,有必要建立化妆品中非甾体的检测方法。
目前,关于NSAIDs的检测方法有液相色谱法、气相色谱法、液相色谱-串联质谱法等[10‒12],且大多应用在药品领域,化妆品中尚无相关标准和文献报道。笔者建立了高效液相色谱法测定水剂和凝胶类化妆品中19种非甾体抗炎药含量的检测方法,为化妆品中非甾体抗炎药的风险筛查和日常监管提供技术支持,同时也为后续相关研究提供参考。
1、实验部分
1.1 主要仪器与试剂
液相色谱仪:LC-20AT型,配二极管阵列检测器,日本岛津公司。
超声波清洗机:S300H型,德国艾尔玛公司。
电子天平:XS205DU型,d=0.01 mg/0.1 mg,瑞士梅特勒-托利多公司。
超纯水机:Milli-Q IQ 7000型,美国密理博公司。
高速冷冻离心机:Eppendorf 5810R型,德国艾本德公司。
乙腈:色谱纯,美国霍尼韦尔公司。
乙酸铵:色谱级,纯度(质量分数)不小于99.0%,上海麦克林生化科技有限公司。
冰乙酸:色谱级,上海麦克林生化科技有限公司。
对乙酰氨基酚、阿司匹林、4-甲氨基安替比林、安替比林、氨基比林、非那西丁、普拉洛芬、舒林酸、醋氯芬酸、异丙安替比林、酮洛芬、萘普生、艾瑞昔布、双氯芬酸钠、吲哚美辛、布洛芬、保泰松、塞来昔布18种非甾体抗炎药标准品:纯度(质量分数)均大于98%,中国食品药品检定研究院。
辛可芬标准品:纯度(质量分数)为100%,阿法埃莎(中国)化学有限公司。
实验用水为超纯水。
化妆品样品:市售。
1.2 溶液配制
乙酸铵溶液:0.02 mol/L,称取1.54 g乙酸铵,加入950 mL水溶解,用冰乙酸调pH值至4.2,再加水至1 000 mL。
乙腈-乙酸铵溶液:取乙腈和0.02 mol/L乙酸铵溶液,按体积比1∶1混匀即得。
19种非甾体抗炎药混合标准储备溶液:精密称取19种非甾体抗炎药标准品各约10.0 mg,置于同一只10 mL棕色容量瓶中,用乙腈-乙酸铵溶液溶解并稀释至标线,摇匀,配制成19种非甾体抗炎药的质量浓度均为1 000 μg/mL的混合标准储备溶液。
19种非甾体抗炎药系列混合标准工作溶液:取19种非甾体抗炎药混合标准储备溶液适量,用乙腈-乙酸铵溶液稀释,配制成19种非甾体抗炎药的质量浓度均分别为5、10、20、50、100、200 μg/mL的系列标准工作溶液。
1.3 仪器工作条件
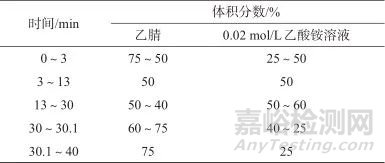
色谱柱:OSAKA SODA CAPCELL PAK C18柱(250 mm×4.6 mm,5 µm,日本OSAKA SODA公司);流动相:A相为乙腈,B相为0.02 mol/L乙酸铵溶液;检测器:二极管阵列检测器;检测波长:布洛芬的检测波长为230 nm,醋氯芬酸、双氯芬酸钠的检测波长为278 nm,其余16种非甾体物质的检测波长均为245 nm;流量:1.0 mL/min;柱温:30 ℃;进样体积:5 µL;梯度洗脱程序见表1。
表1 梯度洗脱程序
Tab. 1 Gradient elution procedure
1.4 样品处理
精密称取样品1.0 g于10 mL比色管中,加入适量乙腈-乙酸铵溶液,涡旋分散1 min,加入乙腈-乙酸铵溶液至近标线,超声提取20 min,放置至室温,用乙腈-乙酸铵溶液定容至标线,摇匀,取上清液用
0.45 μm有机滤膜过滤,即为样品溶液。
2、 结果与讨论
2.1 色谱柱选择
分别考察两种粒径(3 µm和5 µm)的OSAKA SODA CAPCELL PAK C18柱(250 mm×4.6 mm)对19种非甾体物质的分离效果。结果发现,采用3 µm粒径的C18柱时,色谱峰型较好,但一些非甾体物质较难分离,且出峰时间延长。采用5 µm粒径的C18柱时,布洛芬、保泰松和塞来昔布色谱峰形稍宽,但能将19种非甾体物质较好分离,不影响各组分的定性定量。综合考虑,选择OSAKA SODA CAPCELL PAK C18柱(250 mm×4.6 mm,5 µm)作为分离柱。
2.2 流动相选择
参考相关文献[13‒22],分别选择乙腈-0.02 mol/L乙酸铵溶液和甲醇-0.02 mol/L乙酸铵溶液作为流动相进行试验。结果表明,以乙腈-0.02 mol/L乙酸铵溶液作为流动相时,19种非甾体物质均能出峰,且调整比例后能达到分离要求;以甲醇-0.02 mol/L乙酸铵溶液作为流动相时,组分出峰时间延后,且布洛芬、保泰松、塞来昔布等组分无色谱峰,因此选用乙腈-0.02 mol/L乙酸铵溶液作为流动相进行洗脱。
2.3 提取溶剂及超声时间选择
分别考察甲醇、乙腈、乙腈-乙酸铵溶液(体积比为75∶25)和乙腈-乙酸铵溶液(体积比为1∶1) 4种不同提取溶剂及不同超声时间(10、20、30 min)时的样品处理效果。结果表明,以乙腈、乙腈-乙酸铵溶液(体积比为75∶25)为提取溶剂时,提取效果较差;以甲醇、乙腈-乙酸铵溶液(体积比为1∶1)为提取溶剂、超声20 min时均能较好地提取样品中的非甾体,考虑到流动相溶剂及溶剂峰的影响,选择乙腈-乙酸铵溶液(体积比为1∶1)作为提取溶剂,超声时间为20 min。
2.4 检测波长选择
对19种非甾体物质在190~600 nm波长范围内进行紫外光谱扫描,结果发现,大部分非甾体在245 nm附近均有较强的紫外吸收,而布洛芬在230 nm附近有较大紫外吸收,其响应值是245 nm处的16倍多,醋氯芬酸、双氯芬酸钠在278 nm附近有较大紫外吸收,其响应值是245 nm处的2倍左右。为了提高检测灵敏度,选择布洛芬的检测波长为230 nm,醋氯芬酸、双氯芬酸钠检测波长为278 nm,其余16种非甾体的检测波长为245 nm。
2.5 专属性试验
分别取空白样品溶液、19种非甾体混合标准溶液及加标样品溶液,按1.3色谱条件进行测定,色谱图如图1所示。图1结果表明,空白样品溶液无干扰,加标样品溶液中19种非甾体物质的保留时间与混合标准溶液中19种非甾体物质保留时间一致,19种非甾体物质的分离效果和峰型均良好,表明该方法具有良好的专属性。

图1 空白样品溶液、19种非甾体混合标准溶液、加标样品溶液色谱图
Fig. 1 Chromatograms of blank sample solution,19 non-steroidal mixed standard solution and spiked sample solution
1—对乙酰氨基酚;2—阿司匹林;3—4-甲氨基安替比林; ;4—安替比林;5—氨基比林;6—辛可芬;7—非那西丁; ;8—普拉洛芬;9—醋氯芬酸;10—舒林酸;11—异丙安替比林; ;12—酮洛芬;13—萘普生;14—艾瑞昔布;15—双氯芬酸钠; ;16—吲哚美辛;17—布洛芬;18—保泰松;19—塞来昔布
2.6 线性方程与方法检出限
取19种非甾体抗炎药系列标准工作溶液,按1.3仪器工作条件进行测定,以标准溶液各组分质量浓度(x,µg/mL)为横坐标,相应色谱峰面积(y)为纵坐标绘制标准工作曲线,得到各组分的线性方程与相关系数,结果见表2。取质量浓度为5 μg/mL混合标准溶液进行逐级稀释并检测,分别以3倍信噪比(S/N)和10倍信噪比(S/N)对应的质量浓度作为方法检出限和定量限,根据样品取样质量为1.0 g,稀释10倍体积换算为样品中的含量,以质量分数表示。19种非甾体抗炎药的质量浓度线性范围、线性方程、相关系数、检出限及定量限见表2。
表2 质量浓度线性范围、线性方程、相关系数、检出限及定量限
Tab. 2 Linear range of mass concentration,linear equation,correlation coefficient,detection limit and quantification limit

2.7 加标回收率与精密度试验
选取空白样品的水剂和凝胶基质,分别加入适量的19种非甾体抗炎药混合标准溶液,按1.4方法制备3种不同质量浓度水平的加标样品溶液,每个加标水平平行测定6次,计算回收率和测定结果的相对标准偏差,结果见表3。由表3可知,在水剂和凝胶基质中的平均回收率分别为93.1%~110.9%和91.3%~108.1%,测定结果的相对标准偏差分别为0.2%~3.5%和0.6%~4.2%。表明该方法在水剂和凝胶两种基质中均具有良好的准确度和精密度。
表3 加标回收率与精密度试验结果(n=6)
Tab. 3 Results of spiked recoveries and precision test (n=6)

2.8 稳定性试验
在一定条件下,有些非甾体不稳定,会发生降解或分解,从而影响定量结果的准确性。对19种非甾体进行日间(24 h)稳定性考察。取质量浓度为20 μg/mL的同一19种非甾体标准溶液,每隔一段时间进行测定,计算各组分在不同时间点的质量浓度,并计算相对标准偏差(RSD),结果见表4。由表4可知,在24 h内19种非甾体标准溶液的质量浓度无太大变化,测定结果的相对标准偏差为0.3%~2.4%,表明在室温条件下标准溶液在24 h内稳定性良好。
表4 稳定性试验结果
Tab. 4 Stability test results
3、 结语
建立了高效液相色谱测定化妆品中19种非甾体抗炎药的检测方法。该方法样品预处理简单、重现性好、灵敏度高,适用于水剂和凝胶类化妆品中19种非甾体物质的定量检测。该方法综合扩充了化妆品中非甾体的检测种类,可为日后化妆品中非甾体的非法添加及质量监管提供参考。
参考文献:
1 王利敏.非甾体抗炎药不良反应发生表现及预防[J].中国伤残医学,2016,24(7):181.
WANG Limin. Occurrence and prevention of adverse reactions to non-steroidal anti-inflammatory drugs[J]. Chinese Journalof Trauma and DisabilityMedicine,2016,24(7):181.
2 陈熠媛,陈硕崴,张谢,等.对乙酰氨基酚肝毒性研究进展[J].中国药房,2019,30(8):852.
CHEN Yiyuan,CHEN Shuowei,ZHANG Xie,et al. Research progress on hepatotoxicity of acetaminophen[J]. China Pharmacy,2019,30(8):852.
3 陈金,姚健凤.非甾体类抗炎药致老年人胃肠道不良反应研究进展[J].中华老年病研究电子杂志,2017,4(4):22.
CHEN Jin,YAO Jianfeng. Research progress of gastrointestinal adverse reactions caused by non-steroidal anti-inflammatory drugs in the elderly[J]. Chinese Journal of Geriatrics Research,2017,4(4):22.
4 吴萍,经纬俊,刘杰,等. 32例含非甾体抗炎药成分的药物致严重皮肤不良反应分析[J].中国医院用药评价与分析,2019,19(8):1 007.
WU Ping,JING Weijun,LIU Jie,et al. Analysis of 32 cases of severe cutaneous adverse reactions caused by drugs containing non-steroidal anti-inflammatory drugs[J]. Evaluation and Analysis of Drug-Use inHospitalsof China,2019,19(8):1 007.
5 王嘉熙. 5597例非甾体抗炎药的不良反应报告分析[J].药物流行病学杂志,2021,30(7):457.
WANG Jiaxi. Analysis of adverse reaction reports of 5597 cases of non-steroidal anti-inflammatory drugs[J]. ChineseJournal of Pharmacoepidemiology,2021,30(7):457.
6 WANG Yuhui,FAN Miaozhen,WANG Huideng,et al. Relative safety and efficacy of topical and oral NSAIDs in the treatment of osteoarthritis:A systematic review and meta-analysis[J]. Medicine 2022,101(36):e30354.
7 LEHRER S,RHEINSTEIN P H. Transspinal delivery of drugs by transdermal patch back-of-neck for Alzheimer's disease:a new route of administration[J]. Discov Med,2019,27(146):37.
8 国家药品监督管理局.国家药监局关于发布《已使用化妆品原料目录(2021年版)》的公告(2021年 第62号)[EB/OL].(2021-04-30)[2024-03-12].https://www.nmpa.gov.cn/xxgk/ggtg/hzhpggtg/jmhzhptg/20210430162707173.html.
National Medical Products Administration. Announcement of National Medical Products Administration on the release of the Catalogue of Used Cosmetic Raw Materials (2021 Edition)(No. 62 of 2021)[EB/OL].(2021-04-30)[2024-03-12].https://www.nmpa.gov.cn/xxgk/ggtg/hzhpggtg/jmhzhptg/20210430162707173.html.
9 国家药品监督管理局.国家药监局关于更新化妆品禁用原料目录的公告(2021年第74号)[EB/OL].(2021-05-28)[2024-03-12].https://www.nmpa.gov.cn/xxgk/ggtg/hzhpggtg/jmhzhptg/20210528174051160.html.
National Medical Products Administration. Announcement of National Medical Products Administration on Updating the List of Prohibited Ingredients for Cosmetics (No. 74 of 2021)[EB/OL].(2021-05-28)[2024-03-12]. https://www.nmpa.gov.cn/xxgk/ggtg/hzhpggtg/jmhzhptg/20210528174051160.html
10 王静,刘燕,杨琪,等. HPLC法测定双氯芬酸钠有关物质[J].中国药师,2020,23(6):1 226.
WANG Jing,LIU Yan,YANG Qi,et al. Determination of diclofenac sodium related substances by HPLC[J]. China Pharmacist,2020,23(6):1 226.
11 王南南,刘发贵.顶空-气相色谱法测定醋氯芬酸中的残留溶剂[J].分析测试技术与仪器,2021,27(3):214.
WANG Nannan,LIU Fagui. Determination of residual solvent in aclofenac by headspace-gas chromatography[J]. Analysis and Testing Technology and Instruments,2021,27(3):214.
12 言慧洁,刘伟,夏青松,等. UPLC-MS/MS法同时检测抗风湿中药制剂中非法添加的12种非甾体抗炎药[J].中国药房,2017,28(27):3 871.
YAN Huijie,LIU Wei,XIA Qingsong,et al. Simultaneous detection of 12 non-steroidal anti-inflammatory drugs illegally added in traditional Chinese medicine preparations for rheumatism by UPLC-MS/MS[J]. China Pharmacy,2017,28(27):3 871.
13 国家药典委员会.中华人民共和国药典(2020年版):二部[M].北京:中国医药科技出版社,2020.
National Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (2020 edition):Part Ⅱ[M]. Beijing:China Medical Science and Technology Press,2020.
14 高翔,王涛,贾首前,等. HPLC法测定小儿酚氨咖敏颗粒中对乙酰氨基酚含量[J].世界最新医学信息文摘,2019(78):266.
GAO Xiang,WANG Tao,JIA Shouqian,et al. Determination of acetaminophen in children's phenolamine camin granules by HPLC[J]. World Latest Medicine Information,2019(78):266.
15 李玲,陈乃江,姜燕.保泰松片HPLC含量检测方法的建立[J].中国医药科学,2015,5(17):61.
LI Ling,CHEN Naijiang,JIANG Yan. Establishment of HPLC method for determination of butazone tablets[J]. China Medicine and Pharmacy,2015,5(17):61.
16 聂安军,周英,吕文俊,等.塞来昔布片中塞来昔布的含量测定方法研究[J].临床医药文献电子杂志,2019,6(5):164.
NIE Anjun,ZHOU Ying,LYU Wenjun,et al. Study on determination method of celecoxib in celecoxib tablets[J]. Electronic Journal of Clinical Medical Literature,2019,6(5):164.
17 逯小萌.高效液相色谱法测定氨糖美辛肠溶片中吲哚美辛含量[J].中国药业,2014,23(24):74.
LU Xiaomeng. Determination of indomethacin in aminometacin enteric-coated tablets by high performance liquid chromatography[J]. China Pharmaceuticals,2014,23(24):74.
18 赵大伟,王佩华.高效液相色谱法测定普拉洛芬滴眼液中普拉洛芬含量[J].中国科技信息,2008,20(23):200.
ZHAO Dawei,WANG Peihua. Determination of praprofen in Praprofen eye drops by high performance liquid chromatography[J]. China Science and Technology Information,2008,20(23):200.
19 刘彬果,叶盛英.高效液相色谱法测定感冒灵颗粒中咖啡因、阿司匹林和非那西丁含量[J].中国药业,2020,29(21):75.
LIU Binguo,YE Shengying. Determination of caffeine,aspirin and phenacetin in Ganmaoling granules by high performance liquid chromatography[J]. China Pharmaceuticals,2020,29(21):75.
20 程侯连,杜学勤,王增仙,等. HPLC法测定复方醋氯芬酸缓释微丸含量及稳定性考察[J].沈阳药科大学学报,2019,36(9):818.
CHENG Houlian,DU Xueqin,WANG Zengxian,et al. Determination of compound acelofenac sustained-release pellets by HPLC and its stability[J]. Journal of Shenyang Pharmaceutical University,2019,36(9):818.
21 卢彦芳,李飞高,张志清. HPLC法测定艾瑞昔布片的含量[J].中国药房,2013,24(45):4 301.
LU Yanfang,LI Feigao,ZHANG Zhiqing. The content of eracib tablets was determined by HPLC[J]. China Pharmacy,2013,24(45):4 301.
22 罗敏婷,何海彤,伍志航.高效液相色谱法测定植物精油中双氯芬酸钠的含量[J].香料香精化妆品,2020,48(6):26.
LUO Minting,HE Haitong,WU Zhihang. Determination of diclofenac sodium in plant essential oil by high performance liquid chromatography[J]. Flavour Fragrance Cosmetics,2020,48(6):26.
引用本文: 张江维,张弦,谭杰,等 . 高效液相色谱法测定化妆品中19种非甾体抗炎药[J]. 化学分析计量,2024,33(5):12. (ZHANG Jiangwei, ZHANG Xian, TAN Jie, et al. Determination of 19 non-steroidal anti-inflammatory drugs in cosmetics by high performance liquid chromatography[J]. Chemical Analysis and Meterage, 2024, 33(5): 12.)

来源:化学分析计量


