您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-03-02 09:11
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:16条资讯,阅读时长约:3分钟 」
恒瑞PD-1二线治疗肝癌适应症即将获批。恒瑞PD-1卡瑞利珠单抗第2个适应症的上市申请(CXSS1900023)已处于"在审批"状态,预计即将获批上市,用于二线治疗肝癌。卡瑞利珠单抗也将成为国内首个获批治疗肝癌的PD-1单抗。2019年5月,恒瑞卡瑞利珠单抗正式获得NMPA批准,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者的治疗。目前,该新药已有3个新适应症申报上市,分别是肝细胞癌、非鳞非小细胞肺癌和食管鳞癌。
1.长春百克鼻喷冻干流感减毒活疫苗获批。长春百克的鼻喷冻干流感减毒活疫苗获国家药监局批准上市,成为国内获批的首个采用鼻腔喷雾给药方式接种的流感疫苗。该疫苗是基于基因重组技术,通过冷适应(ca)流感病毒供体株与野生型(wt)流感病毒重组制备的,经鼻喷雾给药。与传统的灭活疫苗相比,减毒活病毒疫苗具有模拟天然感染的优点,可诱导局部中和抗体、细胞免疫应答和更持久的保护作用,而且采用鼻腔喷雾给药方式接种,使用方便,易于大规模免疫。
2.华海药业左乙拉西坦片通过一致性评价。华海药业4类仿制药左乙拉西坦片获国家药监局批准上市,并视同通过一致性评价。左乙拉西坦片主要用于成人及4岁以上儿童癫痫患者部分性发作(伴或不伴继发性全面性发作)的治疗;成人及16岁以上青少年癫痫患者全面性强直阵挛发作的加用治疗。该药原研药由UCB公司研发,2006年获批进口中国。目前,该品种获批的国内厂商有京新药业、普洛康裕、信立泰等。2018年左乙拉西坦片全国等级医院销售额约人民币8.94亿元。
3.药明奥测开发出三款新冠病毒检测试剂盒。2月26日,上海药明奥测宣布已成功研发三款新型冠状病毒检测试剂盒,包括:2019新型冠状病毒IgM抗体检测试剂盒(酶联免疫法)、2019新型冠状病毒IgM/IgG抗体检测试剂盒(酶联免疫法)及2019新型冠状病毒核酸检测试剂盒(PCR-荧光探针法)。这三款科研级的试剂盒形成一套“整合检测”方案,能够帮助医疗机构快速、准确地检测新冠病毒,助力各级疾控部门开展疫情防控。
4.和铂医药PD-L1抗体HBM9167在美获孤儿药资格。2月27日,和铂医药宣布,其人源化IgG1抗PD-L1单克隆抗体HBM9167的Ⅱ期试验已获得FDA批准,并被授予治疗鼻咽癌的孤儿药资格。HBM9167(又称KL-A167)由科伦药业控股子公司科伦博泰开发,和铂医药拥有其在大中华地区以外的全球开发和商业化权益。目前,HBM9167在中国正在开展治疗鼻咽癌、复发或难治性经典型霍奇金淋巴瘤等多个肿瘤适应症的Ⅰ期和Ⅱ期临床试验,HBM9167已初步显示出良好的的安全性。
5.百济神州新一代B-RAF抑制剂临床新进展。MapKure公司、百济神州以及SpringWorks公司联合宣布,其新一代B-RAF抑制剂BGB-3245治疗晚期或复发性实体瘤患者的Ⅰ期临床在澳大利亚已实现首例患者给药,同时该在研药的新药研究申请(IND)获得FDA许可。据悉,这项Ⅰ期试验是一项开放性、剂量递增和剂量扩展的首次人体试验,试验设计旨在确定剂量以及评估BGB-3245的耐受性,并根据初期抗肿瘤活性信号,有可能开展分组拓展试验。
6.贝达药业2019年全年净利2.23亿。2月27日,贝达药业发布业绩快报,2019年1-12月实现营业收入15.47亿元,同比增长26.38%,化学制药行业平均营业收入增长率为11.80%;归属于上市公司股东的净利润2.23亿元,同比增长33.9%,化学制药行业平均净利润增长率为11.70%。公告显示,报告期内贝达药业产品埃克替尼销售继续放量,全年实现营业总收入15.47亿元,较去年同期增长26.38%;归属于上市公司股东的净利润2.23亿元,较去年同期增长33.90%。
1.Biohaven偏头痛口服新药Nurtec获FDA批准。FDA批准Biohaven公司的CGRP受体抑制剂Nurtec (rimegepant)口腔崩解片(ODT)上市,用于急性治疗成人偏头痛发作。据悉,这是首款拥有快速口腔崩解片剂型的CGRP受体小分子拮抗剂,一片Nurtec ODT能够让患者在1小时内恢复正常功能。一项Ⅲ期临床结果显示,rimegepant达到消除疼痛和最困扰患者症状的双重主要终点。86%的患者在服用一片rimegepant治疗后24小时内不需要接受其它补救疗法(例如其它止痛药)。
2. Esperion口服非他汀类复方药物获FDA批准。Esperion公司非他汀类降胆固醇口服复方疗法Nexlizet(bempedoic acid/ezetimibe)获FDA批准,治疗杂合子家族性高胆固醇血症和动脉粥样硬化性心血管疾病成人患者。Nexlizet也是首款降低低密度脂蛋白胆固醇(LDL-C)的非他汀类复方疗法。在一项Ⅲ期临床中,Nexlizet与他汀类药物(最大耐受剂量)联用能够将患者的LDL-C水平降低38%。Bempedoic acid是一款“first-in-class”的ATP柠檬酸裂解酶(ACL)抑制剂。
3.FDA批准首款止吐补救疗法。Acacia Pharma公司开发的选择性多巴胺D2/D3受体拮抗剂Barhemsys(amisulpride注射剂,APD421)获FDA批准,作为单药或与其它疗法联用,治疗和预防患者术后的恶心和呕吐症状(PONV)。Barhemsys是首款获批用于对先前预防失败患者进行补救治疗的止吐药物。在一项针对常用止吐疗法预防失败的患者群体的试验中,Barhemsys治疗组中患者的疗效显著优于安慰剂组,疗效比分别为42%和29%(p=0.003)。该公司预计将在今年下半年将Barhemsys推向市场。
4.Puma公司HER2靶向药物获批扩展适应症。Puma公司宣布,FDA批准其HER2/EGFR酪氨酸激酶抑制剂Nerlynx(neratinib)扩展适用范围,治疗转移性晚期HER2阳性乳腺癌成人患者。一项Ⅲ期临床NALA试验结果显示,与活性对照组(lapatinib+capecitabine)相比,neratinib联用capecitabine可显著改善患者的PFS。治疗组中29%患者的PFS达到12个月,而活性对照组中达到这一水平的患者比例仅为15%。治疗组中12%的患者的PFS达到24个月,而活性对照组中达到这一水平的患者比例仅为3%。此外,治疗组和活性对照组中患者的中位OS分别为21个月和18.7个月,ORR分别为32.8%和26.7%。
5.新基Revlimid组合方案治疗滤泡性淋巴瘤获NICE推荐。英格兰成本效益监管机构NICE宣布,推荐批准新基Revlimid(来那度胺)与Rituximab(利妥昔单抗)组合疗法(R2),用于先前接受过治疗的滤泡性淋巴瘤(FL,1-3a级)的成年患者。在一项评估R2治疗既往已接受治疗的FL和边缘区淋巴瘤(MZL)的III期研究AUGMENT中,与利妥昔单抗+安慰剂组相比,R2治疗组PFS具统计学意义的显著改善(中位PFS:39.4个月 vs 13.8个月,p<0.0001)。该结果也支持R2在复发/难治性FL(包括利妥昔单抗难治的FL)患者中的疗效和安全性。R2方案在美国已获批用于既往已接受治疗的FL或MZL成人患者。
6.渤健布局神经系统疾病领域。渤健与基因组医学公司Sangamo签署一项全球许可合作协议,合作开发并商业化包括ST-501用于阿尔茨海默氏病在内的多种tau蛋白相关疾病、ST-502用于帕金森氏症在内突触核病、1个针对神经肌肉疾病的未公开项目,以及9个针对神经系统疾病治疗的未公开项目。根据协议,渤健将支付3.5亿美元的预付款、潜在的高达23.7亿美元的里程碑付款以及产品销售分成。渤健将拥有ST-501、ST-502以及第三个未公开项目的独家全球权利,以及在五年的项目选择期内获得最多9个其他未公开在研药物的专有权。Sangamo将负责产品的早期开发,费用将由双方共同承担。
1.广东版磷酸氯喹治疗新冠病毒肺炎专家共识发布。为指引并规范氯喹在新型冠状病毒肺炎中的使用,广东省科技厅、广东省卫健委氯喹治疗新冠病毒肺炎多中心协作组经充分讨论后,制定了广东版磷酸氯喹治疗新冠病毒肺炎专家共识:对确诊为新型冠状病毒肺炎轻型、普通型和重型患者,排除氯喹禁忌证后,可以使用磷酸氯喹片每次500 mg,2次/天(Bid),疗程10 天。该专家共识网络预发表在《中华结核和呼吸杂志》(2020,43 )上。
2.上海市级医院3月2日起全面恢复普通门诊。上海市卫健委新闻发言人郑锦在2月28日上海市新冠肺炎疫情防控系列新闻发布会上介绍,自3月2日起,各市级医院在普通门诊全面恢复的基础上逐步恢复专家门诊,住院、手术服务持续有序开展。眼科、口腔科、五官科等部分防控高风险科室的诊疗项目也将在采取严格防护措施的前提下,于下周开始逐步恢复。目前,对暂未恢复的检查项目,医生会根据临床需要选择其他替代性诊疗手段。
3.世卫组织上调新冠肺炎疫情全球风险级别。世卫组织总干事谭德塞28日在日内瓦宣布,将新冠肺炎疫情全球风险级别由此前的“高”上调至“非常高”。他同时强调,几个国家出现了相互关联的疫情发展,但多数病例仍然可以追踪到密切接触者,而且并未发现病毒在社区自由传播的证据。只要阻断病毒传播链条,尽早发现病例、对病人进行隔离和护理、追踪密切接触者,全球仍有机会控制新冠肺炎疫情。
【华海药业】公司的左乙拉西坦片获《药品注册批件》,该药用于癫痫患者。
【科伦药业】1)2019年度实现营业收入176.40亿元(+7.88%);归母净利润9.35亿元(-22.89%)。2)公司董事、副总经理潘慧女士因工作安排需要申请辞去公司第六届董事会董事以及公司副总经理职务,同时辞去公司及相关子(分)公司其他职务,其辞职后将不再担任公司任何职务。3)公司决定终止2019年度配股公开发行证券。
【海思科】公司注销回购股份合计1,065.84万股(公司总股本的0.98%),本次回购股份注销完成后,公司总股本将由108,430万股减少至107,364.16万股。
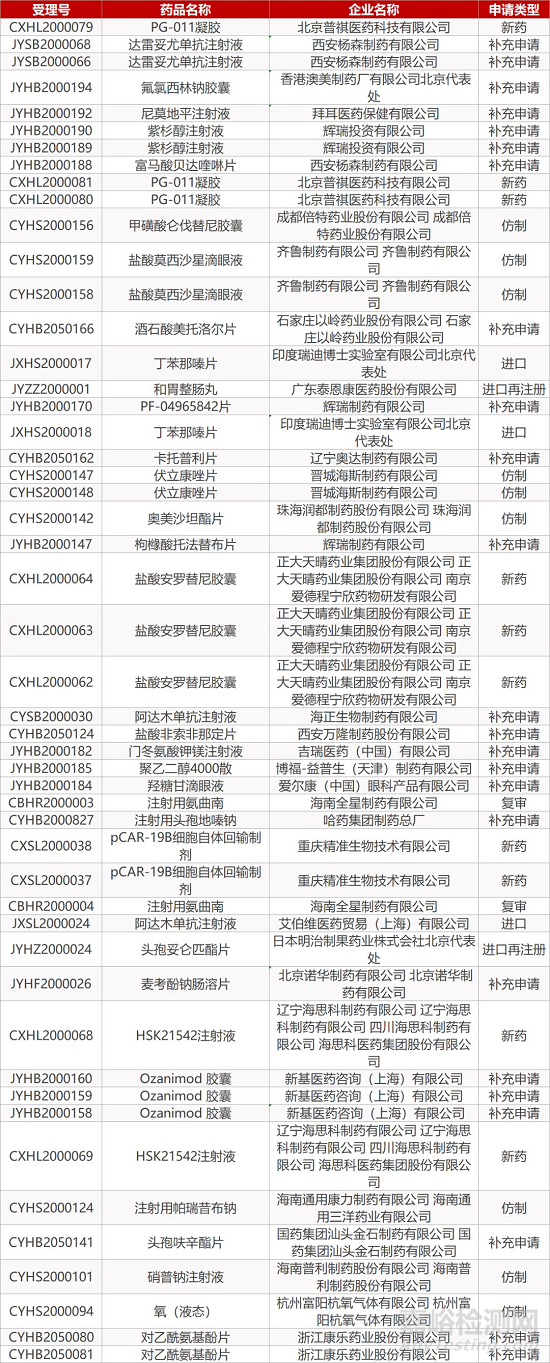
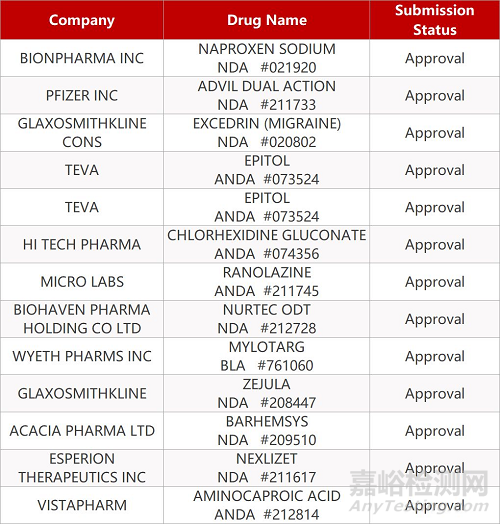

来源:药研发


