您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-21 11:34
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
赛默罗外周镇痛药获FDA临床许可。上海赛默罗生物自主研发、外周神经病理痛候选药物SR419获FDA批准,在美国直接进入II期临床试验。SR419具有全新的作用机制,没有阿片类镇痛药的副作用,并且结合外周靶点,不用通过血脑屏障,减少了很多潜在的中枢神经副作用。该药已在澳大利亚和中国开展多项不同阶段临床试验,并获得良好的安全性和有效性数据。
国内药讯
1.德琪口服SINE药物国内获批上市。德琪医药口服SINE(选择性核输出蛋白抑制剂)药物希维奥(ATG-010)获国家药监局附条件批准上市,与地塞米松联用,治疗既往接受过治疗且对至少一种蛋白酶体抑制剂,一种免疫调节剂以及一种抗CD38单抗难治的复发或难治性多发性骨髓瘤。XPOVIO®(ATG-010)是同类首款口服型SINE抑制剂,已获FDA和韩国药监部门批准上市。
2.正大天晴PD-L1启动头对头Ⅲ期临床。正大天晴发布PD-L1单抗TQB2450联合安罗替尼头对头百济神州PD-1替雷利珠单抗一线治疗晚期非鳞非小细胞肺癌(NSCLC)的Ⅲ期临床招募信息。这是天晴PD-L1单抗启动的第2项头对头临床试验。今年9月,该公司已登记启动一项TQB2450联合安罗替尼对比默沙东PD-1帕博利珠单抗一线治疗NSCLC的Ⅲ期临床,该项临床试验已在8月中旬开始全国招募。
3.瑛派药业ATR抑制剂国内报IND。上海瑛派药业1类新药IMP9064片的临床试验申请获CDE受理,适应症预计为实体瘤的治疗。IMP9064是一款ATR抑制剂,为合成致死靶向药领域的热门。在临床前研究中,IMP9064显示出较高的选择性与良好的抑制活性。该新药目前已在美国获批开展Ⅰ/Ⅱ期临床,在晚期实体瘤患者中评估IMP9064单药以及与PARP抑制剂senaparib联合治疗的安全性、药代动力学特征及疗效。
4.国产十五价HPV疫苗报IND。辽宁成大生物与北京康乐卫士生物共同申报的重组十五价人乳头瘤病毒疫苗(大肠埃希菌)的临床试验申请获CDE受理。该疫苗经过筛选目标血清型优势基因序列,构建目标血清型的工程菌株,开发检测试剂盒并优化蛋白纯化工艺,可以预防全部高危型HPV病毒和与尖锐湿疣高相关的HPV6/11型,用于预防相应型别的持续感染及由此引起的宫颈癌、外阴癌、阴道癌、肛门癌和尖锐湿疣以及CIN1/2/3、宫颈原位腺癌、VIN2/3、VaIN2/3、AIN1/2/3等相关疾病,对宫颈癌的预防效果达到96%以上。
5.丹诺医药注射用TNP-2092报IND。丹诺医药(苏州)注射用TNP-2092的临床试验申请已获CDE受理。TNP-2092是一个多靶点偶联分子,通过抑制RNA聚合酶、DNA旋转酶和拓扑异构酶IV的多靶点活性产生杀菌作用,降低耐药频率并对生物膜感染具有很强的杀菌活性,拟用于医疗器械相关生物膜感染的治疗。在美国,TNP-2092已获FDA的合格传染病产品(QIDP)资格、快速通道和孤儿药资格认定。
国际药讯
1.TSLP靶向哮喘新药获批上市。安进与阿斯利康联合开发的创新TSLP单抗药物Tezspire(tezepelumab-ekko)获FDA批准上市,用于附加维持治疗12岁以上儿童和成人严重哮喘患者。在一项Ⅲ期临床NAVIGATOR中,tezepelumab维持治疗在重度哮喘患者中达到所有主要终点和关键性次要终点。与安慰剂相比,将每年哮喘急性加重率(AAER)降低56%(p<0.001)。NAVIGATOR试验结果已发表在《新英格兰医学杂志》上。
2.首款FcRn单抗获FDA批准上市。Argenx公司FcRn拮抗剂VYVGART™(efgartigimod alfa-fcab)获FDA批准上市,用于治疗AChR阳性、成人全身性重症肌无力 (gMG)。在一项国际III期ADAPT试验中,与安慰剂相比,Efgartigimod治疗使这类患者重症肌无力日常生活(MG-ADL)评分显著改善的比例更高(68%vs30%,p<0.0001)。Efgartigimod也是首个获得FDA批准的抗FcRn单抗。再鼎医药拥有该新药在大中华区的独家权利。
3.GSK/Vir新冠中和抗体获欧盟批准上市。欧盟委员会(EC)批准葛兰素史克(GSK)和Vir公司开发的中和抗体Sotrovimab(Xevudy)上市,用于早期治疗COVID-19患者。在一项Ⅲ期COMET-ICE试验中,与安慰剂相比,sotrovimab能够将高危、新诊断的COVID-19患者的住院率或死亡率降低85%。两家公司目前正在完成体外假病毒中和实验,以评估该药能中和所有奥密克戎突变的组合,新的实验结果计划在2021年底前发布。
4.血友病B基因疗法获EMA加速评估。欧洲药品管理局(EMA)批准杰特贝林(CSL Behring)公司B型血友病基因疗法etranacogene dezaparvovec(EtranaDez)营销授权申请(MAA)进行加速评估的请求。etranacogene dezaparvovec是一种基于AAV-5的基因疗法,目前已在关键性Ⅲ期临床HOPE-B中获得积极结果,与凝血因子IX(Factor IX,FIX)预防性治疗相比,该疗法第18个月时实现FIX稳定表达后评估的ABR(年出血率)达到非劣效性标准(1.51vs4.19)。
5.渤健/卫材Aβ单抗遭欧盟拒绝批准。欧洲药品管理局(EMA)人用医药产品委员会(CHMP)拒绝批准渤健与卫材联合开发的单抗药物Aduhelm上市,用于治疗早期阿尔茨海默病(AD)。EMA认为,这款抗体药物显示它可以减少大脑中的β淀粉样蛋白斑块,但其效果与实际临床改善之间的联系仍然存在疑问。EMA的决定是在上月CHMP对Aduhelm上市申请进行负面“趋势投票”后做出的。
6.辉瑞/BioNTech新冠疫苗拟开展儿童增强针临床。辉瑞与BioNTech宣布将针对6个月至5岁以下儿童,修改一项评估其新冠疫苗的大型临床试验。两家公司计划在该子试验中,评估已完成两次主要接种的(6月-5岁)年龄组,在第二次接种至少两个月后,第三次接种(3 µg)的疗效与安全性。两家公司期望明年上半年向监管机构提交紧急使用授权(EUA)申请,以用于6个月至5岁以下儿童的新冠疫苗增强接种。
7.BridGene布局化疗耐药卵巢癌难成药靶标。BridGene Biosciences与Peter MacCallum癌症中心(Peter Mac)达成一项研究合作协议,将利用Peter Mac的卵巢化疗耐药表型筛选技术,结合BridGene专有的化学蛋白质组学IMTAC技术平台,发现治疗化疗耐药卵巢癌的新靶标,并开发小分子候选药物。BridGene正在开发针对几种癌症潜在治疗的早期项目,并预计于2023年向FDA提交新药临床试验申请。
医药热点
1.国家基金委生命部优先发展领域发布。国家自然科学基金委生命学部发布“十四五”优先发展领域,包括生物大分子的修饰、相互作用与活性调控;细胞命运决定的分子机制;配子发生与胚胎发育的调控机理;免疫应答与效应的细胞分子机制;糖/脂代谢的稳态调控与功能机制;重要性状的遗传规律解析;神经环路的形成及功能调控;认知的心理过程和神经机制;物种演化的分子机制;生物多样性及其功能等。
2.我国癌症5年生存率提升到40.5%。2021中国肿瘤早诊早治与规范化诊疗大会暨第九届国家癌症中心学术年会在深圳市召开。会上,国家癌症中心南方分中心揭牌,落户中国医学科学院肿瘤医院深圳医院。目前,我国城市癌症早诊早治项目已覆盖29个省份75个城市,开展了风险评估26.26万例,完成筛查14.97万例。我国的癌症5年生存率已从10年前的30.9%提升到40.5%。
3.中药研发2021年同比翻4倍。根据公开数据,2021年我国已有11款中药新药获批上市,分别是中国中医科学院的清肺排毒颗粒、一方制药的化湿败毒颗粒、步长制药的宣肺败毒颗粒、以岭药业的益肾养心安神片、华康医药的益气通窍片、康缘药业的银翘清热片、方盛制药的玄七健骨片、凤凰制药的芪蛭益肾胶囊、天士力的坤心宁颗粒、一力制药的虎贞清风胶囊和解郁除烦胶囊。2021年中药新药获批数量远超2016年至2020年五年总和。
评审动态
1. CDE新药受理情况(12月20日)
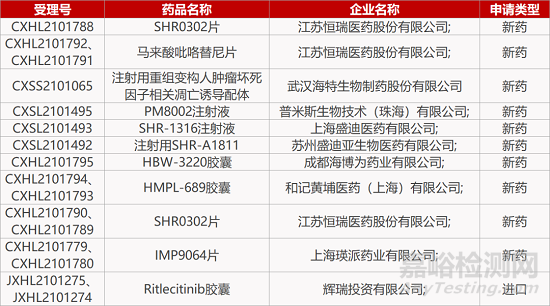
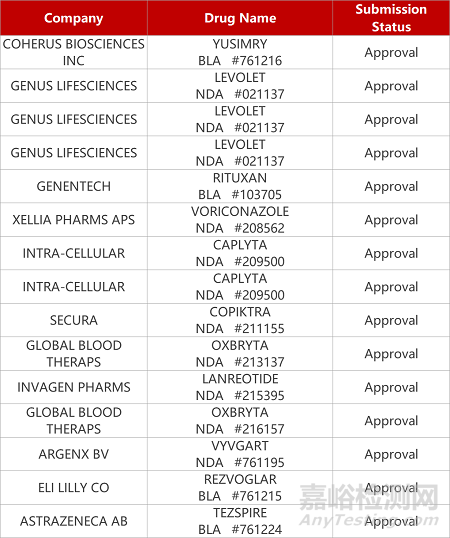

来源:药研发