您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2022-02-07 21:26
01 过渡期Transition Period
MDR有多久的过渡期?
2017年5月5日,欧盟官方期刊(Official Journal of the European Union)正式发布了欧盟医疗器械法规(MDR)。2017年5月25日,MDR正式生效。对于向欧盟销售医疗器械的制造商来说,这标志着MDR过渡期已开始。
医疗器械指令MDD(93/42/EEC)和有源植入类医疗器械指令AIMDD(90/385/EEC)被医疗器械法规MDR(EU 2017/745)取代,法规过渡期设为3年。制造商应在过渡期内更新技术文件和流程以满足法规要求。具体可以参阅法规Article 120中若干过渡条款的要求。
MDR的新要求是否可以延后执行?
不可以, MDR覆盖的所有产品都必须满足新法规的要求。过渡期结束后,不符合MDR要求的产品不可在欧盟上市。
证书未在过渡期结束前签发怎么办?
对于持有符合MDD或AIMDD的CE证书的制造商,将有3年的过渡期来满足MDR的要求。
在过渡期按照MDD和AIMDD签发的CE证书,在正式生效日期(2020年5月26日)后将继续有效,但有效期最多不能超过4年。而在过渡期结束后的证书有效性取决于法规Article 120 clause 3所述规定。
如果您符合MDD的CE证书在过渡期内失效,且又未在过渡期内取得符合MDR的CE证书。那么你的产品必须从欧盟市场退出,直到产品获得符合MDR的CE证书才可重新上市。
备注:建议您现在就开始准备转版,以确保您可以尽快向具有资质的公告机构申请新法规MDR下的CE认证。这将有助于确保您可在转版期结束前获得CE证书。
MDR执行时间轴
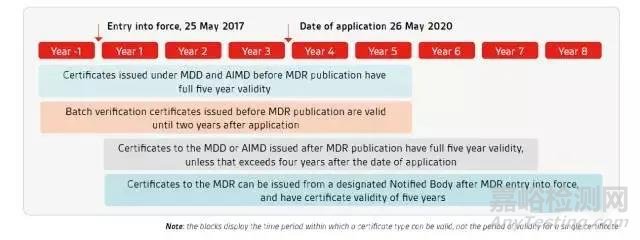
02 公告机构Notified Body Activity
当我的公告机构获取MDR的审核资质后,我还可以申请MDD证书吗?
如果您符合法规Article 120 clause 3所述的条件,是可以的。但是,这些证书在过渡期结束后,至多只有4年的有效期。也就是说,这些证书的有效期是有限的。
BSI何时开始按照MDR进行符合性评审?
所有公告机构需要获得欧盟主管当局的认可后,才能按照MDR进行审核。
我们公司的公告机构可以提供咨询服务吗?
作为公告机构,无法提供任何咨询服务。
认证专家评审组(Panel)的审核是在欧盟委员会审核之前还是之后?
认证专家评审组(Panel)的审核始终是认证流程的最后一步,将在所有符合性评估,包括任何与欧盟委员会的评审之后进行。
03 质量管理体系QMS
对于QMS是否符合MDR的要求,有具体的截止日期嘛?
无论是已满足医疗器械指令(MDD)要求的医疗器械,还是未满足MDD的医疗器械,按照医疗器械法规(MDR)认证都需要符合MDR的要求。
MDR要求制造商能够展现出有效的质量管理体系。因此,要满足MDR的认证要求,您必须按照法规Article 120的要求,在过渡期内建立合格的质量管理体系。
备注:ISO 13485:2016已于2016年3月发布,过渡期为三年。我们仍在等待协调标准的出台,通过协调标准来证实满足指令的基本要求。同样重要的是,要考虑到ISO 13485:2016是否会在将来作为欧盟医疗器械法规的协调标准。
新MDR对分包方(contract manufacturers)有什么影响?
如果分包方要为他们所服务的制造商承担责任,那么他们必须全面遵守法规要求。
如果分包方不需要为他们所服务的制造商承担责任,那么他们仅需代表制造商接受审核,包括飞行检查。
04 MDR适用范围MDR Scope
MDR涵盖哪些产品?
MDR包含了MDD及AIMDD涵盖的所有产品。新法规扩大了应用范围,覆盖一些非医疗用途的产品,如美瞳、面部填充或注射、吸脂减肥、皮肤改善和美容等产品。具体可参阅MDR中的Annex XVI。
产品分类是否有变化?
MDR对于产品的分类规则有一些变化,应用范围比MDD和AIMDD的范围更广。具体可参阅MDR中的Annex VIII。
05 技术文件Technical Documentation
IIb类植入式医疗器械的符合性评估程序是否有变化?
IIb类植入式医疗器械需要有特定产品证书(product specific certificates)——具体内容可参见医疗器械法规MDR Annex IX或Annex X 。此证书上需要显示产品的UDI。此类产品在欧盟上市前,如证书信息有变更,必须通过公告机构的审核。
IIb类植入式医疗器械的技术文档评估可以按照通用产品组中抽样原则进行嘛?
MDR指出IIb类植入式医疗器械需要通过详细的技术文档审核,类似于MDD中III类产品的技术文件要求。因此抽样的方案是不可行的。
III类产品的5年换证审核是由欧盟委员会审核,还是由发证的公告机构审核?
如果产品没有实质性的变化,5年的换证审核不需要由欧盟委员会审核。如产品有重大变更,则需要欧盟委员会的介入。
对于IIb类用于给药的器械的技术文档是否有额外要求?
MDR要求提供一套更健全的技术文件(Technical Documentation),类似于MDD / AIMD的设计文档(Design Dossier)。IIb类用于给药的有源器械仍需要接受欧盟审核,可参见MDR Annex IX或Annex XI 。
MDR涵盖的产品是否可以申请自我声明?
MDR中对于I类(非测量、非灭菌、非重复使用的产品)可以使用自我声明。
对于I类可重复使用的产品,需要提供什么样的文件以证明产品的清洁?
除了产品的清洁说明书和相关确认文件,公告机构的审核还包括其他方面,如消毒、灭菌、保养和功能测试。更多信息,可参见MDR Article 52 。
可吸收的植入产品是否需要植入卡?
是的,所有植入产品都需要植入卡。
06 临床要求Clinical Requirements
对照器械(equivalent device)是否需要进行ISO 10993测试?
有可能。从生物学角度来看,这取决于此器械和对照器械实质等同的程度。此外还需注意的是,MDR有与器械生物安全性相关的、独立的安全和性能要求,此要求也可能需要器械按照ISO 10993进行测试。
定期安全性更新报告(PSUR)是否会纳入临床评价报告(CER)?
MDR要求临床评价需要根据上市后监督(PMS)的数据定期更新。但是,将定期安全性更新报告(PSUR)纳入临床评价报告(CER)并非强制。应使用定期安全性更新报告(PSUR)所基于的上市后监督(PMS)数据来更新临床评价报告(CER)。
向公告机构报告提供上市后的定期安全性更新报告是否仅适用于III类植入式产品,还是适用于所有III类产品,还是适用于所有植入性产品?
我们认为此要求适用于所有III类产品以及所有植入性产品。
定期安全性更新报告(PSUR)和安全及性能要求概述(SSP)的产品对象是个别器械还是同系列的器械?
这将需要根据具体情况加以考虑。关于SSP,第32章要求SSP中需要包含产品识别码(Device Identifier)。关于PSUR,第86章指出PSUR可根据个别器械或同系列的器械出具。如存在此系列分组,公告机构需要制造商明确记录产品分组的理由。
07 通用规范Common Specification
什么是通用规范?
法规Article 2.71将通用规范(Common Specification)定义为“一套不同于标准的技术和/或临床要求,为器械、过程或体系提供了合规的方法”。
通用规范什么时候发布?
具体时间还不清楚。目前可以确定的是通用规范将适用于没有医用目的的器械和再生医疗器械。
08 药械组合产品 Device-drug Combination
MDR对药械组合产品的要求是否有变化?
理论上来说,除了产品本身需要额外的审查程序,MDR对药械组合产品的符合性评审要求没有变化。MDR中关于UDI、PMS、临床评价等附加要求也适用于这些产品。然而,“行为责任”(liable to act)一词已经从Rule 14中删除,因此可能会有更多的产品需要药品咨询。
09 动物源性医疗器械 Tissue of Animal Origin
您能否总结出MDR对动物源性医疗器械的影响以及法规的要求?
Rule 18的描述中增加了使用人源细胞或组织的器械。然而,除了包括UDI、PMS、临床评价等附加要求外,评价使用动物源组织的产品的方式不会有变化。
010 唯一器械标识UDI
从何时起我必须使用UDI?对于现有产品是否有过渡期?
目前,我们尚不确定UDI要求是否会按照法规Article 120和Article 123的转版要求,有可能会有针对UDI的执行出台授权法案。
是否会有记录UDI的数据库?
有,欧盟将使用EUDAMED(欧盟医疗器械数据库)记录。
对于独立产品包装以及多个产品的包装, UDI是否都适用?
如果是独立包装的产品,在每个产品的包装上都需要有UDI。对于多个产品的包装,(例如,一盒外科手套),只要求外包装显示UDI。具体请参阅法规Article 27和 Annex VI。
对于运输包装以及外包装,UDI是否适用?
MDR要求除了运输集装箱以外的包装都需要显示UDI。
欧盟是否已澄清纯软件器械UDI的使用?
是的,对软件UDI的要求已在法规Annex VI Part C Section 6.5中列出。
新的UDI要求是否与现行的美国FDA的UDI要求一致?
MDR与美国FDA对于UDI的要求是存在一定差异的。但是也有许多相似点。具体可参见法规Annex VI关于UDI的要求。
是否可以采用国际物品编码协会(GS1)颁发的UDI去满足MDR的要求?
GS1是UDI发行机构。如果GS1符合MDR Article 27的要求,那么GS1颁发的UDI可满足MDR。
获得全球贸易项目代码(GTIN)是否就符合UDI的要求?
MDR并不使用GTIN的概念。但是对于这种情况,美国FDA有类似的规定。制造商必须就欧盟主管当局和其他监管机构所要求的UDI的要求进行差距分析。有关更多信息,请参见MDR Annex VI。
如果变更UDI需要更新CE证书,这将需要多长时间?
公告机构的审核时间取决于产品变化的性质。
011 如何申请MDR的CE证书 HOW To apply for an MDR CE certificate ?
MDR的主要变化
1.扩大了应用范围
2.提出了新的概念和器械的定义
3.细化了医疗器械的分类
4.完善了器械的通用安全和性能要求
5.加强对技术文件的要求
6.加强器械上市后的监管
7.完善临床评价相关要求
8.提出Eudamed数据库的建立和使用
9.提出器械的可追溯性(UDI)
10.对NB提出严格的要求
对NB提出的严格要求
对“公告机构”,新版MDR花费大篇幅对其进行职能和要求进行描述;各NB需按照附录VII的要求重新申请MDR的三方审核的授权
MDR适用范围扩大
新MDR不仅包含了MDD及AIMDD涵盖的所有产品;还覆盖专门用于器械的清洁、消毒或灭菌的器械,以及Annex XVI列举的无预期医疗目的的产品,如美瞳、面部填充或注射、纹身、皮肤改善和美容等产品。
包含某些药械结合产品,详细请见Article1(8,9)。
包含某些由非活性或处理为非活性的人类来源组织或细胞衍生物制造的特定产品。
包含声称仅具有美容目的或另一种非医疗目的,但在功能和风险特征方面类似于医疗器械的特定产品组
声明纳米材料器械属于MDR范围,且要接受最为严格的评估程序。
包含发射离子辐射的器械和医疗用途的软件。
MDR提出了新的概念和器械的定义
MDR中增加了很多新的概念,从MDD中的14个概念,增加到现在的71个,如增加了一些临床试验方面和上市后监管方面的概念,如 “recall ,withdraw ,serious incident, clinical consent, clinical benefit(召回、撤回、严重事件、临床同意、临床受益)”.详情请见Article2
器械的分类变化
从MDD到MDR,器械仍分为四大类:I类、I*类(Is(一类灭菌)/Im(一类测量)/Ir(一类可重复使用))、IIa类、IIb类、III类,其中一类中可重复使用器械归属为I*类。
MDD中与分类相关是93/42/EEC中的 Annex IX 和相应的指南MEDDEV 2. 4/1 Rev. 9;新的MDR中Article51和Annex VIII 详细阐述了产品的分类信息。主要变化是由MDD的“18条”,改为MDR的“22条”。
器械类型 MDD MDR
NON-INVASIVE DEVICES Rule 1- Rule 4 Rule 1-Rule 4
INVASIVE DEVICES Rule 5-Rule 8 Rule 5-Rule 8
ACTIVE DEVICES Rule 9-Rule 12 Rule 9-Rule 13
SPECIAL RULES Rule 13-Rule 18 Rule 14-Rule 22
Rule1-Rule 4:NON-INVASIVE DEVICES非侵入性器械
Rule3:增加了用于体外直接从人体或人类胚胎取下体外使用的人体细胞、组织、气管,然后再植入或注入体内,此类器械为III类。
Rule 5-Rule 8:INVASIVE DEVICES侵入性器械
Rule 8:在原来的基础上添加了:有源植入器械或其相关附件,乳房植入物或心脏修补网状织物,完整或部分关节置换物,直接与脊柱接触的椎间盘置换植入物为III类。
Rule 9-Rule 13:ACTIVE DEVICES有源器械
Rule9:在原来的基础上增加了“针对治疗目的释放电离辐射的有源器械”以及“用于控制、监测或直接影响有源植入式器械”,这两大类器械均为II b类。
Rule11:新添加,提出用于提供诊断或治疗目的决策信息和监测生理过程的软件,均为II a类;其他软件类为I类。
Rule 14-Rule 22:SPECIAL RULES特殊规则
Rule14:进一步完善了“衍生自人体血液或血浆的医疗产品”分类的要求。
Rule 18:进一步完善“利用非活性或处理为非活性的人体或动物源组织或细胞或其他衍生物制成的器械”的分类要求。
Rule19:添加对纳米材料器械的分类要求。
Rule20:添加了通过吸入方式,与身体孔口相关的侵入器械的分类。
Rule 21:添加了引入人体可吸收物质到人体的器械。
Rule22:添加了具有集成或合并诊断功能的有源治疗器械的分类。
此外还删除了MDD中对血袋的单独分类。
器械的通用安全性和性能要求
由MDD中Annex 1 ESSENTIAL REQUIREMENTS 进一步完善为“ANNEX I GENERAL SAFETY AND PERFORMANCE REQUIREMENTS”;从原来的13个条款增加到现在的23个,同时MDD中 Article 13: Information supplied by the manufacturer 在MDR中作为一个单独的章节 “CHAPTER III REQUIREMENTS REGARDING THE INFORMATION SUPPLIED WITH THE DEVICE”。细化了多条性能要求,强调将风险分析和管理贯穿于设计和生产、销售、上市后监管等整个产品周期中。
技术文件的要求
MDR中添加了对技术文件内容的要求;且明确指出上市后监管计划和安全性更新报告(PSUR)都是技术文件的一部分,并要求依据上市后监管体系收集的资料对技术文件中相应信息进行更新。
技术文件的基本内容
器械说明与性能指标
包括变型和附件包含器械说明与性能指标,以及引用的前代和类似器械的信息。
制造商提供的信息
设计与制造信息
通用安全与性能要求
包含其符合附录I提供的通用安全与性能要求的证明资料。
风险利益分析和风险管理
产品验证与确认
临床前和临床数据(包含临床评价计划/报告,PMCF计划/报告);以及针对含药器械、人体/动物来源组织或其衍生物制备的器械、引入人体并被吸收器械、具有测量功能器械等的相关附加信息
上市后监督的技术文件
AnnexIII TECHNICAL DOCUMENTATION ON POST-MARKET SURVEILLANCE 详细说明了要按照Article83-86 编写上市后监管的文件,包含上市后监管计划、上市后监管报告或定期安全性更新报告(PSUR)。
符合性声明文件
ANNEX IV EU DECLARATION OF CONFORMITY 详细说明了“符合性声明”文件包含的内容。
加强器械上市后监管体系
Chapter VII POST-MARKET SURVEILLANCE, VIGILANCE AND MARKET SURVEILLANCE 着重说明上市后监管、警戒和市场监管。
建立、实施和维护上市后监管体系(见Article83)。
强调上市后监管体系贯穿整个生命周期,并不断更新。
建立“上市后监管计划”(见Article84),具体内容见Annex III。
I类器械编写“上市后监管报告”(见Article85)。
IIa、IIb和III类器械编制“定期安全性更新报告(PSUR)”(见Article86)。
PSUR需定期更新并作为技术文件的一部分。
建立警戒和上市后监管电子系统(见Article 92)。
在整个器械使用寿命期间,依据实施PMCF后取得的临床数据对临床评价及技术文件进行更新(Annex XIV part B)。
完善临床评价相关要求
新法规提出:
要求根据Article61和附录XIV partA执行、评估、报告和更新临床评价资料;
提出对特定III类和IIb类器械,CER中要考虑咨询专家小组的意见;
对植入和III类器械,提出考虑临床研究;
要求CER按照PMCF取得数据进行更新;
针对III类和可植入器械,提出了CER更新的频率;
明确证明实质等同性需考虑的特点;
要求其与风险管理的相互作用
Eudamed数据库
新法规提出:
明确欧洲医疗器械数据库(Eudamed)建立目的和包含的信息(Article 33);
信息的公开性:
要求III类器械和植入式器械,安全和临床性能信息通过Eudamed向公众开放。
提出器械的可追溯性(UDI)
除定制和研究器械外,其他器械均需建立UDI系统;
UDI信息体现在标签或包装上(不包含集装箱);
UDI-DI信息需要载明于符合性声明中(见Article27);
Annex VI Part B提出UDI-DI包含的信息;
可植入、重复使用、软件、可配置器械的UDI有特殊要求(见Annex VI Part C)
包装或标签上UDI实施的时间见Article123 (f)。
UDI 发行实体由欧盟委员会指定。
过渡性:Article 120指出“在委员会根据第27(2)条指定发行实体前,GS1、HIBCC和ICCBBA应被视为指定的发行实施

来源:Internet


