您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-03-13 22:26
摘要:非霍奇金淋巴瘤 (NHL) 是一种十分常见的造血系统恶性肿瘤。大量的基础研究证实了 B 细胞分化抗原 20(CD20)是治疗淋巴瘤的重要靶点。抗 CD20 单克隆抗体药物不仅可以治疗 NHL,还为多发性硬化、风湿性关节炎等疾病提供了更多治疗机会。本研究从 CD20 抗原靶点、抗 CD20 单克隆抗体药物作用机制以及抗 CD20 单克隆抗体药物的发展等方面进行了综述,为抗 CD20 单克隆抗体药物的发展提供参考。
国际癌症研究机构 (International Agency for Research on Cancer,IARC) 发布的 2020 年全球恶性肿瘤负担状况最新评估报告指出,恶性肿瘤将成为 21 世纪个体死亡的首要原因 [1],也是我国公民健康的一大挑战。淋巴瘤泛指起源于淋巴组织的肿瘤,是一种十分常见的造血系统恶性肿瘤,属于血液瘤。根据《中国肿瘤登记年报》的数据,2003至 2013 年,恶性淋巴瘤的发病率约为每 10 万人中 6.68 人,每年新发病数近 9 万例,位列所有恶性肿瘤发病率第 8 位。目前我国淋巴瘤患者的 5年整体生存率约为 38%,远低于美国的 64% [2]。淋巴瘤根据病理分为霍奇金淋巴瘤 (Hodgkin lymphoma,HL) 和非霍奇金淋巴瘤 (non-Hodgkin lymphoma,NHL)2 种。80%~ 90%的淋巴瘤属于 NHL[3],而大部分 NHL 属于 B 细胞淋巴瘤,其中超过 95%的 B 细胞淋巴瘤都有 B 细胞分化抗原20(CD20) 高表达的特征 [4—5]。
生物药物的研发及市场化是健康中国的一个重要组成部分,而单克隆抗体药物是生物药物中最重要的一大类药物。全球已有 80 多种抗体药物获批上市,用于治疗恶性肿瘤、自身免疫性疾病和代谢疾病等。对于血液恶性肿瘤之一的 B 细胞淋巴瘤,抗体类药物具有特异性靶向作用、不良反应小、疗效显著的优点。数十年来的医学研究成果为治疗 B细胞淋巴瘤提供了明确的药物靶点,包括 CD20。深入研究及开发 CD20 靶点的单克隆抗体药物对于治疗血液恶性肿瘤来说极为重要。
本研究将从 CD20 靶点和抗体药物的作用机制、发展进程及未来研究方向等方面进行综述,以期为抗体药物的研发提供参考。
一、CD20靶点及其抗体药物
1.1 CD20 靶点
CD20 作为抗体类药物中十分重要的靶点,是一种由 279 个氨基酸组成的跨膜磷蛋白,同时也是特有的、存在于人类 B 淋巴细胞表面的标识,相对分子质量为 33 000 ~ 37 000,有 4 个跨膜结构域,其中,主要的抗原表位位于细胞质膜内侧的第三及第四跨膜区之间 [6],构成的主要抗原表位对 B 淋巴细胞的分化和增殖具有非常重要的调节作用 [7—9]。CD20 表达于除浆细胞 ( 分泌免疫球蛋白的 B 细胞 )外的发育分化各阶段的 B 细胞表面,通过调节跨膜钙离子流动直接对 B 细胞起调节作用 [10]。B 淋巴细胞抗原 CD20 是在 B 淋巴细胞表面表达的糖基化磷蛋白,是一种 B 细胞分化抗原,仅位于前 B 细胞和成熟 B 细胞,在 95%以上的 B 细胞淋巴瘤中均有表达 [11]。在人体 B 细胞从前 B 细胞到成熟 B细胞的发育分化周期中,CD20 的抗原表面丰度逐渐增加,但在 B 细胞发育的最初和最后阶段不表达。CD20 在 B 细胞淋巴瘤、毛细胞白血病、B 细胞慢性白血病和黑色素瘤的肿瘤干细胞中均有表达,但在造血干细胞、血浆细胞和其他正常组织中均不表达 [12]。
CD20 在正常生理组织和肿瘤组织中的差异性表达使 CD20 可以作为一个辨识度良好的 B 细胞疾病的靶点。由于造血干细胞、部分成熟前的 B 细胞和浆细胞中没有此抗原,即使抗 CD20 单抗将正常的 B 细胞和肿瘤细胞一起大量清除,成熟前的 B细胞和造血干细胞也能补充 B 细胞的数量,同时浆细胞也能负责维持人体的免疫功能 [13—14],这对于一个抗肿瘤靶点来说,无疑具有得天独厚的优势。
1.2 CD20 抗体药物
近 30 年 来, 已 有 针 对 约 20 个药物靶点的80 多种抗体药物获批上市,其中有 4 个药物靶点研究较广、成药较多,被市场上各大制药企业争相生产上市,其分别为 CD20 单抗药物、抗表皮生长因子受体 (EGFR) 单抗药物、程序性细胞死亡蛋白 1(PD-1) 单抗药物、人表皮生长因子受体 2(HER2) 单抗药物。从世界卫生组织 (World Health Organization,WHO) 收录的在研和上市药物情况可以看出 ( 见表 1[15]),CD20 靶点相关的上市药物数量仍位列第一,足以表明市场现状及其需求。
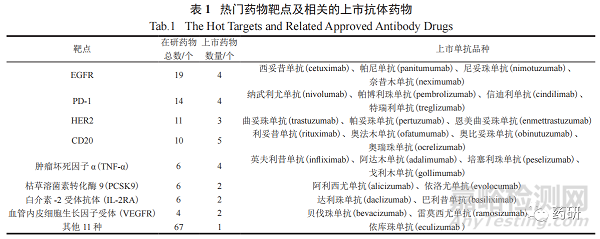
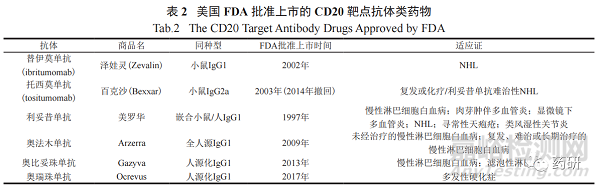
又如表 2 所示,美国 FDA 批准上市的 CD20靶点抗体类药物共有 6 个 [16],包括 2 个鼠抗体偶联同位素药物。其中利妥昔单抗 —— 美罗华(rituximab) 获得较大的市场占有率,在 2019 年的销售额接近 70 亿美元,奥法木单抗、奥比妥珠单抗、奥瑞珠单抗也分别在 2009、2013、2017 年上市,用于治疗白血病和多发性骨髓瘤。
二、CD20单抗药物的作用机制
CD20 抗原具有 4 个跨膜结构域、2 个环区(79 ~ 84 个氨基酸的短环和 142 ~ 188 个氨基酸的大环 )。作用在大环或短环上的抗体均有成功成药的例子,上市的 CD20 抗体药物的结合位点可能在短环或大环上,以美罗华为代表的抗体结合位点位于大环上,称为Ⅰ型 (type Ⅰ )CD20 抗体 ;以百克沙为代表的抗体结合位点位于短环上,称为Ⅱ型 (type Ⅱ )CD20 抗体。已上市的抗体药物中,Gazyva 为Ⅱ型 CD20 抗体,Arzerra 在大环和短环上均有结合,而 Ocrevus 则在大环上有部分结合。
靶向 CD20 抗体的抗肿瘤活性主要包括诱导凋亡作用、补体依赖的细胞毒性作用 (complement dependent cytotoxicity,CDC) 和抗体依赖的细胞介导的细胞毒性作用 (antibody-dependent cell-mediated cytotoxicity,ADCC),Ⅰ型和Ⅱ型 CD20 抗体作用于 CD20 的位点不同,其主要作用机制也不同 [16]。 2 种类型的抗体均有较强的 ADCC 活性,Ⅰ型抗体的 CDC 活性较强,诱导凋亡的作用较弱,会引起 CD20 的聚集而导致抗体本身出现内吞行为,细胞膜表面表达的 CD20 同时也会减少 [16—17],Ⅱ型抗体具有较强的诱导凋亡活性,但 CDC 活性较弱,不引起 CD20 的聚集内化和抗体内吞化。
基于此,以 CD20 为靶点的抗体药物的抗肿瘤活性作用主要包括内吞作用、CDC 和 ADCC[18]。其中内吞作用是通过形成吞噬溶酶体来促进细胞凋亡的机制,加速清除体内 CD20 阳性 B 细胞以达到治疗的目的。CDC 的作用原理为通过抗体和抗原的特异性结合,活化补体后形成膜攻击复合物 (membrane attack complex,MAC),MAC 能形成跨越靶细胞膜的孔道,使靶细胞内外的离子可以自由交换,从而溶解靶细胞、达到治疗的目的。ADCC 的作用机制为抗体与靶细胞表面的抗原特异性结合,巨噬细胞、中性粒细胞等细胞借助抗体的结晶片段 (crystallizable fragment,Fc) 与 FcγR(IgG Fc 段受体 ) 结合,从而杀伤靶细胞。
三、CD20单抗药物的发展进程
人体的免疫系统主要是以 T 细胞为主导的细胞免疫,但对于肿瘤细胞,仅依靠自身免疫系统产生的抗体通常是不够的。1975 年,KOHLER 和MILSTEIN 发明了淋巴细胞杂交瘤技术,使大量制备单克隆抗体成为可能。这种杂交细胞既可以像 B淋巴细胞一样分泌抗体,又可以像骨髓瘤细胞一样无限增殖。
杂交瘤技术的应用大幅度地促进了包括 CD20抗体在内的单克隆抗体药物的发展,抗体药物也从最初的鼠源型单克隆抗体逐渐发展到人 - 鼠嵌合型单克隆抗体、人源化单克隆抗体和全人源单克隆抗体 ( 见表 3[19])。随着抗体中鼠源比例的减小,个体的排异反应相应减少,同时抗原结合能力有所下降,直至全人源抗体的出现,显示了其与人体免疫系统的良好相容性。

以 CD20 为靶点的抗体药物的发展经历了三代:第一代抗 CD20 单抗主要是以利妥昔单抗为代表的鼠源或嵌合抗体,能特异性结合 B 淋巴细胞上的CD20[20],通过 ADCC 与 CDC,最终导致细胞凋亡 [21] ;第二代抗 CD20 单抗是以奥法木单抗为代表的全人源单抗,用于氟达拉滨和阿仑珠单抗治疗无效的顽固性慢性淋巴细胞白血病,通过与 CD20 分子上的小环抗原靶向结合,促使细胞溶解,诱导细胞凋亡,从而专一性地杀灭 B 淋巴瘤细胞而对其他正常组织无不良影响 [22—23] ;第三代抗 CD20 单抗以 Fc 片段糖基化修饰的奥比妥珠单抗为代表,其适应证包括慢性淋巴细胞白血病,以及联合苯达莫司汀二线治疗复发性滤泡性淋巴瘤 [24—25]。
3.1 第一代抗 CD20 单抗药物
第一代抗 CD20 单抗药物以利妥昔单抗为代表,由日本 IDEC 公司研发,是首个获批用于临床治疗NHL 的人鼠嵌合抗体,于 1997 年批准上市 [26]。利妥昔单抗由鼠抗 CD20 单抗的可变区 Fab 和人 IgG1抗体稳定区 Fc 片段构成,含 1 328 个氨基酸残基,相对分子质量约为 1.44×105 [27]。利妥昔单抗可诱导CDC 和 ADCC,能够杀伤淋巴瘤细胞。自上市以来,广泛应用于治疗表达 CD20 的恶性 B 细胞淋巴瘤以及慢性淋巴细胞白血病 [28—29]。利妥昔单抗和化疗药物的联合使用已成为治疗某些特定类型 NHL 的标准方案,随后又被批准用于治疗中至重度活动性风湿性关节炎、CD20 阳性的慢性淋巴细胞白血病和韦格纳肉芽肿等疾病 [30—31]。
第一代抗 CD20 单抗药物,除了重磅产品利妥昔单抗,还包括日本 IDEC 公司研发的泽娃灵和英国 GSK 公司研发的百克沙 [16]。泽娃灵是全球首个放射性核素铟 111 或钇 90 标记的抗 CD20 单抗,被批准用于治疗难治性复发性 B 细胞 NHL。携带放射性核素的抗 CD20 单抗注入患者体内后,会与表达 CD20 的成熟 B 细胞和 B 细胞肿瘤细胞结合,通过所携带的放射性核素释放的放射线来杀死这些细胞 [32]。百克沙和泽娃灵类似,利用单抗和放射性分子碘 131 相连,用于治疗复发性难治性滤泡或变形的 NHL[33]。泽娃灵和百克沙均需要在专门的核医学部门进行治疗,所以在临床推广上存在较多困难。
虽然,第一代抗 CD20 单抗在抗肿瘤治疗上取得了巨大的成功,但由于第一代抗 CD20 单抗属于鼠源型单抗或嵌合型单抗,人源化程度不高,部分患者使用后会产生耐药或不良反应。并且由于低水平的补体活性或激活补体的细胞毒性降低,一些淋巴细胞对 CDC 具有抵抗作用。此外,利妥昔单抗可导致表达 CD20 的 B 细胞凋亡而直接抑制 B 细胞生长 [34]。因此,随着抗体人源化技术的发展,人源化程度更高、不良反应更小的第二代单抗进入市场。
3.2 第二代抗 CD20 单抗药物
为了解决第一代抗体免疫原性高的缺陷,研究者开始进行第二代抗 CD20 单抗的研发。来自丹麦Genmab 公司的奥法木单抗是首个全人源抗 CD20单抗。相比利妥昔单抗,奥法木单抗在细胞膜表面更易结合 CD20 抗原,并有较慢的脱离速率和更高的补体活性 [35]。体外试验结果证明,奥法木单抗的 Fab 区域与 CD20 分子结合,Fc 区域通过调节免疫因子的功能而导致 B 细胞裂解,能有效诱导对利妥昔单抗产生耐药性的细胞凋亡和 CD20 低表达的恶性 B 细胞产生 CDC 细胞毒性 [36]。
由于奥法木单抗在Ⅲ期临床试验中表现出可持续的临床治疗效果,于 2009 年获得美国 FDA 批准用于治疗对氟达拉滨和利妥昔单抗耐药的慢性淋巴细胞白血病 [36—37] ;欧洲药品管理局 (European Medicines Agency,EMA) 于 2010 年也批准了奥法木单抗在欧盟国家的销售和使用。此外,第二代抗CD20 单抗还有维妥珠单抗 (vedolizumab) 和奥瑞珠单抗,二者的体外作用机制相似 [38]。维妥珠单抗是高度人源化的Ⅰ型 IgG1 抗 CD20 单抗,具有90%~ 95%的人抗体序列,主要针对利妥昔单抗治疗无效的 NHL。奥瑞珠单抗是于 2017 年批准上市的全人源抗 CD20 单抗,用于治疗 T 细胞介导的多发性硬化 [39]。
3.3 第三代抗 CD20 单克隆抗体
为了改善第二代抗体的缺点,第三代抗 CD20单抗提高了抗体的特异性和与抗原结合的亲和力,在 Fc 部分进行了糖基化修饰 [40]。2013 年,来自美国罗氏制药公司的人源羰基化Ⅱ型单抗 —— 奥比妥珠单抗获得美国 FDA 批准上市,主要适用于未经治疗的慢性淋巴细胞白血病患者以及联合苯达莫司汀二线治疗复发性滤泡性淋巴瘤 [31]。美国罗氏制药公司公布了奥比妥珠单抗和利妥昔单抗在治疗滤泡性淋巴瘤的Ⅲ期临床试验结果,该研究表明对于之前未接受治疗的滤泡性淋巴瘤患者,奥比妥珠单抗能够显著提高患者的无进展生存期。然而,在弥漫大 B 细胞淋巴瘤 (diffuse large B cell lymphoma,DLBCL) 的Ⅲ期临床试验中,通过比较奥比妥珠单抗和利妥昔单抗的头对头试验,观察到奥比妥珠单抗的主要临床终点对先前未经治疗的 DLBCL 患者的无进展生存时间 (progression-free survival,PFS)虽有显著延长,但并没有达到预设的临床终点 [41]。
目前,抗 CD20 单抗已经发展到第三代,每一代抗体药物均有各自特有的临床应用价值。通过表4 中三代产品代表药物的比较可知 [42],其适应证不尽相同,各有优缺点,但后续产品确实并未在前产品的领域中获得显著突破。

利妥昔单抗即美罗华,销量一直远高于其他抗CD20 单抗 [33]。从慢性淋巴细胞白血病到类风湿性关节炎,再到罕见病中的韦格纳芽肿、显微镜下多血管炎等,美罗华可用于多种适应证 [43]。
CD20 至今仍然是被验证了的充满活力的靶点,在免疫治疗领域还将发挥重要作用,如作为免疫毒素、嵌合抗原受体 T 细胞疗法 (chimeric antigen receptor T,CAR-T) 靶点等,应用于多种临床适应证 [44—46]。
四、我国CD20单抗药物的发展概况
我国一直致力于改善民生问题,全力降低医疗成本,其中很大一方面是降低用药价格,特别是纳入医保目录的药品。并且,我国十分鼓励生物类似药的发展,目前我国有 270 个生物类似药处于研发状态,约有一半处于临床前研究阶段,其中 65 个已提交临床申请,有 10 个已获得临床批准,有望近期开展临床试验 [47]。国内获批的单抗产品主要针对 CD20 阳性的滤泡性 NHL 和弥漫大 B 细胞性NHL,国内针对 CD20 靶点的新申报生物制品情况见表 5。此外,由上海复宏汉霖生物制药有限公司研发的生物类似药 —— 汉利康,是我国首个利妥昔单抗注射液生物类似药,于 2019 年 2 月获批上市。

在中国,除了用 CD20 单抗药物治疗 B 细胞淋巴瘤外,以 CD20 为靶点的 CAR-T 和抗体偶联药物 (antibody drug conjugat,ADC) 也在积极开发中。以 CAR-T 为例,针对血液瘤复发后耐药性更强的特点,已有多家企业及机构开展试验,绝大多数试验地点位于我国,为我国 CD20 靶点抗体的发展提供了优厚的条件 [48]。
五、展望
通过众多临床试验及以往多年研究积累,证实了 CD20 靶点是治疗 B 细胞淋巴瘤的重要靶点,以CD20 为靶点研发出的药物在临床治疗 B 细胞淋巴瘤中发挥了关键作用。然而,肿瘤的发展可能受多因素、多基因作用影响,通过多个靶点联合用药,或多功能药物治疗可能对进展期肿瘤更有效 [49—52]。现阶段,基于 2 个或多个已知靶标的联合靶向治疗方法已被越来越多地应用于临床试验和研究中 [53—55]。结合 2 个不同靶标的双特异性抗体药物已引起研究者浓厚的兴趣 [56],多种与 CD20 靶点结合的双特异性抗体药物以及 CAR-T 治疗已显示了初步的成果,如美国罗氏制药公司研发的治疗 DLBCL 的 CD3/CD20 双抗正在进行临床试验,有望为更多的双特异性抗体药物的发展开辟一条新的道路。

来源:Internet


