您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-06-13 11:31
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
上海优锐引进COPD吸入剂报IND。优锐医药从Verona公司引进的1类新药吸入用ensifentrine混悬液(RPL554)的临床试验申请获CDE受理。RPL554是一款吸入式磷酸二酯酶-3和-4(PDE3和PDE4)双抑制剂,目前正在国际Ⅲ期临床中评估用于慢性阻塞性肺病维持治疗的安全性和有效性。优锐医药拥有该新药的大中华区开发和商业化的独家授权。
国内药讯
1.首款TROP-2-ADC在华获批上市。NMPA批准云顶新耀引进新药注射用戈沙妥珠单抗上市,用于治疗既往两种系统治疗(至少一种为针对转移性疾病的治疗)的不可切除的局部晚期或转移性三阴性乳腺癌。这是全球首款获批上市的TROP-2靶向抗体偶联药物,是吉利德通过收购Immunomedics公司所得。在一项国际Ⅲ期临床ASCENT中,戈沙妥珠单抗与化疗相比使患者死亡风险降低49%,使疾病进展或死亡风险降低57%。
2.百济神州PD-1获批治疗鼻咽癌。百济神州PD-1替雷利珠单抗(百泽安)获国家药监局批准第9项适应症,用于一线治疗复发或转移性鼻咽癌患者。在一项Ⅲ期临床RATIONALE 309中,与对照组相比,替雷利珠单抗联合吉西他滨和顺铂显著提高患者的PFS(中位PFS:9.2个月vs7.4个月),在6、9和12个月时的PFS率分别为66.1%、51.0%和35.7%(vs53.0%、21.6%和12.2%)。
3.恩格列净在华获批治疗心衰。勃林格殷格翰与礼来联合开发的恩格列净片(欧唐静)获NMPA批准一项新适应症,用于治疗射血分数降低的心力衰竭成人患者。在一项Ⅲ名期临床中,与安慰剂相比,恩格列净可将患者的心血管死亡和因为心衰而住院构成的复合终点风险降低25%;将患者因为心衰而首次或再次住院的风险降低30%。恩格列净是一款SGLT2抑制剂,此前已在中国获批用于2型糖尿病患者。
4.百奥泰新冠中和抗体获批临床。百奥泰开发的新冠双特异性中和抗体「注射用 BAT2022」获国家药监局临床试验默示许可。BAT2022通过特异性结合病毒刺突蛋白上的两个不同表位来阻断病毒侵染宿主细胞, 直接阻断病毒与宿主细胞受体血管紧张素转化酶2(ACE2)的结合,从而阻断病毒侵染细胞。在体外真病毒细胞感染实验中,BAT2022显示出对多种突变株均有高效中和能力。
5.华奥泰PD-L1/TIGIT双抗报IND。华奥泰生物开发的1类生物制品HB0036注射液的临床试验申请获CDE受理。HB0036是一款靶向PD-L1和TIGIT的双特异性抗体,旨在高特异性结合PD-L1和TIGIT两个关键免疫检查点,阻断PD-1/PD-L1和TIGIT/CD155两条信号通路的信号传导,从而解除其介导的免疫抑制作用,重新激活细胞毒性T淋巴细胞和NK细胞对肿瘤细胞的杀伤作用。今年1月,该产品已在美国获批开展临床试验。
国际药讯
1.安斯泰来贫血新药获NICE批准。珐博进与安斯泰来联合开发的罗沙司他(Evrenzo)获英国国家卫生与临床优化研究所(NICE)批准,纳入英国国家医疗服务体系(NHS),用于无缺铁的3-5期慢性肾脏病(CKD)相关的贫血患者和未接受透析的患者。Evrenzo是全球首款口服HIF-PH抑制剂,已在中国、日本和欧盟获批用于非透析依赖(NDD)和透析依赖(DD)成人CKD贫血的治疗。安斯泰来上个月宣布,4项试验汇总分析显示,Evrenzo与促红细胞生成刺激剂(ESA)相比,并没有增加心血管事件或死亡的风险。
2.蓝鸟基因疗法获FDA专家推荐上市。FDA细胞、组织和基因疗法咨询委员会推荐批准蓝鸟生物基因疗法elivaldogene autotemcel(eli-cel)上市,用于治疗18岁以下携带ABCD1基因突变的早期脑性肾上腺脑白质营养不良患者(CALD)。如果获批,eli-cel将成为首款FDA批准用于这类罕见病的基因疗法。在一项Ⅱ/Ⅲ期临床Starbeam中,eli-cel使90%的患者达到第24个月无MFD的生存终点,并且大多数患者的神经功能得以维持。
3.阿斯利康长效新冠鸡尾酒III期临床积极。阿斯利康长效抗体鸡尾酒疗法Evusheld(tixagevimab与cilgavimab)治疗轻中度COVID-19门诊患者的III期临床TACKLE达主要终点。与安慰剂相比,Evusheld(600mg)可将疾病进展为重症或死亡的相对风险显著降低50%(95% CI 15, 71;p=0.010 ) ;在出现症状3天内治疗的患者中,Evusheld将该风险降低88%(95% CI 9, 98)。Evusheld总体耐受性良好,两组不良事件 (AE) 发生率分别为36%和29%。
4.登革热候选疫苗长期预防效果积极。武田开发的基于减毒登革热病毒(血清型2)生成的四价疫苗TAK-003,在关键Ⅲ期临床中获积极结果。疫苗接种后54个月随访期间,TAK-003预防因登革热住院的效力达到84%,预防出现症状的登革热的效力为61%。此外,TAK-003耐受性总体良好,未发现重要安全风险,未发现疾病增强的证据。
5.杨森FGFR抑制剂实体瘤临床积极。强生旗下杨森在ASCO2022年会上公布FGFR激酶抑制剂Balversa(erdafitinib)用于治疗FGFR突变、晚期实体瘤的关键Ⅱ期临床RAGNAR中期分析结果。IRC评估的总体客观缓解率为29.2%(95% CI 22.7-36.5),疾病控制率为72.5%(95% CI 65.3-78.9)。中位缓解持续时间为7.1个月(95% CI 5.5-9.3)。研究中Balversa的安全性与该药在转移性尿路上皮癌(mUC)研究相一致。
6.DLB基因编辑疗法临床前研究积极。Seelos公司拟用于针对路易体痴呆症(DLB)的新型表观遗传学基因编辑疗法SLS-004,在临床前研究中获积极结果。SLS-004旨在通过CRISPR-dCas9引导的DNA甲基转移酶3A(DNMT3A),在SNCA基因内含子1的特定位置提高DNA甲基化。从而精准地降低SNCA的表达。在DLB体外模型中,与对照组相比,SLS-004能够将SNCA的mRNA水平降低19%;使α突触核蛋白水平降低40%。
医药热点
1.互联网诊疗监管细则发布。国家卫健委等部门联合印发《互联网诊疗监管细则(试行)》,进一步规范互联网诊疗活动,加强互联网诊疗监管体系建设,防范化解互联网诊疗安全风险。在处方开具及处方药方面,《细则》要求处方应由接诊医师本人开具,严禁使用人工智能等自动生成处方。处方药应当凭医师处方销售、调剂和使用。严禁在处方开具前,向患者提供药品。严禁以商业目的进行统方。
2.2008年-2021年:美国新药上市价格上涨近90倍。哈佛医学院教授在国际顶尖医学期刊《美国医学会期刊》上发表“Trends in Prescription Drug Launch Prices, 2008-2021”文章。分析发现,从2008年到2021年,新药上市价格年增长率为20.4%,根据药物特点调整后为13%,净价年增长率为10.7%。中位价格从2008年的2115美元/元增加到2021年的180007美元/年。价格最高的药物是罕见病用药和肿瘤药,二者中位价格分别为168441美元/年、155091美元/年。
3.4家中国药企入榜全球制药50强。6月10日,美国《制药经理人》杂志(PharmExec)公布2022年全球制药企业TOP50榜单。该榜单主要依据各家药企的2021财年处方药销售收入进行排名。前十名分别是:辉瑞、艾伯维、诺华、强生、罗氏、BMS、默沙东、赛诺菲、阿斯利康、GSK。此次有4家中国企业上榜,分别为恒瑞医药(第32名)、中国生物制药(第40名)、上海医药(第41名)、石药集团(第43名)。
评审动态
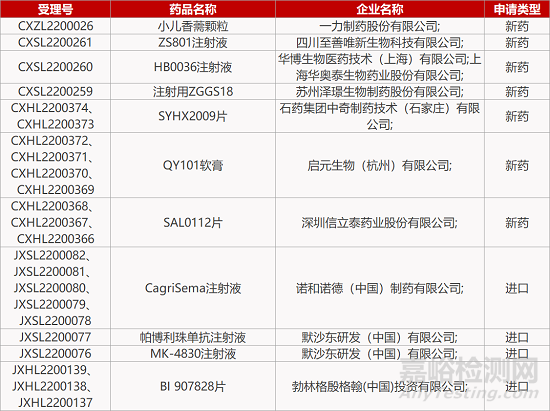
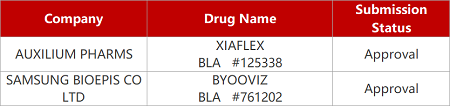

来源:药研发