导读
2022年,国家药监局(NMPA)共批准了49款新药,其中进口新药30款,国产新药19款。从类型上看,包括27款化药、13款生物制品、5款疫苗以及4款中药。
据相关媒体统计,2019年国家药监局共批准了51款新药,2020年批准了48款新药,2021年创纪录地批准了83款新药。就数量而言,2022年似乎又回到了常态。
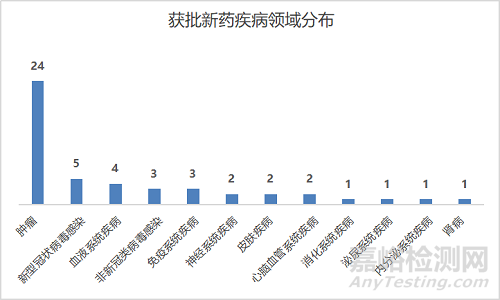
从疾病领域看,2022年NMPA批准的新药中,抗肿瘤(实体瘤+血液瘤)药物独占鳌头,占比49%;治疗新冠药物(口服药+疫苗)位居第二,占比10.2%;其次是血液疾病新药,占比8.2%、非新冠类病毒感染新药占比6.1%、免疫系统疾病新药占比6.1%等。
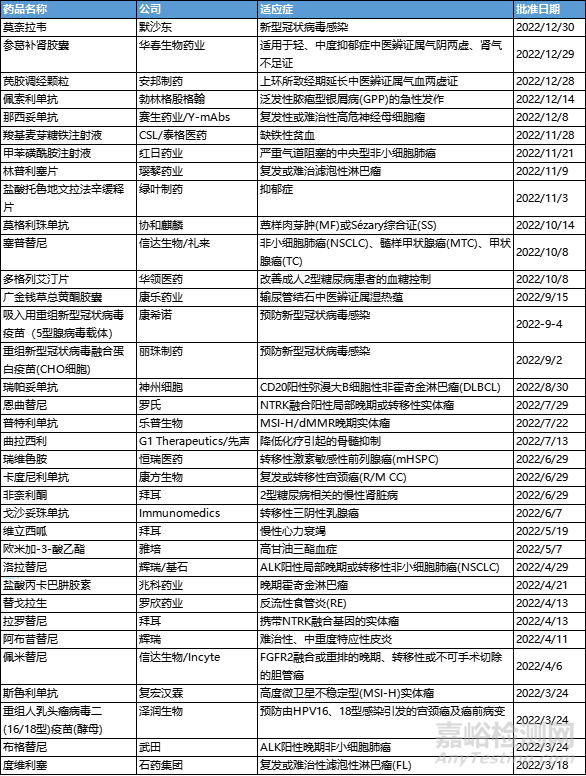
从审评角度看,通过优先审评审批/应急审评审批方式获批上市的新药有24款,占比49%,化药、生物药、中药均有涉及。
通过优先审评审批/应急审评审批方式获批的新药
总体而言,2022年NMPA批准的新药中有不少亮点,在具体产品类别上也带来多款“首个”。这些新药的上市,为多种疾病提供了全新的疗法和更多的治疗选择。
本文将节选部分2022年获NMPA批准上市的新药进行回顾总结,供大家参考。
国产创新药表现亮眼
我国创新药在2022年迎来了新的突破,多款全新机制新药获批上市。这不仅标志着本土药企迎来了研发的收获期,也代表着中国创新药发展体系进一步靠近国际先进水平。
去年6月29日,国家药监局附条件批准康方生物自主研发的PD-1/CTLA-4双特异性抗体药物开坦尼(卡度尼利单抗注射液)上市,用于治疗复发或转移性宫颈癌。这是国内获批上市的首款双抗药物,也是首款获批用于晚期宫颈癌的免疫治疗药物,同时还是全球获批的首款PD-1/CTLA-4双抗,填补了国产双特异性抗体药物研发的市场空白,亦或标志着中国创新药发展体系进一步靠近国际先进水平。
根据已披露的数据现实,作为一种基于PD-1免疫检查点的全新双特异性抗体新药,卡度尼利单抗既可以充分发挥PD-1和CTLA-4两个免疫检查点的协同抗肿瘤作用,同时副作用较两个靶点的单抗联合治疗明显降低,优异的抗肿瘤疗效和安全性将为全球广大肿瘤患者带来切实的临床获益提升。
去年10月,华领医药first in class降糖药多格列艾汀获批上市,用于改善成人2型糖尿病患者的血糖控制。这是全球范围内首个获批上市的葡萄糖激酶启动剂(GKA)药物,是过去近十年来糖尿病领域首个全新机制的原创新药,也是首次在中国推出2型糖尿病全球首创新药。
新冠口服药应急批准上市
伴随着疫情的不断变化,新冠口服药似乎成为了新的曙光。2022年,药监局不仅批准了首个国产新冠口服药——阿兹夫定,还应急附条件批准了两款进口新冠口服新药。
去年2月,药监局按照药品特别审批程序,进行应急审评审批,附条件批准辉瑞Paxlovid(奈玛特韦片/利托那韦片组合包装)进口注册,用于治疗成人伴有进展为重症高风险因素的轻至中度新型冠状病毒肺炎(COVID-19)患者。
Paxlovid是3CL蛋白酶抑制剂nirmatrelvir与低剂量利托那韦(Ritonavir)的复方制剂,由300mg(两片150mg片剂)的nirmatrelvir和一片100mg的利托那韦片进行组合给药供新冠患者口服,每日给药2次,持续5天。利托那韦有助于减缓nirmatrelvir的代谢或分解,使其在体内有效浓度维持较长时间,持久对抗病毒。
根据已披露的临床试验数据现实,Paxlovid一项治疗非住院、具有发展成重症疾病的高风险成人COVID-19感染患者的随机、双盲、II/III期EPIC-HR研究的期中分析结果。数据显示,在症状出现三天内接受治疗的患者中,与安慰剂相比,Paxlovid可使COVID-19相关的住院或因任何原因死亡的风险降低89%(主要终点)。症状出现五天内接受治疗的患者中,与COVID-19相关的住院或死亡也有类似的减少。
去年12月,药监局按照药品特别审批程序进行应急审评审批,附条件批准默沙东公司新冠病毒治疗药物莫诺拉韦胶囊进口注册,用于治疗成人伴有进展为重症高风险因素的轻至中度COVID-19患者。
在作用机制上,与辉瑞的Paxlovid不同的是,Molnupiravir是一种RNA聚合酶(RdRp)抑制剂,通过阻断新冠病毒RNA依赖的RNA聚合酶的合成,达到抑制或清除病毒的作用。而Paxlovid属于3CL蛋白酶抑制剂,其通过阻断新冠病毒3CL蛋白酶的活性,从而破坏病毒RNA的复制过程。
在基于全部随机入组患者(n=1433)的分析中,Molnupiravir降低了住院或死亡风险:对照安慰剂组中9.7%(68/699)的患者住院或死亡,服用Molnupiravir的患者中有6.8%(48/709)的患者住院,绝对危险度下降3.0%(95%置信区间[CI]: 0.1, 5.9)。安慰剂组有9例死亡报告,Molnupiravir有1例死亡报告。
去年9月,默沙东/国药集团联合宣布双方签署合作框架协议,默沙东将其和Ridgeback公司将Molnupiravir的经销权和独家进口权授予国药集团,同时双方将评估技术转让的可行性,以便该药物在中国境内生产、供应和商业化。
中药创新药研发热情高涨
近些年,在诸多利好政策及审评持续优化的驱动下,中药创新药获批品种数、申报上市品种数及申报临床品种数逐年上涨,中药创新药研发热情高涨。2022年,药监局批准了淫羊藿素软胶囊、广金钱草总黄酮胶囊、参葛补肾胶囊、芪胶调经颗粒4款1类中药创新药上市。
去年1月,NMPA批准了北京珅诺基1.2类中药创新药淫羊藿素软胶囊的上市申请,用于治疗既往未接受过全身系统性治疗的不可切除的肝细胞癌。该药物的主要成分是从淫羊藿中提取、分离、纯化得到的活性药物单体。
根据相关报道显示,全国28家研究中心共同参与完成的多中心、随机、双盲、双模拟Ⅲ期研究中,淫羊藿素软胶囊用于不可切除的晚期肝细胞癌一线治疗,在预后更差的富集人群中相较于华蟾素对照组显示出持续显著生存获益和更优的安全性及生活质量。在最新更新的《CSCO肝癌诊疗指南(2022版)》正式将淫羊藿素软胶囊纳入晚期肝癌一线治疗推荐药物目录(Ⅰ级专家推荐)。国家卫健委发布的《原发性肝癌诊疗指南(2022版)》也将淫羊藿素软胶囊作为推荐方案。
去年9月,NMPA批准了人福医药1.2类中药创新药广金钱草总黄酮胶囊的上市申请,适应症为清除湿热、利尿排石,用于湿热蕴结所致的淋沥涩痛,输尿管结石和上述证候者。该药的主要成份是从广金钱草中提取得到的总黄酮类成份。
去年12月,NMPA批准了安邦制药中药新复方制剂芪胶调经颗粒上市。该药品由黄芪、阿胶、党参、白芍等9味药组方,具有益气补血、止血调经功效,用于上环所致经期延长中医辨证属气血两虚证。
去年12月,NMPA批准了新疆华春生物药业1.1类中药创新药参葛补肾胶囊的上市申请。该药品开展了随机、双盲、安慰剂平行对照的多中心临床试验,临床试验研究结果显示,主要疗效指标HAMD -17评分与基线的差值,试验组疗效与氟西汀(Fluoxetine)相当,优于安慰剂组。
该药品益气,养阴,补肾,适用于轻、中度抑郁症中医辨证属气阴两虚、肾气不足证。该药品的上市为抑郁症患者提供了又一种治疗选择。
罕见病疗法层出不穷
去年1月,国家药监局药审中心发布了《罕见疾病药物临床研发技术指导原则》,这也是国家层面为推动更多药物研发、生产机构关注罕见病群体的需求,研发罕见病治疗药物做出的贡献。2022年药监局批准的新药中,罕见病也是获批新药较多的治疗领域。
去年1月,安进/日本协和麒麟(Kyowa Kirin)研发的第二代TPO受体激动剂注射用罗普司亭获得NMPA批准上市,用于治疗原发慢性免疫性血小板减少症(ITP)。
同月,新基(BMS)研发的红细胞成熟剂注射用罗特西普获得NMPA批准上市,用于治疗β地中海贫血患者。罗特西普是中国首个且唯一获批的红细胞成熟剂,也是十余年来中国首个获批治疗β-地中海贫血的创新药物。
去年3月,苏庇医药(Sobi)研发的干扰素γ(IFNγ)靶向疗法依马利尤单抗获得NMPA批准上市,用于特定的原发性噬血细胞性淋巴组织细胞增多症(HLH)成人和儿童患者的治疗。
依马利尤单抗(emapalumab)最初由Novimmune SA公司开发,Swedish Orphan Biovitrum AB(苏庇医药)于2018年通过独家许可协议获得了依马利尤单抗的全球权益。这是一款与干扰素γ(IFNγ)结合的单克隆抗体,能够中和IFNγ的作用。IFNγ是诱导细胞凋亡的关键细胞因子,IFNγ的大规模过度表达被认为是导致免疫系统过分激活的主要原因,这最终会导致器官衰竭。
同日,豪森制药引进的抗CD19单抗伊奈利珠单抗获批用于治疗抗水通道蛋白4(AQP4)抗体阳性的视神经脊髓炎谱系疾病(NMOSD)成人患者。伊奈利珠单抗是翰森制药首款上市的生物药,也是国内上市的首款CD19单抗。
去年12月,勃林格殷格翰罕见皮肤病靶向生物制剂佩索利单抗(商品名:圣利卓/Spevigo)获得NMPA批准上市,用于治疗成人泛发性脓疱型银屑病(GPP)发作。佩索利单抗是一款可阻断白介素-36受体(IL-36R)激活的单克隆抗体,可抑制IL-36的信号传导,也是中国首个获批专门用于治疗成人GPP发作的治疗药物。
佩索利单抗注射液的获批是基于其全球关键性Effisayil 1 II期临床研究。该研究是全球首项针对GPP发作患者进行的国际多中心、双盲、随机对照研究,覆盖了全球12个国家/地区,包括中国。研究表明:54.3%的患者经佩索利单抗注射液治疗1周便达到皮肤无可见脓疱;42.9%的患者经佩索利单抗注射液治疗1周可达到皮肤症状清除或几乎清除。同时在整个研究中,佩索利单抗注射液的安全性数据是可接受的,患者常见的不良事件包括发热和轻度至中度感染。
附表:2022年NMPA批准的新药