您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2023-02-23 08:13
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
菲鹏中美双报CD47单抗获批临床。菲鹏集团旗下菲鹏制药自研CD47单抗FP002获FDA临床许可,拟评估用于晚期恶性肿瘤的安全性和有效性。该抗体在保持与肿瘤细胞表面CD47强结合的前提下,基本不结合人红细胞表面的CD47,不引起血液凝集,在药物安全性实验评价中显示出良好的安全性,并在多种临床前肿瘤模型中展现出优于同类产品的药效。该公司目前同步提交中国的临床试验申请。
国内药讯
1.君实PD-1单抗出海英国报产。君实生物宣布特瑞普利单抗的上市许可申请获英国药品和保健品管理局(MHRA)受理,联合顺铂和吉西他滨用于一线治疗局部复发或转移性鼻咽癌、以及联合紫杉醇和顺铂一线治疗不可切除局部晚期/复发或转移性食管鳞癌。特瑞普利单抗是中国首个获批的国产PD-1抑制剂,目前在中国已获批6项适应症。
2.罗欣引进抑酸新药新适应症报产。罗欣药业从HK inno.N Corporation公司引进的钾离子竞争性酸阻滞剂(P-CAB)替戈拉生片(商品名:泰欣赞)的新适应症上市申请获NMPA受理,拟用于治疗十二指肠溃疡。替戈拉生通过竞争性地阻断H+/K+-ATP酶上的K+结合位点而起到抑制胃酸分泌的作用。该新药已于2022年4月获国家药监局批准上市,用于治疗反流性食管炎。
3.茂行B7-H3靶向CAR-T获孤儿药资格。茂行生物自研靶向B7-H3的同种异体通用型CAR-T产品MT027获FDA授予孤儿药资格,用于治疗复发性高级别胶质瘤。除脑胶质瘤外,B7-H3在肾癌、胰腺癌、卵巢癌、乳腺癌、结肠癌等多种肿瘤组织中均呈现高表达。临床前研究结果显示,MT027已在上述肿瘤细胞及动物模型中观察到积极的抗肿瘤活性。
4.上海医药微生态活菌制剂获批临床。上海医药全资子公司上药信谊申报的WST01制剂临床试验申请获FDA批准,即将开展I期临床试验评估用于体重管理的安全性和有效性。WST01由上药信谊和上海市内分泌代谢研究所合作研发,是一种口服微生态活菌制剂。目前,全球尚无与该项目同类的活体生物药上市。
5.华东医药引进创新双抗报IND。华东医药全资子公司中美华东从Provention Bio公司引进的CD32B/CD79B双抗PRV-3279的临床试验申请获CDE受理。PRV-3279可同时结合CD32B和CD79B受体,触发对B细胞功能和自身抗体产生的抑制,从而在不引起B细胞耗竭的情况下调节B细胞。华东医药拥有PRV-3279治疗系统性红斑狼疮、预防或降低基因治疗的免疫原性这两个临床适应症在大中华区的开发及商业化权益。
6.恒瑞源正宫颈癌TCR-T报IND。恒瑞源正(上海)自主研发的1类生物制品“HRYZ-T101注射液”临床试验申请获CDE受理(受理号:CXSL2300144)。HRYZ-T101是一款拟开发用于治疗宫颈癌的TCR-T细胞治疗产品,其靶点尚未公布。这是恒瑞源正第二款推进到临床阶段的产品,其首款产品“多抗原自体免疫细胞注射液”(MASCT-Ⅰ)此前已获批开展用于恶性实体瘤治疗的临床试验。
国际药讯
1.首款血友病B基因疗法获批欧盟上市。欧盟委员会批准CSL Behring公司基因疗法Hemgenix(etranacogene dezaparvovec)有条件上市许可,用于治疗中重度血友病B成人患者。在临床试验中,该疗法能显著提升患者体内的凝血因子IX水平,并减少预防性治疗;一次性基因疗法治疗第18个月时患者的年出血率(ABR)降低64%(p=0.0002)。2022年11月,Hemgenix已获FDA批准上市,是首款获批用于这类患者的基因疗法。
2.罗氟司特泡沫制剂报脂溢性皮炎NDA。Arcutis公司PDE4抑制剂罗氟司特外用泡沫配方ARQ-154向FDA提交新药申请(NDA),用于治疗成人和青少年中重度脂溢性皮炎。在III期STRATUM研究中,与安慰剂相比,ARQ-154组达到IGA评分为0或1且改善2%的患者比例显著提高(79.5%vs58.0%,P<0.0001)。2022年7月,Arcutis开发的罗氟司特(0.3%)乳膏(ZORYVE)已获FDA批准上市,适应症为斑块状银屑病。
3.再生元C5单抗获FDA优先审评。再生元靶向补体因子C5的IgG4单抗Pozelimab的生物制品许可申请(BLA)获FDA授予优先审评资格,拟用于治疗CHAPLE综合征。PDUFA日期为2023年8月20日。在一项II/III期临床试验(NCT04209634)中,24周治疗结果显示,100%患者的血清白蛋白快速且持续恢复正常,且临床症状改善或无恶化。目前该疾病尚无相关疗法获批上市。
4.辉瑞双价RSV疫苗获FDA优先审评。辉瑞重组RSV融合前F蛋白双价疫苗RSVpreF(PF-06928316)的生物制品许可申请(BLA)获FDA受理,拟通过怀孕妇女产生主动免疫,进而预防婴幼儿自出生起至六个月出现RSV引起的下呼吸道疾病。FDA同时授予其优先审评资格,PDUFA日期为2023年8月。在Ⅲ期临床MATISSE中,疫苗避免婴孩出生后90天内感染严重性MA-LRTI的保护力达81.8%(CI:40.6-96.3%),避免婴孩在出生后6个月的追踪期间感染严重性MA-LRTI的保护力达69.4%(CI:44.3-84.1%)。
5.吉利德Trop-2 ADC治疗mUC的Ⅱ期临床积极。吉利德靶向Trop-2的抗体偶联药物Trodelvy(sacituzumab govitecan-hziy)治疗转移性尿路上皮癌(mUC)的Ⅱ期临床(TROPHY-U-01)结果积极。在含铂化疗和检查点抑制剂(CPI)治疗进展的患者中,Trodelvy单药的总缓解率(ORR)为28%,中位总生存期(OS)为10.9个月。在含铂化疗后进展的患者中,Trodelvy联用PD-1抑制剂帕博利珠单抗的ORR为41%,中位OS为12.8个月。云顶新耀拥有该新药在大中华区的开发权益。
6.默沙东新冠口服药最新III期临床不理想。默沙东新冠口服药莫诺拉韦(molnupiravir)用于新冠暴露后预防的III期MOVe-AHEAD研究未能达到主要终点。该项研究评估莫诺拉韦与安慰剂相比在家庭内部预防COVID-19传播的效果。结果显示,与安慰剂相比,莫诺拉韦使受试者感染COVID-19(基线后SARS-CoV-2检测呈阳性并有症状和体征)的风险降低23.6%,但无统计学意义;药物的安全性与既往试验一致。莫诺拉韦是全球首款获批的口服抗新冠药。
医药热点
1.中国研究型医院学会高血压专委会成立。2月18日,中国研究型医院学会高血压专业委员会成立大会在北京召开。会议选举产生高血压专业委员会第一届委员、常务委员、副主任委员及主任委员,其中北京大学第一医院霍勇教授当选为主任委员,四川大学华西临床医学院陈晓平教授、复旦大学附属中山医院崔兆强教授、广东省人民医院冯颖青教授、阜外华中心血管病医院高传玉教授、华中科技大学同济医学院附属协和医院黄恺教授等共14位专家当选为副主任委员,马为教授同时兼任高血压专委会秘书长。
2.甲流引发多地学校学生发热停课。据多家媒体报道,北京、上海、天津、浙江等地近日部分学校都出现因学生发热而停课的情况,发热原因为甲型流感,引发公众关注和担忧。南方科技大学公共卫生及应急管理学院流行病学教授魏晟在接受采访时表示,因麻疹、水痘、流感、手足口病等传染病导致的停课是很常见的疫情应对方式,学校为避免校园内疫情的进一步扩散会采取小范围停课的方式来应对,大众不必因为“停课”二字而过度恐慌。
评审动态
1. CDE新药受理情况(02月22日)
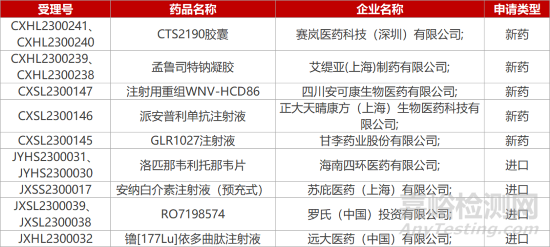
2. FDA新药获批情况(北美02月21日)
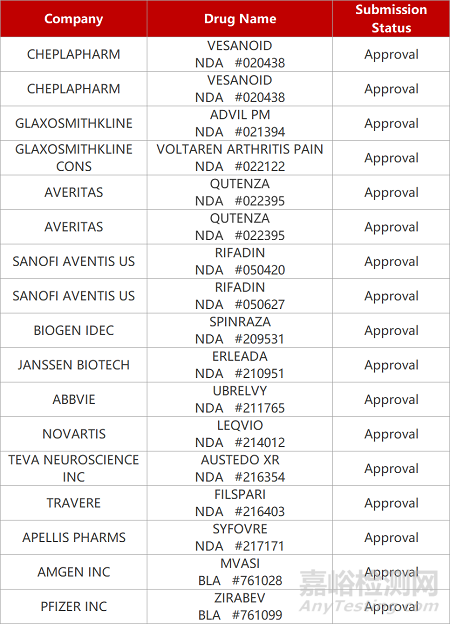

来源:药研发