今日头条
德琪ERK1/2抑制剂上美国Ⅰ期临床。德琪医药在美国开展的小分子ERK1/2抑制剂ATG-017联合PD-1疗法纳武利尤单抗治疗晚期实体瘤的I期ERASER研究完成首例患者给药。该项试验拟评估ATG-017联合用药的安全性/耐受性、药代动力学和初步疗效。该项研究的单药疗法部分目前正在澳大利亚顺利推进。临床前研究数据显示,ERK1/2抑制剂联合免疫检查点抑制剂(ICI)具有协同抗肿瘤作用。
国内药讯
1.FDA完成替雷利珠单抗生产现场检查。百济神州日前宣布,FDA已完成对其PD-1抑制剂替雷利珠单抗(tislelizumab,百泽安)的生产检查,预期替雷利珠单抗将在今年下半年在美国获批,用于二线治疗不可切除或转移性食管鳞状细胞癌(ESCC)。在全球III期研究RATIONALE 302中,替雷利珠单抗与化疗相比平均延长患者2.3 个月的寿命。如果获批,替雷利珠单抗将成为首个进入美国市场的国产检查点抑制剂。
2.恒瑞Aβ单抗早期临床积极。恒瑞医药在2023AAIC会议上公布其Aβ单抗(IgG1 亚型)SHR-1707在中国与澳大利亚健康人中完成的单次剂量递增的I期研究(NCT04973189、NCT04745104)积极结果。数据显示,在2-60 mg/kg的剂量范围内,SHR-1707在年轻人中的暴露量以略大于剂量比例的方式增加;血浆中Aβ 42水平及较基线变化呈现剂量依赖性;药物耐受性良好。PK、PD数据支持进一步临床研发。
3.杭州启函多位点基因编辑疗法获批临床。启函生物1类生物制品QN-019a细胞注射液获国家药监局临床试验默示许可。启函生物运用多位点基因编辑技术修改人源多能诱导干细胞(iPSC),并将其分化成为靶向CD19阳性B细胞肿瘤的自然杀伤细胞(NK)产品QN-019a,拟开发用于治疗CD19阳性的复发难治性侵袭性B细胞非霍奇金淋巴瘤(B-NHL)。
4.天泽云泰罕见病基因疗法获批临床。天泽云泰自主研发的1类生物药VGM-R02b获国家药监局临床试验默示许可,拟开展用于戊二酸血症I型(GA-I)治疗的临床研究。GA-I是一种罕见的常染色体隐性遗传性神经代谢性疾病,已被列入我国《第一批罕见病目录》。VGM-R02b也是该公司第三个获批进入临床的基因治疗产品,该产品已被FDA授予用于治疗GA-I的罕见儿科疾病认定(RPDD)。
5.科兴二价手足口疫苗获批临床。科兴生物开发的1.4类生物制品二价肠道病毒灭活疫苗获国家药监局临床试验默示许可,拟开发用于接种后刺激机体产生抗EV71与CA16的免疫力,预防由EV71、CA16感染所致手足口病。EV71和CA16是20余种手足口病致病病毒中最为常见的两种病毒。此前,该公司研发的益尔来福(肠道病毒71型灭活疫苗(Vero细胞))已获批上市,用于预防由EV71引起的手足口病。
国际药讯
1.强生c-Met/EGFR双抗肺癌III期临床积极。强生旗下杨森EGFR/MET双抗amivantamab-vmjw(Rybrevant)一线治疗EGFR外显子20插入突变的晚期或转移性非小细胞肺癌(NSCLC)的III期PAPILLON研究结果达到主要终点。与单纯化疗相比,Rybrevant联合化疗显著改善患者的无进展生存期(PFS),药物的安全性与已知研究一致。2021年5月,FDA已加速批准该新药上市,用于铂类化疗后进展的EGFR外显子20插入突变的晚期或转移性NSCLC患者。
2.KOR拮抗剂抑郁症Ⅱ期临床积极。Neumora公司宣布将启动一项评估新型κ阿片受体(KOR)拮抗剂navacaprant(NMRA-140)单药治疗重度抑郁症的Ⅲ期临床。在Ⅱ期临床中,在第4周和第8周时,navacaprant治疗较安慰剂显著改善中重度MDD患者的17项汉密尔顿抑郁量表(HAMD-17)评分(-3.0,p=0.015;-2.8,p=0.037)和快感缺乏量表(SHAPS)评分(-2.4,p=0.071;-4.8,p=0.001);两组治疗伴发不良反应发生率分别为35.3%和44.1%。
3.助听器可降低认知衰退风险近50%。科学家在AAIC2023会议上公布一项评估助听器用于减少老年人长期认知功能下降的临床试验积极结果。研究结果显示,在具有轻中度听力损失,而且认知能力下降风险更高的老年人亚群中,使用助听器3年能够将认知衰退风险降低接近一半(减缓48%)。详细结果同时发表在医学期刊《柳叶刀》上。
4.诺华10亿美元收购siRNA药物公司。诺华与神经科学领域siRNA药物公司DTx Pharma达成收购协议,获得后者拟开发用于治疗1A型Charcot-Marie-Tooth病(CMT1A)的先导候选药物DTx-1252,以及另外两个用于其他神经科学适应症的临床前项目。DTx-1252旨在通过靶向PMP22蛋白来解决CMT1A的根本原因,以恢复髓鞘的正常功能。根据协议,诺华将支付5亿美元的预付款,最高5亿美元的里程碑潜在付款。
5.AβO抗体临床前数据积极。ProMIS公司β-淀粉样蛋白寡聚体(AβO)抗体PMN310在AAIC会议上公布用于治疗阿尔兹海默病(AD)的临床前积极数据。表面等离子共振(SPR)结果显示,与其它Aβ抗体相比,PMN310能够选择性地结合AD患者脑提取物中的毒性AβO;除Acumen公司的Aβ抗体ACU193外,PMN310对Aβ单体的结合能力也要小于包括渤健/卫材的lecanemab和礼来的donanemab等在内的其它Aβ抗体。此外,PMN310也显示出完整保护记忆功能的潜力。
6.辉瑞联手Flagship开发10个创新候选药。辉瑞与Flagship Pioneering公司将利用后者旗下40多家药物研发公司和多个生物技术平台,针对辉瑞核心战略兴趣领域,合作开发10个创新候选药物。根据协议,Flagship和辉瑞将各自投入5000万美元款项;辉瑞将资助并有选择权收购每个选定的开发项目;Flagship及其生物平台公司将有资格获得每个产品高达7亿美元的里程碑和特许权使用款项。
医药热点
1.美首例机器人肝移植手术成功。据美国圣路易斯华盛顿大学医学院官网报道,该院一个外科团队今年5月完成美国首例机器人肝脏移植手术。术后一个月,患者不仅行走自如,还恢复一定的运动能力。此次成功意味着微创机器人手术的优势扩展到肝脏移植领域,可实现更小切口、更少疼痛和更快恢复,并且具备最有挑战性的腹部手术之一所需的精确度。
2.全球首个胰腺保护指南发布。7月16日,由中国抗癌协会主办的“中国肿瘤整合诊治技术指南(CACA)-胰腺保护”精读巡讲活动在浙江杭州隆重举办。《CACA技术指南-胰腺保护》是全球首个全面、系统阐述如何保护来自多种肿瘤对胰腺损伤的指南。本指南的发布将为临床及时发现肿瘤胰腺损伤并开展规范化诊治提供开创性的重要指导。
3.国家高原病医学中心设置标准发布。国家卫健委发布《国家高原病医学中心设置标准》。《设置标准》强调,国家高原病医学中心应位于或毗邻高原,具备丰富的高原病诊治经验,综合诊疗能力突出,具有高水平的高原病学科带头人和专科人才梯队。同时,要求已建立省级以上紧急医学救援队伍,近5年,在超高海拔地区(海拔≥3500米)开展不少于3次高原卫生应急救援演练。
评审动态
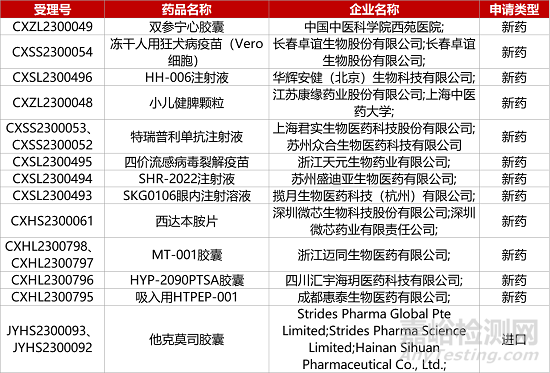
1. CDE新药受理情况(07月19日)
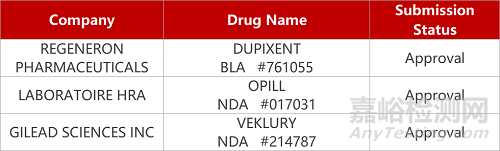
2. FDA新药获批情况(北美07月14日)