今日头条
恒瑞JAK1抑制剂RA适应症报产。恒瑞医药JAK1抑制剂艾玛昔替尼片(SHR0302)新适应症的上市申请获CDE受理,推测申报的适应症为类风湿性关节炎(RA)。SHR0302能针对性阻断JAK/STAT通路,目前已开展了包括类风湿性关节炎、溃疡性结肠炎、特应性皮炎、斑秃、银屑病关节炎等多领域的临床研究。今年6月和8月,艾玛昔替尼片已向CDE递交用于治疗皮炎和活动性强直性脊柱炎(AS)的两项新药申请。
国内药讯
1.百济神州HER2双抗拟纳入优先审评。百济神州HER2双抗注射用泽尼达妥单抗获CDE拟纳入优先审评,用于既往接受过全身治疗的HER2高表达的不可切除局部晚期或转移性胆道癌患者。在国际Ⅱb期HERIZON-BTC-01试验中,该产品在这类患者中经独立中心审查(ICR)确认的客观缓解率(cORR)为41%。中位反应持续时间(DOR)为12.9个月;中位随访时间为12.4个月。治疗相关TRAE发生率为72%,3级TRAEs发生率为18%。
2.精准生物CAR-T疗法拟纳入突破性品种。精准生物1类生物制品pCAR-19B细胞自体回输制剂获CDE拟纳入突破性治疗品种,用于治疗3~21岁患有CD19阳性复发/难治性急性淋巴细胞白血病(B-ALL)的患者。在Ⅰ期注册临床中,所有9例患者均获得完全缓解(CR),总体缓解率达100%;且药物总体安全性良好。pCAR-19B还在CD19阳性弥漫大B细胞淋巴瘤、滤泡性淋巴瘤和套细胞淋巴瘤患者中开展临床研究。
3.强生口服抗凝药中国启动Ⅲ期临床。强生与百时美施贵宝开发的口服XIa因子抑制剂milvexian在中国登记启动两项国际Ⅲ期临床,拟评估用于治疗急性冠脉综合征(ACS),以及评估用于预防发生急性缺血性卒中或高危短暂性脑缺血性发作(TIA)的成人患者发生缺血性卒中的有效性与安全性。今年5月,该新药已获得FDA快速通道资格,用于缺血性中风、ACS以及房颤这3项适应症。
4.晟斯血友病长效疗法获批临床。晟斯生物超长效重组八因子产品FRSW117获FDA临床许可,将在美国开展用于治疗血友病A的临床研究。FRSW117采用了Fc融合与聚乙二醇(PEG)两种长效化技术开发,旨在解决“一周一次”的给药频率,具有“功能性治愈”的潜力。血友病A是一种由凝血因子八基因突变引起的出血性疾病。
5.上海医药CD19/22靶向CAR-T获批临床。上海医药自主研发、“靶向CD19和CD22的嵌合抗原受体自体T细胞注射液”获国家药监局临床试验默示许可,拟开发用于治疗儿童和青少年CD19+/CD22+复发或难治性B系急性淋巴细胞白血病。该产品在互不影响的情况下分别结合B淋巴细胞表面表达CD19或CD22;同时针对CD19和CD22靶点进行组合治疗,可以覆盖原发与复发的B细胞恶性血液肿瘤患者的各种细胞亚群。
国际药讯
1.创新P-CAB获批治疗糜烂性食管炎。Phathom公司新型钾离子竞争性酸阻滞剂(P-CAB)Voquezna(vonoprazan,伏诺拉生)片剂(10mg和20mg)获FDA批准上市,用于治疗成人糜烂性食管炎(GERD),维持糜烂性GERD的愈合,并缓解与糜烂性GERD相关的胃灼热。在III期PHALCON-EE研究中,vonoprazan(20mg)的治愈率与兰索拉唑(30mg)相比达到非劣效性(93%vs85%);Vonoprazan(10mg)在6个月内缓解胃灼热效果也不劣于兰索拉唑(15mg)。
2.Incyte公司JAK1抑制剂上白癜风III期临床。Incyte公司选择性JAK1抑制剂Povorcitinib(INCB054707)在ClinicalTrials网站上登记两项III期临床(STOP-V1和STOP-V2),拟评估用于治疗成人非节段性白癜风的有效性与安全性。公布于EADV大会上的IIb期研究52周数据显示,Povorcitinib(45mg和75mg)组患者的的总白癜风面积评分指数(T-VASI)分别改善42.7%和41.3%,面部白癜风面积评分指数(F-VASI)分别改善63.8%和64.4%;最常见的治疗相关不良事件是COVID-19。
3.VMAT2抑制剂治疗亨廷顿病长期疗效积极。Neurocrine公司VMAT2抑制剂Ingrezza(valbenazine)胶囊治疗亨廷顿病(HD)相关舞蹈病的Ⅲ期KINECT-HD2临床最新结果积极。此前,第6周治疗数据显示,Ingrezza治疗组达到CGI-C(临床总体变化印象)和PGI-C(患者总体印象变化)指标改善的患者比例分别达到58.9%和60.9%。50周数据显示,这两个指标进一步改善,分别有76.9%和74.2%比例达到CGI-C和PGI-C的改善。药物的安全性与既往研究一致。
4.ETA受体拮抗剂慢性肾病Ⅱb期临床积极。阿斯利康选择性内皮素a(ETA)受体拮抗剂zibotentan联合达格列净(dapagliflozin)治疗慢性肾病(CKD)的Ⅱb期ZENITH-CKD试验积极结果公布于ASN2023年会以及《柳叶刀》上。与dapagliflozin相比,zibotentan组合患者12周时的尿白蛋白与肌酐比值(UACR)降低33.7%(p<0.001)和 27.0%(p=0.002);联合治疗患者UACR较基线平均降幅分别为52.5%和47.7%。阿斯利康预计年底开展zibotentan组合Ⅲ期临床。
5.BI小分子ASi创新药肾病Ⅱ期研究积极。勃林格殷格翰创新醛固酮合成酶抑制剂(ASi)BI690517联合SGLT2抑制剂恩格列净(empagliflozin)治疗慢性肾病(CKD)的Ⅱ期临床结果积极。14周治疗数据显示,与安慰剂相比,BI690517联合恩格列净治疗使患者的白蛋白尿显著减少,降幅达39.5%;将肾脏疾病相关临床事件的风险降低至少30%;药物安全性良好,未观察到不可预见的安全性问题。
6.司美格鲁肽前三季度大卖146亿美元。11月2日,诺和诺德发布2023Q3财报,前三季度总营收1663.98亿丹麦克朗(约合241.71亿美元),同比增长29%。其中,司美格鲁肽注射液Ozempic(降糖)收入656.53亿丹麦克朗(95.37亿美元,+53%);司美格鲁肽片Rybelsus收入128.40亿丹麦克朗(18.65亿美元,+77%);司美格鲁肽注射液Wegovy(减肥)收入217.29亿丹麦克朗(31.56亿美元,+481%)。三款产品合计收入145.58亿美元。
7.Kymera终止一款IRAK4靶向蛋白降解剂开发。基于战略原因,Kymera公司已决定停止开发IRAK4激酶靶向降解剂KT-413项目。KT-413靶向IRAK4与IMiD底物Ikaros和Aiolos,拟用于治疗携带MYD88基因突变的弥漫性大B细胞淋巴瘤(DLBCL)。KT-413已在I期临床中达到预期降解水平,并且没有引起剂量限制性毒性。据悉,Kymera还拥有另一款IRAK4激酶靶向降解剂KT-474,目前正在与赛诺菲联合开发当中。
医药热点
1.天津市预防医学科学院挂牌成立。10月31日,天津市疾病预防控制科技创新发展研讨会暨天津市预防医学科学院挂牌成立仪式成功举办。天津市预防医学科学院的挂牌成立将加强预防医学应用基础研究、科技创新和人才培养的重要途径,有力推进天津市疾病预防控制中心整体科研水平的提档升级,旨在推动京津冀一体化协同发展。
2.史加海出任南通大学附属医院院长。11月2日,南通大学附属医院召开干部大会,宣布南通大学党委对行政主要领导调整的决定,史加海同志任附属医院党委副书记、院长,施炜同志不再兼任附属医院院长。根据公开信息,史加海,主任医师,教授,擅长肺、食管疾病微创治疗,特别是微创单孔胸腔镜肺部手术;胸部机器人手术;胸腺疾病及部分重症肌无力系统化治疗。
3.罗氏旗下基因泰克CEO离职。11月1日,罗氏集团宣布,旗下基因泰克首席执行官Alexander Hardy已决定离开公司,并于2023年11月1日立即卸任;美国商业组合负责人Ashley Magargee担任临时首席执行官,直到宣布正式继任者为止。同日,Alexander Hardy官宣任职去向,将于12月1日在BioMarin拜玛林制药首席执行官Jean-Jacques Bienaimé卸任后,出任BioMarin拜玛林制药首席执行官。
评审动态
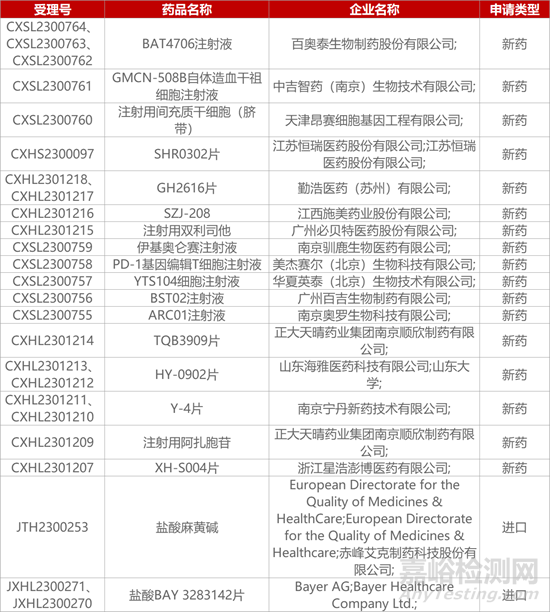
1. CDE新药受理情况(11月04日)
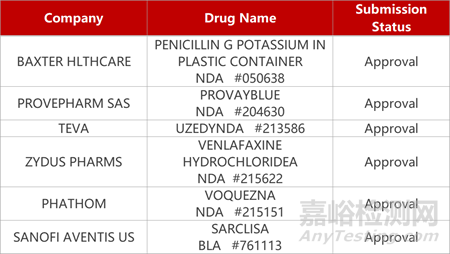
2. FDA新药获批情况(北美11月02日)