您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-01-07 18:47
为防止海水鱼养殖及运输贮藏过程中微生物过度繁殖导致食物腐败变质,常使用四环素和喹诺酮两类药物。相关国家标准规定,鱼类皮和肉中恩诺沙星(以恩诺沙星与环丙沙星含量合计)、四环素、土霉素、金霉素及多西环素的最大残留限量分别为100,200,200,200,100μg·kg−1,氧氟沙星、诺氟沙星及培氟沙星均不得使用。由于部分养殖者对相关药物的非法滥用,养殖海水鱼中这两类抗生素药物的检出率居高不下,由此带来的食品安全问题日益突出,不仅对人体健康产生直/间接危害,而且导致细菌严重耐药进而对生态系统产生毒害。因此,开发可靠、快速、高通量、高精度、易操作的监测海水鱼中这两类药物残留量的分析方法尤为重要。检测关键点主要集中在前处理方法和测定方法的选择上。这两类药物残留的样品前处理方法主要有液液萃取法、固相萃取法及 QuEChERS等。相较传统的液液萃取法及固相萃取法,QuEChERS精密度和准确度更好,分析更快,有机溶剂用量更少,操作更简单等,适用于大批量样品分析。但是QuEChERS无法完全消除基质干扰,对定量结果存在一定影响。因此,本工作优化了QuEChERS前处理条件,选择同位素内标法定量,提出了一种基于Cleanert LipoNo净化管的操作简单、快速、高效、准确、可靠的QuEChERS-超高效液相色谱-串联质谱法,用于测定大批量海水鱼样品中4种四环素类药物及5种喹诺酮类药物的残留量。
1、试验方法
称取均质好的样品于离心管中,加入混合内标工作液,涡旋混匀。加入Na2EDTA溶液,涡旋后加入乙腈,涡旋,超声后离心。取全部上清液,加至Cleanert LipoNo净化管,振摇后静置。取全部上清液,氮吹至干,用初始流动相复溶,过有机滤膜,滤液收集至进样瓶,按照仪器工作条件测定。
2、结果与讨论
2.1 色谱条件的选择
试验比较了分别以水-乙腈、5mmol·L−1乙酸铵溶液-乙腈、0.1%甲酸溶液-乙腈体系作流动相时目标物的峰形及响应情况,根据试验结果,选择0.1%甲酸溶液-乙腈体系作流动相。在优化的色谱条件下,加标空白海水鱼基质溶液的提取离子色谱图见图1。

由图1可知,9种药物及2种内标的色谱峰峰形对称、尖锐,保留时间为 3.72~5.03min,满足定量分析要求。
2.2 前处理条件的选择
2.2.1 提取条件
适用于QuEChERS提取的溶剂主要有甲醇及乙腈,相较甲醇,乙腈可以有效沉淀蛋白,且对糖类和脂肪的溶解程度更低,因此试验选择采用乙腈提取样品中的目标物。考虑到四环素类药物容易与金属离子、蛋白质等发生螯合作用,提取难度较高,试验进一步优化提取溶剂,确定采用0.1mol·L−1Na2EDTA溶液+乙腈提取,该溶剂组合有利于沉淀蛋白,并能将药物从生物组织中释放出来,充分溶解在乙腈中。为确保提取充分,试验比较了分别对加标空白基质(加标量5μg·kg−1)提取1,2,3次时各目标物的回收率,结果见图2。
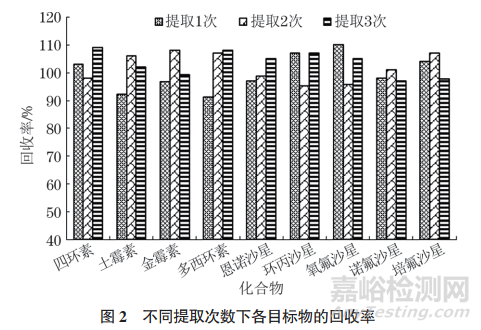
由图2可知,不同提取次数下回收率均在90.0%~110%内。为节省分析时间,试验选择只提取1次。
2.2.2 净化方法
在日常监督抽样检测中发现,液液萃取法对试验人员的操作能力要求较高,且耗费时间过长;固相萃取法需要专门的固相萃取装置,净化过程包括固相萃取柱活化以及样品提取液上样、淋洗、洗脱、收集等步骤,操作繁杂、耗时较长,且容易发生固相萃取柱堵塞等问题。因此,试验选择采用QuEChERS净化样品,并比较了分别采用净化材料Cleanert LipoNo、C18+N-丙基乙二胺(PSA)(质量比 1∶1)、氧化锆吸附脂类等非极性干扰物(用量均为1g)时加标空白基质(加标量5μg·kg−1)中各目标物的基质效应(ME)值(外标法所得ME值绝对值,分别采用空白基质溶液和初始流动相配制混合标准溶液系列并制作标准曲线,以前后二者标准曲线斜率比和 1 的差值的绝对值计算),结果见图3。

由图3可知,Cleanert LipoNo所 得ME值绝对值更小,说明其净化效果更好,这是由于Cleanert LipoNo是一种表面修饰了大量大颗粒长碳链的除脂材料,可针对性地吸附脂肪等非极性干扰物,且操作简单,试验人员只需将提取液转移进填充有Cleanert LipoNo的净化管中,振摇后静置分层,2min即完成全部净化工作,操作简单、快速,无需专门净化设备,且成本较固相萃取法更低。
2.3 基质效应及消除
采用超高效液相色谱-串联质谱法分析动物源性食品时,由于样品基质往往会对定量结果产生严重影响,因此需要对基质效应进行评估。参考文献计算ME值,当ME值绝对值不大于10%时,基质效应可以忽略;当ME值绝对值在 [10%,50%)内时,存在中等基质增强或抑制效应;当ME值绝对值大于50%时,存在强基质增强或抑制效应,对定量结果影响较大。当存在中等或强基质效应时,需要优化检测方法,将ME值绝对值控制在10%以内。目前消除基质效应的方法主要有空白基质匹配标准曲线法和内标法。在实际检测中,样品基质种类多样,不同基质对同一目标物产生的基质效应差异较大,若每种基质都用来制作空白基质匹配标准曲线,则所需空白基质数量庞大,经济及操作上均难以实现。同位素内标法不仅准确度高、操作简单,且无需制作空白基质匹配标准曲线;在同一类型药物中选取1~2种同位素内标直接进行内标法定量分析,既兼顾了经济性又能确保方法的准确度。综合考虑,试验选择采用四环素-d6作为四环素类药物的同位素内标,恩诺沙星-d5作为喹诺酮类药物的同位素内标,并以市场销售量较高的6种空白海水鱼基质(黄花鱼、黄翅鱼、带鱼、海鲈鱼、金线鱼和鲳鱼,其中黄花鱼及黄翅鱼中目标物检出率较高)为待测对象,考察了分别采用内标法与外标法测定时各目标物的ME值,所得结果见图4。
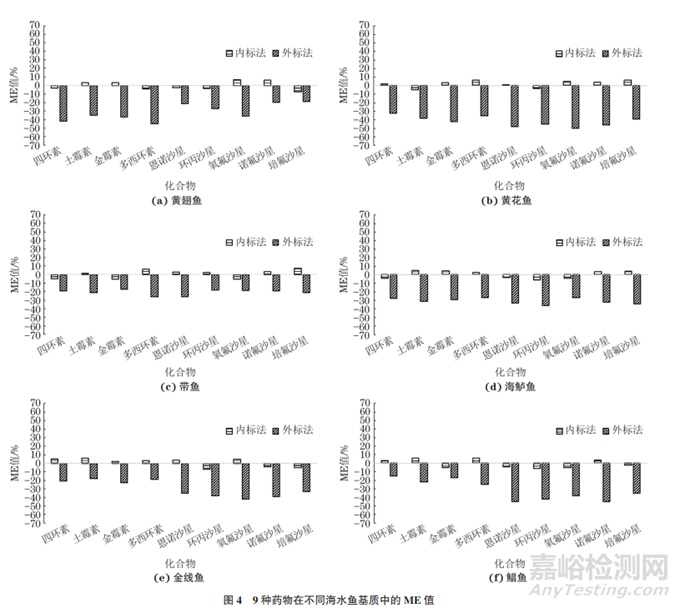
由图4可知:采用外标法定量时,两类药物ME值绝对值在 [10%,50%) 内,均显示为基质抑制效应;采用内标法定量时,两类药物ME值绝对值均小于10%,说明内标法能有效消除基质效应。
2.4 方法学考察
2.4.1 标准曲线、检出限和测定下限
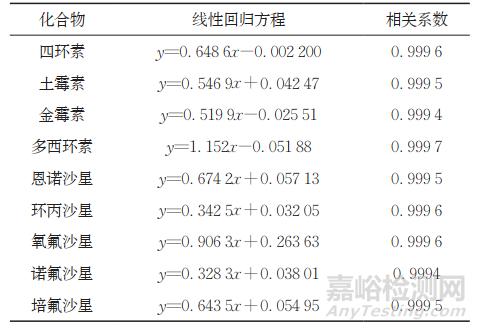
分别取混合标准工作液及混合内标工作液适量,用初始流动相稀释,配制成含内标50μg·L−1,各目标物5.00,10.0,25.0,50.0,75.0,125μg·L−1的混合标准溶液系列,按照仪器工作条件测定。以各目标物质量浓度与内标质量浓度的比值为横坐标,对应的目标物的定量离子色谱峰面积与对应内标子离子色谱峰面积的比值为纵坐标绘制标准曲线,所得各标准曲线的线性范围均为5.00~125μg·L−1,其他线性参数见表1。
表1 线性参数
在空白海水鱼基质中加入标准溶液,制备一系列低浓度加标水平的海水鱼样品(加标量1.00,2.00,5.00,10.00μg·kg−1),按照试验方法测定。以信噪比接近3,10的加标量作检出限和测定下限,检出限和测定下限分别为2.00,5.00μg·kg−1。
2.4.2 精密度和回收试验
选取不合格率较高的空白黄花鱼基质,在1,2,10倍测定下限水平下各进行6次平行加标回收试验,计算回收率和测定值的相对标准偏差(RSD),结果见表2。
表2 精密度和回收试验结果 (n=6)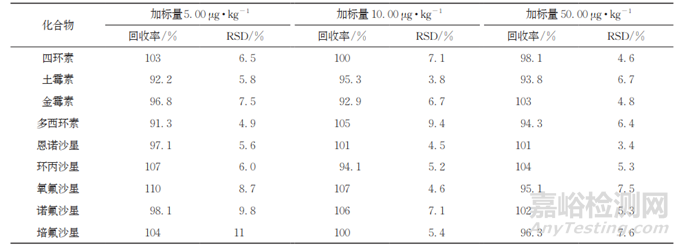
由表2可知,9种药物的回收率为91.3%~110%,测定值的RSD为 3.4%~11%,满足实际检测准确度和精密度要求。
2.5 样品分析
按照试验方法分析2022— 2023年实验室监督抽样中留存的200批海水鱼样品,检出结果与当年实验室监督抽样所用国家标准方法的进行比对。结果显示:四环素类药物均未检出;在41批样品中检出了喹诺酮类药物,其中41批样品检出了恩诺沙星,36批样品同时检出了环丙沙星,6批样品中恩诺沙星和环丙沙星总检出量超过国家标准规定(100μg·kg−1),比对结果如表3所示。
表3 方法对比结果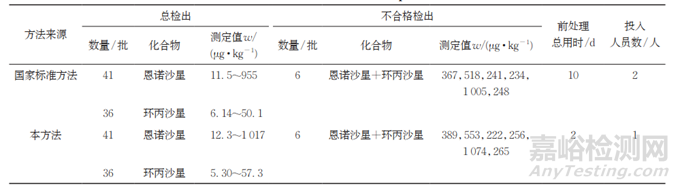
由表3可知,200批海水鱼样品的检出结果与当年监督抽样检验结果基本一致,但是本方法所需前处理时间及投入人员数大大减少,说明本方法操作更为简便、快速,且结果稳定可靠。
3、试验结论
研究人员采用基于Cleanert LipoNo净化管的QuEChERS-超高效液相色谱-串联质谱法测定海水鱼样品中四环素和喹诺酮类药物的含量,大大
缩短了样品前处理和仪器运行时间,同时保证了较高的准确度及精密度,适用于大批量海水鱼样品中抗生素残留的快速、高效、准确测定。后续研究可增加药物种类及样品种类,一次性实现对多基质中多种类药物的快速定量分析,进而为政府大规模开展食用农产品监督抽样及风险监测提供有利技术支持。
作者:蔡振世,许琨琨,卢文斌
单位:泉州市食品药品检验所
来源:《理化检验-化学分册》2024年第10期

来源:理化检验化学分册


