您当前的位置:检测资讯 > 监管召回
嘉峪检测网 2025-03-04 11:28
FDA发布一项关于飞利浦外周产品(Tack)一级召回的事件,如果继续使用此设备,可能会导致严重伤害或死亡。本次召回涉及从使用或销售的地方召回Tack。
涉及产品
Tack Endovascular System (4F,1.5-4.5mm), 150cm
Tack Endovascular System (6F, 3.5 - 6.0mm), 135c
Tack Endovascular System (6F, 4.0 - 8.0mm), 135cm
召回原因
医生使用过程中出现操作困难,包括需要额外干预措施才能取出Tack植入物的案例。所有客户应立即停止使用Tack,飞利浦将永久停止Tack的分销。
使用受影响产品可能导致严重健康风险,包括:
短期风险:血管部分/完全闭塞、动脉内膜撕裂、动脉壁穿孔
长期风险:疼痛、组织坏死、血管再狭窄、需搭桥手术、截肢甚至死亡
目前已有20例伤害报告,尚无死亡病例。
应对措施
立即停止使用Tack。
立即检查库存中是否存有受影响产品
隔离受影响设备以防止使用
不得开封或使用任何已识别的产品
在七天内填写、签署并寄回信函附带的响应表
回顾
Tack由Intact Vascular设计开发,在2019年获得FDA批准上市。Tack适用于治疗膝关节上方或下方球囊血管成形术后的外周动脉夹层。飞利浦于2020年花费2.75亿美金收购Intact Vascular,从而获得首个精准PAD术后动脉壁修复支架Tack。
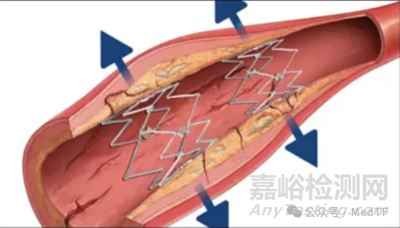

来源:MedTF


