您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-04-22 08:36
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
诺和诺德每周1次长效GLP-1降糖药即将获批。诺和诺德「司美鲁肽注射液」(索马鲁肽注射液)上市申请审评状态变更为「待审批」,即将获批上市,辅助饮食控制和运动以改善2型糖尿病患者的血糖控制。索马鲁肽注射液是诺和诺德研发的一种长效GLP-1受体激动剂,每周只须注射1次即可达到降糖效果。目前全球范围内已批准上市每周注射1次的同类产品有5款,分别是利拉鲁肽、度拉糖肽、索马鲁肽(注射+口服)、艾塞那肽微球。
国内药讯
1.诺诚健华BTK抑制剂最新临床数据积极。诺诚健华新型BTK抑制剂奥布替尼治疗复发/难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(R/R CLL/SLL)的Ⅱ期临床最新数据积极。中位随访时间为25.6个月,研究者评估的ORR达到93.9%,其中CR高达21.3%,部分缓解率为61.3%,伴淋巴细胞增多的部分缓解率为11.3%。达到首次缓解的中位起效时间1.87个月,中位PFS和DOR均未达到。值得一提的是,奥布替尼CR率是其他BTK抑制剂的4-7倍。
2.微芯生物西达本胺肺癌Ⅱ期临床获受理。微芯生物西达本胺的临床试验申请获CDE受理,拟联合PD-L1恩沃利单抗开展治疗经PD-1抑制剂治疗耐药的非小细胞肺癌(NSCLC)Ⅱ期试验。西达本胺是全球首个亚型选择性HDAC抑制剂,已在中国获批治疗外周T细胞淋巴瘤、乳腺癌适应症,目前正在关键性Ⅲ期临床中评估治疗弥漫大B细胞淋巴瘤的潜力。在一项Ⅰb /Ⅱ期临床中,西达本胺针对晚期NSCLC患者客观缓解率达38%,疾病控制率为75%。
3.创胜集团PD-L1 /TGF-β双抗获FDA临床许可。创胜集团创新PD-L1/TGF-β双抗TST005获FDA临床试验许可。TST005由PD-L1抗体和融合在其C端的经工程改造的TGF-β受体II型蛋白组成。在多个同源小鼠肿瘤模型中,TST005可显著增加CD8阳性T细胞向PD-L1表达的肿瘤中的浸润并在高表达TGF-β的同源小鼠肿瘤模型中显示出剂量依赖性的肿瘤生长抑制。该公司计划在获得TST005国内临床批件后,在相同的I期方案下于中美两国同步开发TST005。
4.华东医药携手诺灵生物布局ADC领域。华东医药旗下杭州中美华东与诺灵生物签署战略合作协议。诺灵生物是一家专注于新一代抗体偶联技术的药物研发公司。根据协议,中美华东将联合福广鸿信通过增资形式共同出资3500万元人民币,对诺灵生物进行股权投资;华东医药将在2026年之前享有诺灵生物产品优先受让权。本次合作是继去年华东医药从美国ImmunoGen公司引入ADC产品IMGN853后,在ADC领域又一重要布局。
5.方达医药收购基因组学公司。方达医药宣布收购美国Ocean Ridge Biosciences公司。Ocean Ridge Biosciences是一家成立已超过15年的基因组学服务公司,可为开发新疗法的客户提供包括分析RNA表达、DNA多态性、甲基化、微生物组成和广泛样本的蛋白质生物标记物的完整服务解决方案。此次收购将增强方达医药的基因组学能力,助力该公司为医疗保健和生命科学行业及学术机构提供更加准确可靠、信息内涵更丰富的优质基因组学服务。
国际药讯
1.强生疫苗恢复在欧洲推广。当地时间20日,欧洲药品管理局表示,强生公司的新冠疫苗与极为罕见的血栓之间存在“可能的联系”,但是接种强生疫苗的好处仍大于风险。强生公司宣布将调整疫苗的包装标签,以警告这种罕见副作用的风险,并提供有关如何识别和治疗该副作用的说明;并恢复在欧洲的推广计划,恢复向欧盟、挪威和冰岛的疫苗运输。
2.Agenus差异化PD-1抗体balstilimab申报美国上市。Agenus公司PD-1疗法balstilimab已通过加速审批程序向FDA提交了生物制品许可申请(BLA),用于治疗在化疗期间或之后疾病进展的复发性或转移性宫颈癌患者。在一项Ⅱ期临床中,balstilimab在PD-L1阳性肿瘤患者的ORR达到20%,所有肿瘤(PD-L1阳性和阴性)患者的ORR为15%,中位DOR为15.4个月。目前,Agenus公司正计划开展一项国际Ⅲ期验证性研究,旨在支持balstilimab的全球注册。
3.礼来治疗斑秃新药baricitinib临床结果积极。礼来与Incyte公司联合开发的JAK抑制剂巴瑞替尼(baricitinib)在治疗重度斑秃的第二项Ⅲ期临床BRAVE-AA1中获积极结果。与安慰剂相比,baricitinib(4 mg、2 mg)治疗组36周后达到头皮毛发覆盖率超过80%的患者比例显著更高(35%、22%,安慰剂5%)。这些数据与3月公布的Ⅲ期临床BRAVE-AA2结果一致。礼来计划今年下半年向FDA提交baricitinib治疗斑秃的补充新药申请,它有望成为FDA批准的首个斑秃疗法。
4.Vertex增加与CRISPR合作的投资。Vertex公司和CRISPR Therapeutics更新了双方联合开发的CRISPR/Cas9基因编辑疗法CTX001的合作协议。CTX001目前已获得FDA授予治疗输血依赖性β地中海贫血综合征(TDT)和镰刀型细胞贫血病(SCD)的再生医学先进疗法认定、以及快速通道和孤儿药资格。根据新的协议,CRISPR将再获得一笔9亿美元的预付款,有资格获得2亿美元的CTX001首次监管批准的里程碑付款。此外,CRISPR将投资进一步的创新,承担40%的成本和获得40%的利润。
5.Alnylam公司RNAi疗法最新研究结果发表。Alnylam公司RNAi疗法Lumasiran治疗原发性1型高草酸尿症(PH1)的最新Ⅲ期研究结果发表在NEJM上。研究结果显示,与安慰剂相比,Lumasiran显著降低患者尿液中的草酸含量,两组患者尿液中的草酸含量平均降低了65.4%和11.8%;两组6个月后患者24小时尿草酸水平不高于正常范围上限的1.5倍的患者比例分别为84%和0%,24小时尿草酸水平等于或低于正常范围的上限的患者比例分别为52%和0%。
6.Akouos基因疗法AK-OTOF获FDA孤儿药资格。FDA授予Akouos公司基因疗法AK-OTOF孤儿药资格,用于治疗耳铁蛋白基因(OTOF)介导的听力损失。AK-OTOF使用腺相关病毒(AAV)载体将OTOF基因的健康拷贝传递到耳蜗的感觉细胞,目的是在单次给药后通过促进正常功能性耳铁蛋白在受影响的耳蜗细胞中的表达,恢复长期的生理听力。
7.强生公布一季度业绩报告,同比增长7.9%。4月20日,强生发布2021年第一季度业绩报告,销售额223亿美元,较去年同期强劲增长7.9%。其中,美国市场销售额111.11亿美元(+3.9%),国际市场销售额112.1亿美元(+12.2%)。制药业务销售额121.99亿美元(+7.4%),其中Tremfya(+46.3%)、Darzalex(+49.2%)、Erleada(+44.0%)等表现出色,COVID-19疫苗销售额1亿美元,但Zytiga下降了64.2%。
医药热点
1.全国医院100强排名出炉。艾力彼医院管理研究中心与社会科学文献出版社日前共同发布了《医院蓝皮书:中国医院竞争力报告(2020~2021)》。其中,“2020年顶级医院100强”排名中,北京协和医院、四川大学华西医院、复旦大学附属中山医院位列前三名。除内蒙古、青海、西藏、贵州、海南,其他省份至少有一家医院进入顶级医院100强榜单,其中北京、上海、广东上榜医院最多。
2.珠海率先实现目标人群接种率超80%。截至2021年4月20日12时,珠海市累计接种新冠疫苗141.7万人,成为全国首个新冠病毒疫苗18-59岁目标人群接种覆盖率超过80%的地级市。为做好大规模接种工作,珠海市成立了疫苗接种工作专班,成立以市长为组长的疫苗接种工作领导小组,下设疫苗接种实施和医疗救治、疫苗及接种工作经费保障等5个专责工作组,统筹推进全市疫苗接种实施工作。目前该市已达到日接种超10万剂次的接种能力。
3.中国科学家开发出非侵入性肺结节诊断新方法。广州医科大学附属第一医院何建行教授、南方医科大学范建兵教授等研究团队在医学期刊The Journal of Clinical Investigation在线发表一篇关于非侵入性DNA甲基化检测对肺结节准确诊断的研究论文。研究人员开发了一种基于血液DNA甲基化的新型诊断模型(PulmoSeek),并对其进行了验证。研究结果显示:PulmoSeek在肺结节的分类方面优于PET-CT和其它预测模型的效果,有助于为早期肺癌患者提供更加精准的治疗。
4.礼来乳腺癌新药启动中国慈善援助项目。4月19日,礼来CDK 4/6抑制剂唯择(阿贝西利片)在中国正式上市,为中国晚期乳腺癌患者带来新的治疗选择。为帮助晚期乳腺癌患者减轻用药经济负担,由中国妇女发展基金会发起、礼来支持的“汝爱有礼”慈善援助项目同时在北京正式启动,项目将为符合条件的患者提供药品援助,捐赠药品将由礼来向中国妇女发展基金会无偿捐赠。
审评动向
1. CDE新药受理情况(04月21日)
申请临床:
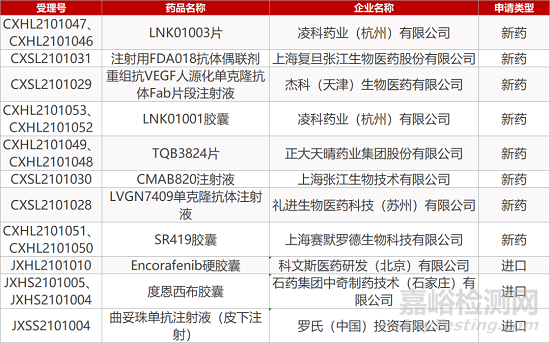
凌科药业的LNK01003片(2个规格)和LNK01001胶囊(2个规格)、复旦张江的注射用FDA018抗体偶联剂、杰科(天津)的重组抗VEGF人源化单克隆抗体Fab片段注射液、正大天晴的TQB3824片(2个规格)、上海张江的CMAB820注射液、礼进的LVGN7409单克隆抗体注射液、上海赛默罗德的SR419胶囊(2个规格)、科文斯医药的Encorafenib硬胶囊。
申请生产:
石药集团中奇的度恩西布胶囊(2个规格)、罗氏的曲妥珠单抗注射液(皮下注射)。
2. FDA新药获批情况(北美04月19日)

股市资讯
【特一药业】公司全资子公司海力制药近日取得了国家药监局颁发的阿莫西林胶囊《药品补充申请批准通知书》,该产品共有2个规格,分别为0.25g、0.5g。
【三生国健】公司重组抗IL-17A人源化单克隆抗体治疗中重度斑块状银屑病II期临床试验于近日完成首例受试者入组。
【复旦张江】注射用FDA018 ADC药物临床申请获NMPA受理。

来源:药研发


