您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-07-23 10:44
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
诗健Trop-2-ADC获批临床。诗健生物「重组人源化抗Trop2单抗-SN38偶联物」获国家药监局临床试验默示许可,拟开发用于治疗实体瘤。这是一款靶向Trop-2的抗体偶联药物(ADC),研发代号为ESG-401,由诗健生物和联宁(苏州)联合开发。在多种Trop-2表达的肿瘤模型中,ESG-401显示出显著的抑瘤活性,具有有效剂量低,对肿瘤生长的抑制时间长等特点。此外,ESG-401具有良好的安全性。
国内药讯
1.国产mRNA新冠疫苗启动III期临床。沃森生物与艾博生物联合开发的mRNA新冠病毒疫苗ARCoVaX(ARCoV)在国内登记启动一项III期临床,拟招募2000例受试者评估间隔28天接种2剂疫苗的保护效力、安全性和免疫原性。ARCoVaX由脂质纳米粒(LNPs) 包裹,靶向SARS-CoV-2棘突蛋白RBD区域。单剂或两剂ARCoV免疫可在小鼠和非人类灵长类动物中激发抗多种流行SARS-CoV-2毒株的强大抗体和T细胞应答。该疫苗临床前研究结果已发表在Cell杂志上。
2.亚盛新药APG-115获FDA孤儿药资格。FDA授予亚盛医药MDM2-p53抑制剂新药APG-115孤儿药资格,用于治疗IIB-IV期黑色素瘤。这也是该新药继胃癌、急性髓系白血病、软组织肉瘤、视网膜母细胞瘤后,获得的FDA授予的第五项孤儿药资格。公布于ASCO2021年会上的一项APG-115联合帕博利珠单抗的II期临床最新数据显示,这一组合在PD-1/PD-L1抑制剂耐药的黑色素瘤队列中的ORR达到24.1%,DCR达到55.2%。
3.BMS抗体组合国内获批临床。百时美施贵宝(BMS)relatlimab/nivolumab固定剂量复方注射液获国家药监局临床试验默示许可,拟开发用于晚期实体瘤。Relatlimab是一款抗LAG-3抗体,此前它与PD-1抗体nivolumab(Opdivo,纳武利尤单抗)的组合疗法,已在治疗转移性或不可切除的黑色素瘤初治患者的Ⅱ/Ⅲ期临床RELATIVITY-047中达到无进展生存期(PFS)的主要终点,组合疗法与nivolumab相比的中位PFS分别为10.12个月和4.63个月。
4.德琪新药ATG-101在澳获批临床。德琪医药新型PD-L1/4-1BB双抗ATG-101获澳大利亚Bellberry人类研究伦理委员会(HREC)批准,即将在澳大利亚开展用于治疗转移性或晚期实体瘤及B细胞非霍奇金淋巴瘤(B-NHL)的I期临床试验,评估ATG-101单药治疗的安全性及耐受性。在临床前研究中,ATG-101在多种PD-1/PD-L1抑制剂耐药或复发性动物模型中,均显示出显著的抗肿瘤效果;在GLP毒理实验中,ATG-101也显示出良好的安全性。
5.雅创医药与华东医药开展联合用药研究。雅创医药FXR激动剂HPG1860与华东医药旗下中美华东的口服GLP-1R激动剂TPP-273等构成的组合方案,将开展联合用药临床研究,评估联合治疗非酒精性脂肪型肝炎(NASH)的有效性和安全性。HPG1860是雅创医药自主研发并拥有全球知识产权的FXR激动剂,用于NASH、原发性胆汁性胆管炎(PBC)和原发性硬化性胆管炎(PSC)等适应症开发已进入II期临床。
国际药讯
1.罕见神经退行性疾病基因疗法获欧盟批准。欧盟委员会(EC)批准bluebird bio公司基因疗法Skysona(elivaldogene autotemcel,Lenti-D)上市,用于治疗18岁以下携带ABCD1基因突变的早期脑性肾上腺脑白质营养不良患者(CALD)。Skysona也是欧盟(EU)批准的首款用于治疗CALD的基因疗法。在一项关键性Ⅱ/Ⅲ期ALD-102试验中,有90%的患者达到第24个月无主要功能障碍(MFD)的生存终点,并且大多数患者的神经功能得以维持。
2.拜耳心衰新药获欧盟批准上市。欧盟委员会批准拜耳维立西呱(Verquvo™)上市,用于治疗症状性慢性心力衰竭成人患者(射血分数降低、近期发生过需要静脉治疗的失代偿事件稳定后)。维立西呱是首个获批用于治疗心力衰竭的sGC刺激剂,已在美国和日本获批上市。一项Ⅲ期临床中位随访时间为10.8个月时,该药较安慰剂降低了因心衰住院和心血管原因死亡的复合终点风险(35.5%vs38.5%,HR=0.90,P=0.02)。
3.Venetoclax再获突破性疗法认定。FDA授予罗氏与艾伯维联合开发的“first-in-class”BCL-2抑制剂Venclexta(venetoclax)突破性疗法认定,与阿扎胞苷(azacitidine)联用,用于一线治疗中/高/极高风险的骨髓增生异常综合征成人患者。Venclexta能够选择性地靶向结合一些血液癌症和实体瘤细胞上高度表达的BCL-2蛋白并抑制其活性,从而恢复肿瘤细胞凋亡的过程。这也是Venclexta获得的第六个突破性疗法认定。
4.罗氏基因疗法SPK-8011长期疗效积极。罗氏旗下Spark Therapeutics开发的基因疗法SPK-8011在ISTH 2021年会上公布其用于治疗血友病A患者的最长达4年的最新随访数据。在接受SPK-8011治疗的18例患者中,有16例患者维持持久的凝血因子VIII表达;患者的年出血率(ABR)下降91.2%,每年因子VIII输注率下降97%。SPK-8011是一款使用AAV-LK03衣壳构成的生物工程化AAV载体递送的基因疗法,已获FDA和欧盟授予的孤儿药资格。
5.罕见遗传性疾病RNAi疗法早期临床积极。Dicerna公司在研GalXC RNAi疗法belcesiran在治疗α-1抗胰蛋白酶缺乏症相关肝病(AATLD)的Ⅰ期临床中获积极结果。Belcesiran旨在靶向产生异常AAT蛋白的基因,以减少肝脏中AAT的产生。该项中期分析的数据显示,与基线相比,belcesiran平均将AAT蛋白水平降低50%(1.0 mg/kg)、69%(3.0 mg/kg)和80%(6.0 mg/kg);而且,belcesiran总体耐受性良好,具有可控的安全性特征。
6.BioNtech收购吉利德抗原TCR平台。BioNTech宣布收购吉利德旗下公司Kite在马里兰州Gaithersburg的实体肿瘤新抗原T细胞受体(TCR)研发平台和临床生产工厂,以扩大其新型细胞治疗管线的开发。该公司肿瘤管线产品包括基于CAR-T细胞扩增mRNA疫苗(CARVac)和拟用于治疗黑色素瘤的候选产品BNT221(NEO-PTC-01),以及新获得的个体化新抗原疫苗BNT122等。其中,BNT122可靶向20种肿瘤新抗原,已在I期实体瘤患者中显示出抗肿瘤活性。
医药热点
1.广东规范医共体联合门诊病房运行。广东省印发《广东省紧密型县域医共体联合门诊和联合病房运行指南(试行)》《广东省紧密型县域医共体双向转诊管理中心运行指南(试行)》,为联合门诊和联合病房运行、双向转诊管理中心运行提供明确指引。针对双向转诊管理,该省要求总医院成立双向转诊管理中心,医共体内县级医院的各临床科室设立连续医疗服务专员,各分院设立连续医疗服务联络员,确保双向转诊时对患者服务的连贯性和闭环性。
2.南京6地调整为中风险地区。南京市卫健委宣布,自2021年7月21日起,南京市禄口街道曹村村张家自然村、欢墩山自然村,永兴社区外槽坊自然村,溧塘村铜山端自然村,茅亭社区百利华府小区三期、茅亭小区由低风险地区调整为中风险地区。根据最新防控要求,南京市倡导市民群众非必要不离宁,确需离宁的,需持有48小时内核酸检测阴性证明。
3.第二批区域医疗中心试点项目公布。国家发改委等部门联合下发 《关于第二批区域医疗中心试点项目有关事项的通知》,共有16家医院获批,包含有福建4家,河南3家,河北、山西、新疆、云南各2家,安徽1家,标志着我国第二批均衡优质医疗资源布局,提升区域医疗服务能力等关键措施正式进入到落地实施阶段。据悉,国家第一批区域医疗中心试点选择了河北、辽宁、山西、福建、安徽、云南等8个省份,促成了10个项目,现已先后投入使用。
审评动向
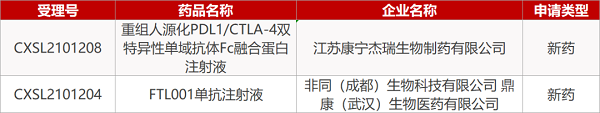
江苏康宁杰瑞的重组人源化PDL1/CTLA-4双特异性单域抗体Fc融合蛋白注射液、非同(成都)/鼎康(武汉)的FTL001单抗注射液。
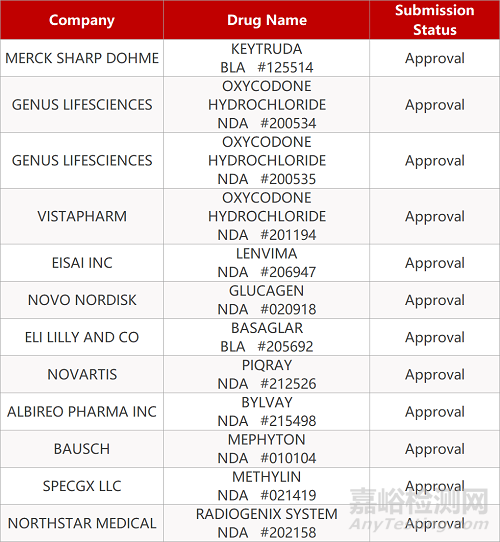

来源:药研发


