您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-09-14 11:05
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
苏州银杏树「赛拉瑞韦钾片」报NDA。银杏树药业(苏州)旗下1.1类新药赛拉瑞韦钾片的上市申请获CDE受理。赛拉瑞韦钾是一款针对丙肝病毒的第二代蛋白酶抑制剂,与第一代上市药物相比,赛拉瑞韦钾具有更好的药效与药代动力学特征。目前国内尚无针对丙肝的小分子靶向药上市,塞拉瑞韦钾片有望成为中国首个口服丙肝疗法。
国内药讯
1.百济神州PD-1单抗在美报BLA。FDA受理百济神州PD-1抗体百泽安(替雷利珠单抗注射液)的新药上市申请(BLA),用于二线治疗不可切除、复发性局部晚期或转移性食管鳞状细胞癌,PDUFA日期为2022年7月12日。在一项全球Ⅲ期临床RATIONALE 302中,百泽安在意向性治疗(ITT)人群的中位总生存期达到8.6个月,降低死亡风险超过30%,且客观缓解率(ORR)达20.3%。详细结果已在ASCO 2021上公布。
2.EpCAM/CD3双抗早期临床积极。友芝友生物EpCAM/CD3双抗M701将于ESMO2021年会上公布针对恶性腹水的Ⅰ期临床积极结果。在16例可评估患者中,M701总体客观反应率(ORR)达到62.5%,疾病控制率(DCR)为100%,总生存时间中位数(mOS)为152天(其中卵巢癌患者的mOS为148天,胃癌患者的mOS为209天)。与已上市的药物相比,M701在卵巢癌和胃癌患者中已初步展示出改善总生存期的趋势。
3.诺和诺德PCSK9抑制剂获批降脂临床。诺和诺德1类新药NNC0385-0434片获国家药监局临床试验默示许可,拟单药或与他汀类药物联合使用,在杂合子型家族性高胆固醇血症、确诊心血管疾病或心血管高风险的成人患者中降低低密度脂蛋白胆固醇(LDL-C)。NNC0385-0434是一款靶向PCSK9的口服制剂,目前正在一项Ⅱ期临床中评估降低心脏病或心脏病高危人群的胆固醇的潜力。
4.恒瑞SHR7280辅助生殖获批临床。恒瑞新型口服GnRHR拮抗剂SHR7280片获国家药监局临床试验默示许可,拟临床应用于辅助生殖,用于控制性超促排卵治疗的患者,防止提前排卵。SHR7280可阻断内源性GnRH与GnRH受体的结合,抑制黄体生成素和卵泡刺激素等促性腺激素的合成和释放,降低睾酮和雌二醇等性激素水平,维持正常的生殖系统功能。
5.RIP1抑制剂在华获批临床。维泰瑞隆(北京)生物1类新药SIR1-365片获国家药监局临床试验默示许可,拟开发用于治疗与全身性炎症反应综合征(SIRS)相关的感染性疾病。SIR1-365是一款RIP1抑制剂,此前已在美国登记启动了一项Ⅰ期临床,旨在评估SIR1-365在重症COVID-19患者中的安全性和有效性。此次为SIR1-365首次在国内获批临床。
国际药讯
1.辉瑞Myfembree新适应症报sNDA。FDA受理辉瑞与Myovant Sciences公司联合开发的Myfembree(relugolix 40mg、雌二醇1.0mg、醋酸炔诺酮0.5mg)的补充新药申请,用于治疗与子宫内膜异位症相关的中重度疼痛,PDUFA日期为2022年5月6日。Myfembree是一款GnRH受体拮抗剂,已于今年5月获FDA批准上市,成为首个治疗绝经前女性子宫肌瘤相关月经过多(HMB)的每日一次药物,治疗持续时间可长达24个月。
2.HER2双抗治疗GEA最新临床数据积极。Zymeworks公司靶向HER2的双特异性抗体zanidatamab,用于一线治疗HER2表达的胃食管腺癌(GEA)患者的临床试验获最新积极数据。截至2021年3月18日,在22例可评估患者中,zanidatamab联合标准化疗达到68.2%的确认客观缓解率。最新结果将在即将召开的ESMO大会上公布。百济神州拥有zanidatamab在亚洲(日本除外)、澳大利亚和新西兰的开发和商业化授权。目前zanidatamab在中国已获批临床。
3.基因编辑干细胞疗法获快速通道资格。FDA授予Vor Biopharma工程化造血干细胞(eHSC)疗法VOR33快速通道资格,用于治疗急性髓系白血病(AML)患者。VOR33是研究人员利用CRISPR/Cas9基因编辑技术,在体外敲除编码CD33基因的一款造血干细胞疗法。该疗法回输到患者体内将产生不表达CD33蛋白的健康新细胞。VOR33旨在替代复发风险高的AML患者的标准移植治疗,降低其潜在的副作用。
4.CD3/D20双抗早期临床积极。Genmab与艾伯维联合开发的CD3/D20双抗epcoritamab用于治疗复发/难治性B细胞非霍奇金淋巴瘤(B-NHL)的Ⅰ/Ⅱ期临床EPCORE NHL-1积极结果发表在《柳叶刀》上。初步结果显示,epcoritamab达到88%的总缓解率(ORR)和38%的完全缓解(CR);而且,在剂量递增过程中未观察到剂量限制性毒性。目前Ⅱ期临床推荐剂量(RP2D)已确定为48 mg。
5.mRNA抗癌疗法发表最新研究成果。赛诺菲、BioNTech联合德国科学家在《科学》子刊上发布最新研究成果。研究人员使用mRNA编码4种促炎性细胞因子(IL-12、IFN-α、粒细胞-巨噬细胞集落刺激因子和IL-15)并瘤内注射给药,在小鼠模型中成功刺激了抗肿瘤免疫应答,显著缩小肿瘤并延长了小鼠的生存期。目前,BioNTech和赛诺菲正在Ⅰ期临床篮子试验中,评估候选药物SAR441000 (BNT131)单药治疗晚期黑色素瘤患者,以及与PD-1/PD-L1抑制剂联用,治疗晚期黑色素瘤等实体瘤。
6.Obsidian公司完成B轮融资。Obsidian公司宣布完成1.15亿美元的B轮融资。Obsidian先导cytoTIL项目cytoTIL15是一款基于cytoDRiVE技术开发的一款工程化肿瘤浸润淋巴细胞(TIL)疗法,目前处于临床前开发阶段,拟用于治疗转移性黑色素瘤和其他实体瘤。此轮融资将用于推动cytoTIL15进入临床,评估用于治疗转移性黑色素瘤的安全性和有效性。Obsidian还计划将cytoTIL15快速扩展到其他多种实体瘤领域。
医药热点
1.CDE官网新版本上线。CDE官网全新版本于13日正式上线。与旧版相比,新网站布局更合理、字体更大;导航栏的临床试验登记、BE试验备案平台整合到登记备案平台(共4个:原辅包、临床试验、BE备案、专利登记);8个热门专题放到了醒目位置:指导原则、ICH、行政受理服务、一致性评价、儿童药、专利登记、化药目录集以及eCTD专栏;信息公开栏目共上线14个数据库,点击浏览更为顺畅。
2.村级医疗卫生巡诊派驻有规范。国家卫健委日前印发《关于做好村级医疗卫生巡诊派驻服务工作的通知》,规范村级医疗卫生巡诊、派驻和邻(联)村卫生室延伸服务工作,巩固实现基本医疗有保障工作成果。《通知》要求,县级相关部门要在药品、设备、车辆等方面提供保障。严格落实邻(联)村服务人员的各项补助。执业医师晋升为副高级职称的,巡诊服务、派驻服务可作为其基层工作经历。
3.中国罕见病定义研究报告发布。9月11日,《中国罕见病定义研究报告2021》在上海发布,报告中首次提出了“中国罕见病2021年版定义”,即应将“新生儿发病率小于1/万、患病率小于1/万、患病人数小于14万的疾病”列入罕见病。罕见病定义的重新修订,为制定中国孤儿药定义提供了参考,也为今后孤儿药的研发和生产,制定保护和激励政策奠定了基础。
4.美国CDC:疫苗有效降低新冠死亡率。美国疾控中心(CDC)10日发布一份报告称,未接种新冠疫苗的美国人被感染的可能性是完成疫苗接种者的4.5倍,住院的可能性是接种疫苗者的10倍,死于新冠肺炎的可能性是接种疫苗者的11倍。该研究显示出接种疫苗对降低新冠肺炎感染率和死亡率的有效性。目前,美国还有近8000万人没接种疫苗。
评审动态
申请临床:
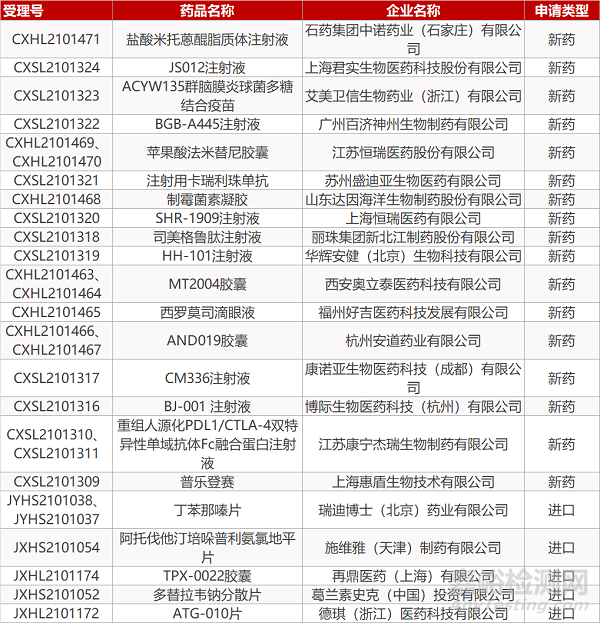
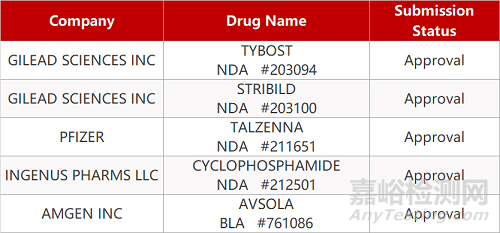
石药集团中诺药业的盐酸米托蒽醌脂质体注射液、上海君实的JS012注射液、艾美卫信生物药业的ACYW135群脑膜炎球菌多糖结合疫苗、广州百济神州的BGB-A445注射液、江苏恒瑞的苹果酸法米替尼胶囊(2个规格)、苏州盛迪亚的注射用卡瑞利珠单抗、山东达因的制霉菌素凝胶、上海恒瑞的SHR-1909注射液、丽珠集团新北江的司美格鲁肽注射液、华辉安健的HH-101注射液、西安奥立泰的MT2004胶囊(2个规格)、福州好吉医药的西罗莫司滴眼液、杭州安道药业的AND019胶囊(2个规格)、康诺亚的CM336注射液、博际生物的BJ-001 注射液、江苏康宁杰瑞的重组人源化PDL1/CTLA-4双特异性单域抗体Fc融合蛋白注射液、上海惠盾生物的普乐登赛、再鼎医药的TPX-0022胶囊、葛兰素史克的多替拉韦钠分散片、德琪的ATG-010片。
申请生产:
瑞迪博士的丁苯那嗪片(2个规格)、施维雅的阿托伐他汀培哚普利氨氯地平片。

来源:药研发


