您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-09-29 11:06
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
李氏大药厂PD-L1单抗将报产。李氏大药厂宣布附属公司中国肿瘤医疗有限公司已获CDE批准提交抗PD-L1单克隆抗体Socazolimab(研发代号:ZKAB001)治疗复发性或转移性宫颈癌的新药上市申请。今年1月,ZKAB001被纳入突破性疗法程序,用于接受过一线含铂方案失败或不能耐受的复发转移性宫颈癌。这是国内第5款提交上市申请的PD-L1单抗。截至目前,国内仅两款进口PD-L1单抗获批上市。
国内药讯
1.康方IL-4Rα单抗启动国际II期临床。康方生物自主研发靶向IL-4Rα的新型自身免疫疾病治疗药物AK120注射液获FDA批准,启动用于治疗中重度特应性皮炎(AD)的全球II期临床。在新西兰和澳大利亚完成的I期临床中,AK120在健康受试者(单剂量600 mg)和AD患者(单剂量300mg)中均表现出良好的安全性和耐受性;在每个给药方案中都呈现出良好的疗效,且具有较好剂量依赖性。
2.绿叶长效GLP-1受体激动剂获批临床。绿叶制药旗下公司博安生物在研的度拉糖肽注射液(BA5101)获国家药监局临床试验默示许可。度拉糖肽是Truliciyt(度易达,礼来)的生物类似药,可通过激活GLP-1受体,进而增加β细胞内cAMP的含量,最终促进葡萄糖依赖性胰岛素的释放,可用于成人2型糖尿病的血糖控制。度拉糖肽是一款长效的降糖用药,每周仅需给药1次,可为患者提供更好的用药体验。
3.降血脂新药IMM-H007报IND。北京谷神生命健康科技公司与中国医学科学院药物研究所共同申报的1类新药IMM-H007片的临床试验申请已获CDE受理。IMM-H007是根据天然产物虫草素(3’-脱氧腺苷)的结构改造合成的一款新型AMPK激动剂,临床前的研究表明其具有良好的安全与药效,有望开发成为降血脂及治疗相关疾病的新药。
4.信达引进新一代PDE4抑制剂。信达生物与UNION公司就UNION处于II期临床、拟用于治疗炎症性皮肤病的PDE4抑制剂orismilast达成独家授权协议。根据协议,信达将获得orismilast在中国(包括中国大陆、香港、澳门和台湾)开发和商业化的独家权益;UNION将获得2000万美元的首付款,累计不超过2.47亿美元的里程碑付款,以及产品的销售分成。UNION保留orismilast在除中国以外的全球其他地区的权益。
5.恒瑞「氟唑帕利」获批临床。恒瑞医药PARP抑制剂氟唑帕利获国家药监局临床试验默示许可,即将开展一项Ib/III期临床,联合贝伐珠单抗对比卡培他滨联合贝伐珠单抗用于不可切除或转移性结直肠癌一线维持治疗。氟唑帕利是恒瑞开发的1.1类新药,已于去年12月获批上市,用于既往经过二线及以上化疗的伴有胚系BRCA突变(gBRCAm)的铂敏感复发性卵巢癌、输卵管癌或原发性腹膜癌,以及铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌的维持治疗。
国际药讯
1.口服补体C5aR抑制剂在日本获批。日本厚生劳动省(MHLW)批准ChemoCentryx、Vifor Pharma与Kissei Pharmaceutical联合开发的C5aR抑制剂Tavneos(avacopan)上市,用于治疗两种主要的抗中性粒细胞胞浆自身抗体(ANCA)相关血管炎:显微镜下多血管炎(MPA)和肉芽肿伴多血管炎(GPA)。在一项Ⅲ期临床中,avacopan治疗组第52周时的缓解率优于标准治疗(65.7%vs54.9%)。这是avacopan在全球范围内首次获批。目前它正在接受FDA的审评。
2.卫材/渤健Aβ抗体报滚动BLA。卫材宣布启动向FDA滚动提交其在研抗Aβ原纤维抗体lecanemab的生物制品许可申请(BLA),用于治疗早期阿尔茨海默病(AD)。在一项Ⅱb期临床(Study 201)中,最高剂量(10 mg/kg)的lecanemab能显著降低患者大脑中的淀粉样蛋白水平;而且接受安慰剂治疗的患者在扩展研究中转为接受lecanemab治疗后,淀粉样蛋白水平也显示出降低的结果。今年6月,FDA已授予lecanemab突破性疗法认定。
3.BMS两款免疫组合疗法报sBLA。FDA受理百时美施贵宝PD-1抑制剂纳武利尤单抗的补充生物制品许可申请(sBLA),与伊匹木单抗构成双重免疫疗法,以及联合氟尿嘧啶和含铂化疗构成的组合疗法,用于一线治疗晚期不可切除性、复发性或转移性食管鳞状细胞癌(ESCC)。在一项关键性Ⅲ期临床中,与化疗对照组相比,纳武利尤单抗加伊匹木单抗,或纳武利尤单抗加化疗,均显著提高患者的总生存期(OS)获益。
4.Keytruda治疗肝癌Ⅲ期临床积极。默沙东PD-1抗体Keytruda治疗接受过索拉非尼(sorafenib)治疗的亚洲晚期肝细胞癌患者的Ⅲ期临床达到总生存期(OS)的主要终点。与安慰剂加最佳支持治疗(BSC)相比,Keytruda与BSC联用使患者的OS获得具有统计学意义的显著改善。该试验同时也达到无进展生存期(PFS)和客观缓解率(ORR)的关键性次要终点。临床中未观察到新的安全性信号。
5.IL-13α1单抗治疗皮炎早期临床积极。亚狮康(ASLAN Pharmaceuticals)IL-13α1靶向单抗ASLAN004治疗中重度特应性皮炎(AD)的Ⅰ期临床获积极初步数据。在修订的意向治疗人群(n=29)中,ASLAN004治疗组第8周时患者的EASI相对基线平均降低65%(n=16),而安慰剂组患者为27%(n=13)(p=0.021);两组达EASI-75应答的患者比例分别为69%和15%(p=0.005)。ASLAN计划今年年底启动一项ASLAN004治疗AD的国际Ⅱb期试验。
6.辉瑞/BioNTech流感mRNA疫苗上临床。辉瑞与BioNTech联合开发的mRNA四价流感疫苗在Ⅰ期临床中完成首批成人志愿者接种。mRNA流感疫苗只需要病毒的基因序列,而且mRNA技术的灵活性和快速、大规模生产特点,能使疫苗株与流行的病毒株很好地匹配,提高流感疫苗有效性。该公司还计划探索mRNA在其它呼吸道病毒中的应用,并将扩展mRNA技术在肿瘤学和遗传疾病中的应用。
医药热点
1.辽宁全科医生转岗培训启动。辽宁省日前启动了2021年度全科医生转岗培训工作,辽宁省省级以上财政补助培训学员800人,补助标准为每人1.5万元。培训对象包括:基层医疗卫生机构中已取得临床执业(助理)医师资格,拟从事全科医疗工作,尚未接受过全科医生专业培训的临床执业(助理)医师;二级及以上医院中取得临床执业医师资格,从事临床医疗工作3年及以上,拟从事全科医疗工作,尚未接受过培训的其他专业临床执业医师。
2.国家发文推进医院安全秩序管理工作。国家卫健委等八部门日前印发《关于推进医院安全秩序管理工作的指导意见》,旨在进一步维护正常医疗秩序,保护医务人员人身安全。《指导意见》明确医院保安员数量应当遵循“就高不就低”原则,按照不低于在岗医务人员总数的3%或者20张病床1名保安或日均门诊量3‰的标准配备,有条件的医院可以在此基础上增加保安员数量。
3.江苏首部医保发展规划出炉。江苏省日前公布了江苏省社会保障制度建立以来第一部医疗保障领域的专项规划——《江苏省“十四五”医疗保障发展规划》。《规划》根据提出的7个方面主要目标,明确了“十四五”医保事业发展的12项主要发展指标和46项举措。到“十四五”末,职工医保和居民医保政策范围内住院报销比例将分别稳定在85%和70%左右,职工参保人数占总参保人数的45%以上,政务服务事项线上、窗口可办率达到100%,住院费用跨省直接结算率达到85%。
评审动态
申请临床:
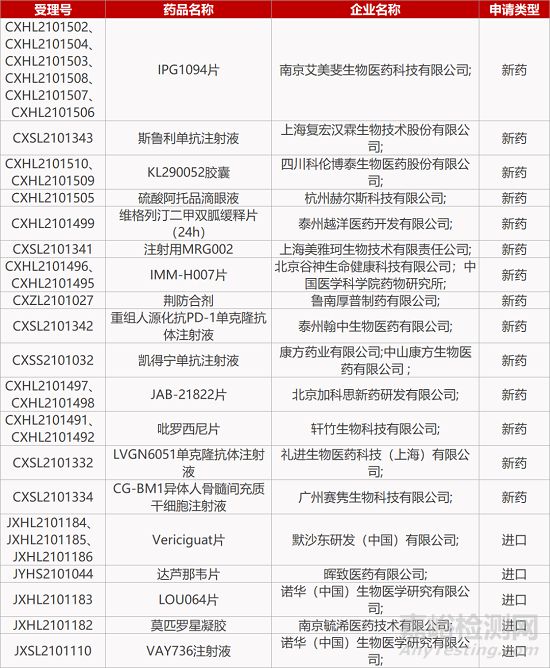
南京艾美斐生物的IPG1094片(6个规格)、上海复宏汉霖的斯鲁利单抗注射液、四川科伦博泰生物的KL290052胶囊(2个规格)、杭州赫尔斯的硫酸阿托品滴眼液、泰州越洋医药的维格列汀二甲双胍缓释片(24h)、上海美雅珂生物的注射用MRG002、北京谷神生命健康/中国医学科学院药物研究所的IMM-H007片(2个规格)、鲁南厚普制药的荆防合剂、泰州翰中生物的重组人源化抗PD-1单克隆抗体注射液、北京加科思的JAB-21822片(2个规格)、轩竹生物的吡罗西尼片(2个规格)、礼进生物的LVGN6051单克隆抗体注射液、广州赛隽生物的CG-BM1异体人骨髓间充质干细胞注射液、默沙东的Vericiguat片(3个规格)、诺华的LOU064片、南京毓浠医药的莫匹罗星凝胶、诺华的VAY736注射液。
申请生产:
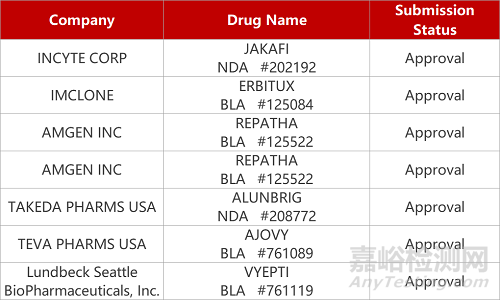
康方药业/中山康方的凯得宁单抗注射液、晖致医药的达芦那韦片。

来源:药研发