您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-11-21 14:33
(一) 测定方法概述


(二)可溶性糖类的提取和澄清
1、提取液制备
(1)常用提取剂——水、乙醇
(2)提取液中含糖量控制0.5~3.5mg/mL
(3)含脂肪食品先脱脂,然后用水提取
(4)含淀粉及糊精食品(乙醇沉淀淀粉等)用70~75%乙醇溶液提取
(5)含乙醇及CO2液态食品,蒸发至1/3~1/4原体积,以除去C2H5OH及CO2
(6)酸性食品应先中和防止低聚糖部分水解
(7) 提取固体样品有时需要加热,以提高提取效果。一般在40~50℃,防止多糖溶出
(8) 乙醇作提取剂加热时应安装回流装置
2、提取液的澄清
(1)影响测定的杂质
色素、蛋白质、果胶、可溶性淀粉、有机酸、氨基酸、单宁,可影响颜色、浑浊、过滤困难。
(2)澄清剂
①醋酸铅(中性)Pb(CH3COO)2·3H2O,形成沉淀,吸附杂质,可除去蛋白质、果胶、有机酸、单宁等。
②乙酸锌和亚铁氰化钾二者生成氰亚铁酸锌↓吸附蛋白质等干扰物。
③硫酸铜和氢氧化钠 Cu离子使蛋白质沉淀。
(3)澄清剂用量
用量适宜,以无新沉淀为准,如2ml饱和醋酸铅(30%)、
(4)除铅剂
由于铅影响还原糖的测定,生成铅糖化合物。
常用除铅剂有草酸钠、硫酸钠、磷酸氢二钠。
(三)蓝—爱农(Lane-Eynon)法
测定还原糖
(国际上常用的定量糖的方法)
1、原理
斐林试剂甲液(CuSO4·5H2O)
斐林试剂乙液(酒石酸钾钠+NaOH)
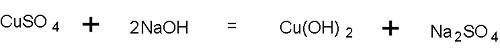
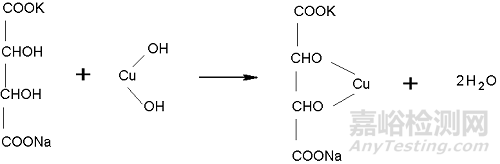
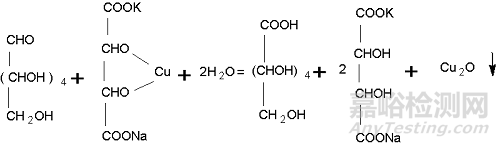
甲、乙混合→酒石酸钾钠合铜
酒石酸钾钠合铜+葡萄糖 →葡萄糖酸 + Cu2O↓(红棕)
终点的确定:
葡萄糖+亚甲基蓝(氧化态)→亚甲基蓝(还原态)
过量 兰色 无色
(兰色消失)
终点时的颜色为:兰色消失了的红棕色
2、测定
①预测
准确吸取斐林试剂甲液5.00mL、乙液5.00mL→锥形瓶中,△至沸腾,再加入亚甲基蓝指示剂,在加热的条件下,用样液滴至蓝色褪尽。(先快后慢,要求很快达到终点,因为亚甲基蓝易被空气氧化为蓝色,且要求在加热的情况下以除去空气)
②测定
甲液5mL、乙液5mL→锥形瓶中,加入比上述预测量少0.5~1ml样液在2min内沸腾,维持沸腾2min,加入3滴亚甲基蓝指示剂,再在3min内滴定至蓝色褪尽。
3、计算
F
还原糖 % = --------------------- ×100
( V1/V ) × m
m--样品质量,mg;V1--滴定量mL;V--样液总mL;
F--还原糖因素,10mL费林试剂,相当的还原糖量mg
F的求得有两种方法:
A、用标准还原糖液用上面同样方法标定10ml费林试剂求得。
B、查蓝—爱农法专用“还原糖因数表”附表
例 若V1=26 则F=49.9
(四)直接滴定法测定还原糖
1、原理 (GB/T5009.7-1985)
斐林试剂甲液(CuSO4·5H2O+亚甲基蓝),斐林试剂乙液(酒石酸钾钠+NaOH+亚铁氰化钾,混合→酒石酸钾钠合铜,酒石酸钾钠合铜+葡萄糖→葡萄糖酸 + Cu2O↓(红棕),亚铁氰化钾使Cu2O↓(红棕)生成无色络合物K2Cu2Fe(CN)6。
Cu2O + K4Fe(CN)6 + H2O →K2Cu2Fe(CN)6 + 2KOH
红棕 无色
终点的确定:葡萄糖+亚甲基蓝(氧化态)→亚甲基蓝(还原态
过量 兰色 无色
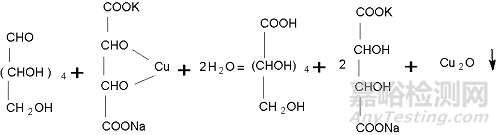
2、测定
①碱性酒石酸铜溶液的标定
(乙液(内有亚铁氰化钾)
取甲、乙液各5.00mL,加入9~9.5ml葡萄糖标准溶液(1mg/mL),△2min内沸腾,准确沸腾30s,滴至蓝色褪去,记下消耗葡萄糖V1。
F = C·V1
(F--10mL斐林试剂相当于葡萄糖质量,mg;C--葡萄糖液浓度mg/mL;V1--葡萄糖液消耗体积)
②预测: 吸取甲、乙液各5.00mL,加水10mL,2min内△至沸,准确沸腾30s,用样液滴定至蓝色褪去,记录V样液预测
③测定: 吸取甲、乙液各5.00mL,加入预测样液V少1mL样液,△,2min内沸腾,准确沸腾30s,继续滴定至蓝色褪去,记下V2
3、计算 F
还原糖 % = --------------------×100
( V2/V ) × m
F---- 10mL斐林试剂相当于葡萄糖质量,mg
V2----消耗样液的体积,ml
V----样液定溶的总体积,ml
M----样品的质量,mg
(五)高锰酸钾法测定还原糖
1、原理 (GB/T5009.7-1985)
还原糖与酒石酸合钠反应生成Cu2O↓
Cu2O + 2Fe3+ + 2H+ → 2Cu2+ + 2Fe2+ + H2O
10Fe2+ + 2MnO4- +16H+ → 10Fe3+ + 2Mn2+ + 8H2O5mol Cu2O 相当于 2mol KMnO4
由KMnO4耗量求出Cu2O量,再由Cu2O检索表得出相当的还原糖量。
2、适用范围及特点
适用于各类食品中还原糖的测定,有色样液不受限制,准确度高,重现性好,但费时,需检索表。
3、测定:吸取样液50ml于烧杯中,加费林试剂甲、乙各25mL,△,4min内沸腾,2min趁热在古氏坩埚中抽滤,60℃热水洗涤去滤液。保留Cu2O↓,将坩埚用硫酸铁溶液50mL分数次将Cu2O溶解,滤入吸滤瓶中,热水洗涤,加入20mL2 mol/L H2SO4,用KMnO4溶液滴至微红色,同时作空白试验(V0)。
4、计算
X=CMnO4-×(V-Vo) ×(5/2)×143.08(MCu2O)
A
还原糖(%)= --------------- ×100
m×V2/V1×1000
X-Cu2O量mg,A-由x查出还原糖量mg,m-样品质量g,如:x=105.8 A=46.0,
也可以参考 P89 (5-2) m1 ( A) = 0.4388x-0.4805
(六)蔗糖的测定
1、原理:蔗糖经用HCl水解,使蔗糖转化为还原糖,然后按还原糖测定方法,分别测定水解前后样液中还原糖含量,两者之差即为由蔗糖水解产生的还原糖量,乘以一个换算系数0.95即蔗糖%
2、测定:吸取样液2份各50ml,其中一份直接加入100ml容量瓶中,用水稀释至刻度。另一份加入5ml 6M HCl,置68~70℃水浴加热15min冷后加入100ml容量瓶加2滴甲基红,用20%NaOH中和至中性,加水至刻度。
然后用直接滴定法或高锰酸钾法测定还原糖含量。
3、结果计算
蔗糖(%)=(转化后还原糖%-转化前还原糖%)×0.95
0.95——蔗糖 + H2O = 葡糖 + 果糖
342 18 180 180
转化糖换成蔗糖系数=342/360 = 0.95
(七)总糖分的测定
食品中的总糖分包括还原性糖(葡、果、乳、麦芽糖)和蔗糖,反映的是可溶性单糖和低聚糖的总量,为常规分析项目
是麦乳精、糕点、果蔬罐头、饮料……质量指标。
1、原理:同蔗糖的测定
2、测定:按测定蔗糖的方法水解样品,再测定还原糖量
3、计算
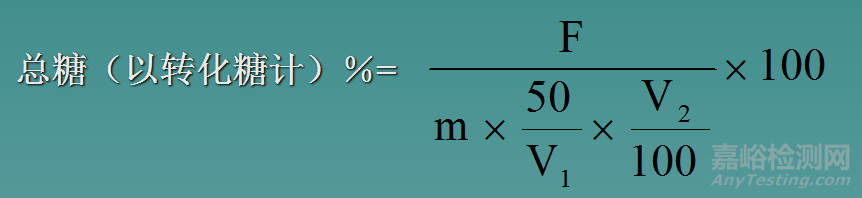
m——样品质量mg
F——10ml斐林试剂相当于葡萄糖质量,mg;
V1、V2——样品总体积、消耗样品液体积
50/100——稀释比例
(八)淀粉的测定
1、酸水解法
淀粉→盐酸水解→葡萄糖→测定还原糖
2、酶水解法
淀粉→酶水解→葡萄糖→测定还原糖
3、旋光法
(九)食物中不溶性膳食纤维的测定
1、实验原理
在中性洗涤剂的消化作用下,样品中的糖、淀粉、蛋白质、果胶等物质被溶解去,不能消化的残渣为不溶性膳食纤维,主要包括纤维素、半纤维素、木质素、角质和二氧化硅等,并包括不溶性灰分。
2、测定步骤
(1)取样1.00g,置高型无嘴烧杯中,如样品脂肪含量超过10%,需先去除脂肪,即样品1.00g,用石油醚(30-60℃)提取3次,每次10mL。
(2)加2.5%α-淀粉酶溶液20mL,于37℃(或者水浴锅)恒温箱中保温1小时。
(3)加100mL中性洗涤剂溶液,再加0.5g无水亚硫酸钠。
(4)电炉加热,5-10min内使其煮沸,移至电热板上,保持微沸1h。
(5)将耐酸玻璃滤器洗净,移至烘箱内,110℃4h,取出置干燥器中,冷至室温,称量,得m1。
(6)将煮沸后样品趁热倒入滤器中,用水泵抽滤。用500mL热水(90-100℃),分数次洗烧怀及滤器,抽滤至干。洗净滤器下部的液体和泡沫,塞上橡皮塞。
(7)于滤器中加丙酮,液面需覆盖纤维,保持5分钟,除去底部塞子,抽干,再以丙酮洗2次。
(8)将滤器置烘箱中,110℃4h,取出,置干燥器中,冷至室温,称量,得m2。
3、结果计算
m2- m1
X(%) = ———— × 100
m
式中:
X—样品中不溶性膳食纤维的含量%;
m1—滤器的质量,g;
m2—滤器及样品中纤维的质量,g;
m—样品质量,g。
(十)果胶物质的测定
常用测定方法:重量法、咔唑比色法
1、重量法原理
样品 + 70%乙醇 → 果胶↓ →
分别用乙醇、乙醚洗涤( 除糖、脂肪、色素)
→残渣→分别用水、酸提取→提取液+NaOH →
果胶酸钠+CH3COOH→果胶酸+CaCl2 →果胶酸钙↓ →烘干→称重
2、适用范围及特点:适用于各类食品,方法稳定可靠,但费时,易夹杂。
3、测定
①样品处理
A.新鲜样品
切片+无水乙醇→ 沸水浴中回流15min→过滤→残渣→分别用乙醇、乙醚洗涤→残渣
B.干燥样品
研细过筛→称样 + 70%乙醇→过滤(反复) →残渣→分别用乙醇、乙醚洗涤→残渣
②提取
A.水溶性果胶:残渣→水→沸腾1h →冷却→定容→过滤(弃去粗滤液)→水溶性果胶提取液。
B.总果胶:残渣+0.05mol/L HCl → 沸水浴中回流1h(装冷凝管)→冷却+0.05mol/LNaOH,中性红,中和→ 定容(250ml)→过滤(弃去粗滤液)→总果胶提取液。
③测定
吸取提取液25ml +0.1mol/LNaOH 100mL →搅拌、放置0.5h +1mol/L CH3COOH 50mL →放置5min + 1mol/L CaCl2 25mL →放置1h(陈化)→煮沸5min→过滤→滤渣+滤纸→干燥恒重。
4、计算
(m1-m0)× 0.9233
果胶酸(%)= —————————— ×100
m ×25/250
m0——埚+纸,m1——埚+纸+胶,m——试样,
0.9233——果胶酸/果胶酸钙系数。

来源:食品论坛


