今日头条
智康弘义ETAR拮抗剂上Ⅱ期临床。智康弘义创新小分子ETA受体拮抗剂SC0062在治疗伴有蛋白尿的慢性肾脏病(糖尿病肾脏病及IgA肾病)的Ⅱ期临床完成首例患者给药。这是一项随机、双盲、安慰剂平行对照临床研究,由浙大一院肾脏病中心主任陈江华教授担任主要研究者。在Ⅰ期临床中,SC0062已表现出良好的安全性和耐受性及药代动力学特征,同时未发现水钠潴留等副作用。
国内药讯
1.百泰EGFR单抗获批胰腺癌NDA。百泰生物开发的靶向表皮生长因子受体(EGFR)的单抗药物尼妥珠单抗(商品名:泰欣生)获国家药监局批准新适应症,联合吉西他滨用于治疗胰腺癌患者。在III期临床中,与吉西他滨相比,尼妥珠单抗联合治疗显著提高患者的总生存期(mOS:10.9个月vs8.5个月,HR=0.50,P=0.025)和无进展生存期(mPFS:4.2个月vs3.6个月,HR=0.56,P=0.013)。2008年1月,该新药已获批用于治疗鼻咽癌。
2.迪哲EGFR-TKI获批肺癌国际Ⅲ期临床。迪哲医药EGFR-TKI创新药舒沃替尼获欧盟批准开展国际Ⅲ期临床(悟空28,WU-KONG28),评估一线治疗EGFR20号外显子插入突变型晚期非小细胞肺癌(NSCLC)的有效性与安全性。近日,迪哲已在ASCO2023年会上公布该新药关键研究(悟空6,WU-KONG6)更新结果。最新数据显示,经独立影像评估委员会(IRC)确认的客观缓解率(cORR)达到60.8%。
3.泽璟JAK抑制剂髓纤Ⅲ期临床积极。泽璟制药在EHA2023年会上公布JAK抑制剂盐酸杰克替尼片治疗中、高危骨髓纤维化的Ⅲ期研究积极结果。与羟基脲组相比,杰克替尼组第24周时患者脾脏体积较基线缩小≥35%(SVR35)的患者比例更高(72.3%vs17.4%),总体症状评分减少≥50%(TSS50)的患者比例也更高(63.8%vs43.5%)。杰克替尼组≥3级治疗期不良事件(TEAE)、严重TEAE发生率均低于羟基脲。
4.信达CD47/PD-L1双抗早期临床积极。信达生物在EHA 2023年会上公布CD47/PD-L1双抗IBI322用于治疗抗PD-(L)1单抗耐药的经典型霍奇金淋巴瘤的Ⅰ期临床积极结果。数据显示,IBI322在23例患者中达到47.8%的客观缓解率(ORR)和91.3%的疾病控制率(DCR)。在7例原发性耐药患者中,ORR高达57.1%,3例患者达到完全缓解(CR)。临床中,治疗相关不良反应(TRAE)发生率为91.7%,其中≥3级TRAE发生率为41.7%。
5.石药ATM抑制剂获批实体瘤临床。石药集团中奇制药小分子新药SYH2051获国家药监局批准开展用于实体瘤治疗的临床试验。SYH2051是一款选择性ATM抑制剂,通过靶向抑制ATM蛋白激酶及其下游信号蛋白CHK2和KAP1的磷酸化,延迟DNA双链断裂修复,导致持续的DNA双链断裂和ATM介导的细胞週期阻滞,从而抑制肿瘤细胞增殖。
6.九芝堂干细胞疗法获批临床。九芝堂美科申报的1类生物制品“人骨髓间充质干细胞注射液”临床试验申请获国家药监局默示许可。这是一款通用型干细胞制剂,源自健康年轻成人供者骨髓,全程在模拟人体真实生理环境——低氧条件下培养,拟开发用于治疗自身免疫性肺泡蛋白沉积症(aPAP)。目前aPAP的标准治疗为全肺灌洗术。尚无治疗aPAP的药物获批上市。
7.上海标新口服分子胶降解剂获批临床。标新生物自主开发的口服小分子新药GT919获FDA临床批件。GT919是标新生物的首个分子胶降解剂产品,拟开发用于恶性血液肿瘤的治疗,旨在解决目前临床上来那度胺类药物的耐药性及安全性问题。2022年12月,该新药已在国内获批临床,目前正在I期临床中评估用于治疗恶性血液肿瘤的安全性、耐受性和药代动力学特征以及初步疗效。
国际药讯
1.首款OTC用ED新药获FDA批准上市。Futura Medical公司硝酸甘油透皮凝胶制剂MED3000获FDA批准上市,用于治疗勃起功能障碍(ED)。在III期FM71研究中,MED3000可在10分钟起效,并在治疗24周时,显著改善患者的勃起功能(p<0.001),其IIEF-EF评分平均提高5.73个单位。据统计,全球1/5的男性患有ED,预计到2025年患病人数将增加到3.22亿。
2.阿斯利康AKT抑制剂获优先审评资格。FDA受理阿斯利康靶向3种AKT激酶异形体(AKT1/2/3)抑制剂capivasertib的新药申请,与Faslodex联用治疗内分泌疗法经治、HR+/HER2-局部晚期或转移性乳腺癌。FDA同时授予其优先审评资格,预计今年年底完成审评。在Ⅲ期临床CAPItello-291中,这一组合降低了患者疾病进展或死亡风险达40%。
3.CRISPR体内基因编辑疗法早期临床积极。Intellia公司体内CRISPR基因编辑疗法NTLA-2002治疗遗传性血管性水肿(HAE)的Ⅰ/Ⅱ期临床结果积极。NTLA-2002通过脂质纳米颗粒(LNP)以mRNA形式递送CRISPR-Cas9基因编辑系统,靶向敲除KLKB1基因,以永久性降低血浆中激肽释放酶活性,从而防止HAE的发作。最新结果显示,单剂NTLA-2002将HAE月发作率平均降低95%。中位随访持续时间为9.0个月。
4.Menin抑制剂血癌早期临床积极。Kura Oncology公司选择性menin抑制剂ziftomenib治疗急性髓系白血病(AML)的Ⅰ/Ⅱ期临床结果积极。20例接受Ⅱ期推荐剂量(RP2D)ziftomenib治疗的NPM1突变型AML患者中有7例(35%)患者实现完全血细胞恢复的完全缓解,中位缓解持续时间为8.2个月(95% CI:1.0-NE),随访的中位时间为8.8个月。临床中有15%的患者经历1或2级不良事件,5%的患者经历3级不良事件。
5.通用型CAR-NK疗法早期临床积极。Nkarta公司在EHA2023年会上公布其同种异体、冷冻保存、靶向CD19的CAR-NK疗法NKX019治疗复发/难治性非霍奇金淋巴瘤(NHL)的Ⅰ期临床积极结果。数据显示,较高剂量水平NKX019治疗达到80%(8/10)的客观缓解率(ORR)和70%的完全缓解(CR)。临床中未观察到剂量限制性毒性、神经毒性、移植物抗宿主病(GvHD)或>3级细胞因子释放综合征(CRS)。其安全性数据支持NKX019应用于门诊治疗的潜力。
6.诺华35亿美元收购肾病药物公司Chinook。诺华宣布以35亿美元的总金额收购加拿大公司Chinook Therapeutics,并获得2款临床后期慢性肾病药物(Atrasentan和Zigakibart)。Atrasentan是一款高选择性内皮素A(ETA)受体拮抗剂,目前正在III期临床中评估用于治疗IgA肾病的有效性与安全性。Zigakibart(BION-1301)是一款抗APRIL单抗药物,目前正在I/II期临床评估治疗IgA肾病的潜力,预计将于今年年中开展III期临床。
医药热点
1.江苏立法推动基层卫生优先发展。近日,江苏省印发《江苏省基层卫生条例》,将于今年9月1日起施行。《条例》明确,政府及有关部门应采取措施,发展壮大基层医疗卫生队伍,完善农村医疗卫生人才培养机制;建立健全全科医生培养制度,推动乡村医生向执业(执业助理)医师资格转化;加大对基层医疗卫生人员的激励力度;动态调整乡村医生补助标准,提高乡村医生收入水平,对未纳入企业职工养老保险、年满六十周岁的乡村医生,采取补助等方式动态提高养老待遇。
2.贵州实施“健康敲门行动”。近日,贵州省卫健委多部门联合印发《2023年贵州省失能老年人“健康敲门行动”实施方案》,明确从今年起为12万名65岁及以上失能老年人提供免费上门健康服务。凡愿意接受上门健康服务的失能老年人,经评估后符合条件可填写《贵州省失能老年人上门健康服务申请表》,由基层医疗卫生机构家庭医生团队为其提供“三个一”免费健康服务,即开展一次上门健康管理服务,提供一套健康服务方案,开通一条健康咨询热线。
评审动态
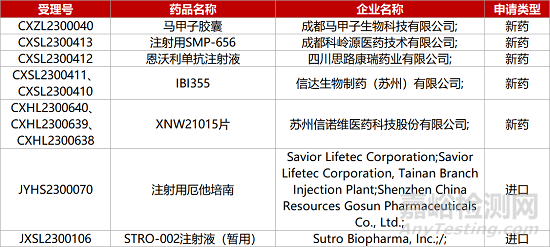
1. CDE新药受理情况(06月13日)
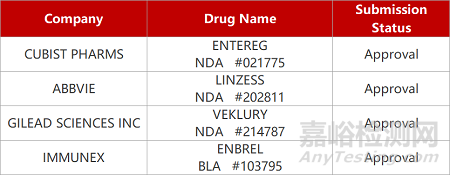
2. FDA新药获批情况(北美06月12日)