1.体系核查优先
2.审评审批优先
3.专项交流
二、申请优先审批的相关要求
符合下列情形之一的医疗器械:
(1) 诊断或者治疗罕见病,且具有明显临床优势;
(2) 诊断或者治疗恶性肿瘤,且具有明显临床优势;
(3) 诊断或者治疗老年人特有和多发疾病,且目前尚无有效诊断或者治疗手段;
(4) 专用于儿童,且具有明显临床优势;
(5) 临床急需,且在我国尚无同品种产品获准注册的医疗器械。
列入国家科技重大专项或国家重点研发计划的医疗器械。
对于其他应当优先审批的医疗器械,由国家药品监督管理局广泛听取意见,并组织专家论证后再确定是否予以优先审批。
以上所提及医疗器械均需属于境内第三类和进口第二类、第三类医疗器械。
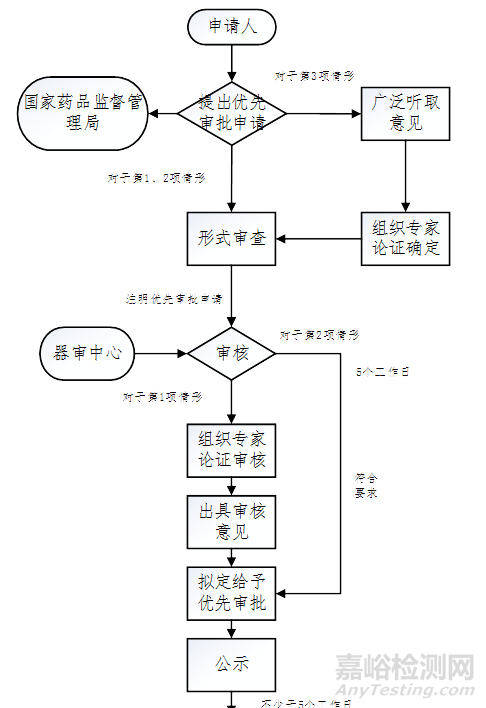
三、审批流程
四、TIPS
1.对公示项目有异议的,器审中心在收到异议起10个工作日内,对相关意见进行研究,并将研究意见告知申请人和提出异议方。
2.器审中心经审核不予优先审批的,将不予优先审批的意见和原因告知申请人,并按常规审批程序办理。
3.对于已纳入优先审评通道的医疗器械,在国家药监局、器审中心已发布实施的沟通交流机制保持不变的基础上,由器审中心定期更新产品清单并交换至分中心,分中心按照专人负责、主动对接、全程指导的工作机制,指派专人主动服务,给予指导。