您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-02-21 08:12
化学药品注册3类是指境内申请人仿制境外上市但境内未上市原研药品的药品,该药品的开发研究丰富药品类型、提高药品可及性、降低医疗支出,按照《境外已上市境内未上市药品临床技术要求》[1],注册3类药品临床试验要求需要结合原研药品临床评价结果及制剂学两个因素综合考虑;而原研药品临床评价无法保证充分性,故需开展必要的临床试验以支持仿制药用于中国患者的安全性和有效性评价;制剂学方面也需通过研究证明仿制药与原研产品质量与疗效的一致性;如何评估化学药品注册3类的临床研究是申请人面临的最大挑战,其中临床研究成本最高的化药3类品种是化药全真3类,绝大多数需要开展pK-BE和验证性临床。本文将分析化药全真3类-阿伐那非片的临床研究方案,为申请人在化药全真3类的临床研究评估方面提供思路。
1.背景信息
阿伐那非具有独特二氢嘧啶衍生结构[2],是一种高度选择性的PDE5抑制剂,用于治疗勃起功能障碍,由于其对PED5高选择性,相对其他已上市的PDE5抑制剂,副作用可能较少;原研未在中国上市,参考ICH E5[3]和《境外已上市境内未上市药品临床技术要求》,阿伐那非片需开展不同剂量安全性和有效性验证性临床研究和生物等效性试验;
已获得批件海思科制药有限公司及上海汇伦医药股份有限公司,都完成了阿伐那非片有效性和安全性验证性临床研究及生物等效性试验,临床试验登记公开信息显示阿伐那非片有效性和安全性验证性临床进行了高/低剂量组、双盲单模拟、安慰剂对照、多临床研究;生物等效性实验设计为空腹/餐后、随机、开放、200mg、两周期交叉试验;
2.阿伐那非在勃起功能障碍的中国受试者中安全性和有效性验证性临床
1)终点指标
验证性临床试验首先需确定终点指标,终点指标分为主要终点指标和次要终点指标,主要终点指标应根据实验目的选择易于量化、客观性强、变异性小、重复性高,并在相关领域已有公认标准的,并用于试验样本量的估计;
FDA原研审评报告中[4]主要终点指标为:a.治疗12周后IIEF-EF专项评分,b.勃起能插入阴道的次数占总性交次数的百分比的变化(SEP2),c.勃起能持续到完成射精的次数占总性交次数的百分比的变化(SEP3);
海思科制药有限公司选择的主要指标是IIEF-EF专项评分[5];上海汇伦医药股份有限公司选择的主要指标是IIEF-EF专项评分和SEP3;
2)样本量估计
样本量估计涉及临床研究成本,影响临床结果评价,是临床试验设计的重要步骤,需充分调研文献确定样本量估计的关键参数。阿伐那非验证性临床样本量估计的关键参数是阿伐那非和安慰剂剂组从基线到治疗12周IIEF-EF评分变化标准差和两组差异值;
FDA原研审评报告中阿伐那非原研片IIEF-EF评分变化有效性试验结果如下图所示:
图1阿伐那非原研片IIEF-EF评分变化有效性试验结果
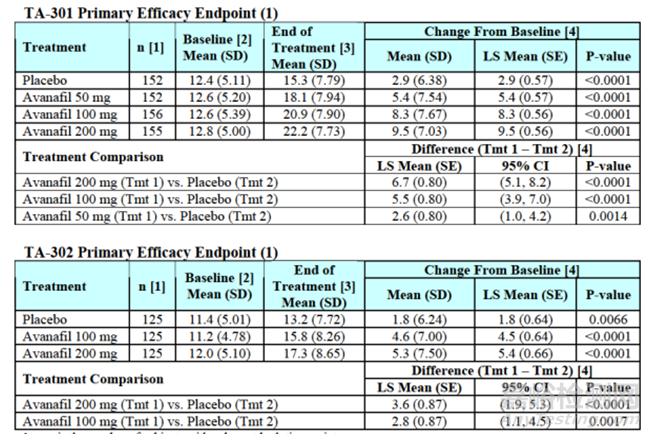
由上结果可知阿伐那非和安慰剂剂组从基线到治疗12周IIEF-EF评分变化标准差范围为6.24~7.67;阿伐那非和安慰剂剂组差异值范围为2.8~6.7;采用PASS软件对样本量进行估算,考虑20%脱落率样本量约为57~447人 ;海思科制药有限公司验证性临床样本量为216人;上海汇伦医药股份有限公司验证性临床样本量为255人;
4)安全性评估
阿伐那非安全性好,副反应与其他PDE5抑制剂相似,最常见的副反应是:头疼、脸红、鼻腔阻塞、消化不良、头昏、背疼;依据ICH E5其安全性评估在有效性临床试验中进行即可;
3.阿伐那非片生物等效性试验
阿伐那非口服后吸收迅速,Tmax约30~45分钟,终末半衰期为5h;药代动力学参数与剂量成比例,小规格可基于大规格生物等效性进行豁免;有文献[6]报道200mg阿伐那非片空腹和餐后个体内变异较小(<20%),利用PASS软件进行样本量估算,考虑20%的脱落率,空腹及餐后样本量需约40~96人;海思科制药有限公司生物等效性临床样本量为86人;上海汇伦医药股份有限公司生物等效性样本量为52人;
4.讨论
阿伐那非为PDE5抑制剂,目前国内已有多种PDE5抑制剂上市,PDE5抑制剂安全性有效性临床研究的文献信息丰富,验证性临床研究和生物等效性试验设计所需的信息均能通过调研获得,相对于临床研究文献信息少,种族敏感性未知的化学注册3类品种而言临床研究难度小,种族敏感性可从药动学是否呈线性、药效学曲线是否陡峭,治疗窗范围的宽窄,药物代谢酶基因的多态性,生物利用度大小等方面进行判定,具有种族敏感性注册3类化学药品的临床研究难度较大,一个临床桥接研究恐不能满足注册申报要求;验证性临床研究需从多个方面考虑,涉及因素复杂,具体品种还应具体分析,并与监管机构进行沟通交流确定研究方案;
[参考文献]
[1] 国家药品监督管理局药品审评中心. 境外已上市境内未上市药品临床技术要求. [EB/OL]. https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=770f8d92463893390a0f91a6307cdc24
[2] Jeffrey A. K, Dana A. B, Jerame K. H. Avanafil for Erectile Dysfunction. [J]. Annals of pharmacotherapy 47(10): 1312-1320
[3] ICH. ICH E5 Ethnic Factors. [EB/OL]. https://database.ich.org/sites/default/files/E5_R1__Guideline.pdf
[4] FDA.STENDRA( Avanafil) MEDICAL REVIEW(S). [EB/OL]. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2012/202276Orig1s000MedR.pdf
[5] Hui Jiang, Haocheng Lin, Fubiao Li, et al. Efficacy and Safety of Avanafil in Chinese Subjects With Erectile Dysfunction : A Multi-Center, Randomized, Double-Blinded, Placebo-Controlled Phase III Clinical Trial. [J]. Sexual Medicine 9(3): 100337, 2021
[6] Xiuhua Ren, Hengyi Yu, Xingxing Qi, et al. A Bioequivalence Study of Avanafil in Healthy Chinese Male Subjects Under Fasting and Fed Condition: Results of a Randomized, Open-Label, Single-Dose, 2-Sequence, 2-Period Crossover Study. [J]. Clinicla Pharmacology in Drug Development 10(12): 1495-1502, 2021

来源:药事纵横


