您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2018-03-22 09:59
医疗器械灭菌参数检测要求及意义
作者:张流波 中国疾病预防控制中心环境与健康相关产品安全所消毒检测中心主任,研究员
张教授首先解说了规范中两个重要的灭菌参数:1.规范中对灭菌时间的要求是最短灭菌时间,例如:预真式灭菌器132℃或134℃需至少达到4分钟,其中一分钟是蒸汽穿透时间,另外3分钟是有效灭菌时间。 2.新规范中对压力这个灭菌参数增加了个范围,压力是影响温度的一个参数,同时也是影响蒸汽是否饱和的重要指标。
接下来举例说明了我国国内面临着压力蒸汽灭菌器灭菌参数严重不合格的问题。同时指出这也是为什么在新规范中增加了对灭菌参数相关的要求。
WS310-2016 增加灭菌参数相关要求
WS310.1-2016、4.1.6 c)应与器械供应商签订协议,要求其做到:1)提供植入物与外来医疗器械的说明书(内容应包括清洗、消毒、包装、灭菌方法与参数);
WS310.2-2016、4.7 应遵循器械供应商提供的外来医疗器械与植入物的清洗、消毒、包装、灭菌方法和参数。
4.4.1.6 使用特定的灭菌程序灭菌时,应使用相应的指示物进行监测
4.4.1.8 灭菌外来医疗器械、植入物、硬质容器、超大超重包,应遵循厂家提供的灭菌参数,首次灭菌时对灭菌参数和有效性进行测试,并进行湿包检查。
4.1.5 b) 压力蒸汽灭菌器应每年对灭菌程序的温度、压力和时间进行检测;
4.4.2.1.2 定期监测:应每年用温度压力检测仪监测温度、压力和时间等参数,检测仪探头放置于最难灭菌部位。
新标准增加的灭菌质量体系----灭菌参数:
遵循厂家说明书------根据厂家灭菌参数灭菌
特定灭菌程序灭菌监测-----根据灭菌参数选择指示物
外来器械首次灭菌-----检测灭菌参数
每年检测灭菌器------检测灭菌参数
特定灭菌程序使用相应指示物监测
张教授还专门对特定灭菌程序使用相应指示物进行了解读:对于复杂的医疗器械和一些管腔器械进行化学和生物监测时,需要专门的PCD(包括管腔PCD)和六类化学指示卡。对于一些特定的灭菌程序,比如延长了灭菌时间,提高了灭菌温度,如果不能保证原有的指示物能放到最难灭菌部位,原有的指示物就失去了监测的意义,要用延时卡和PCD进行监测。
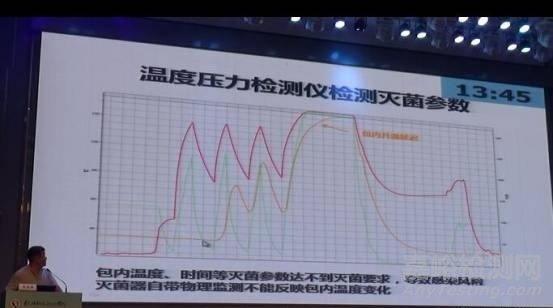
包内灭菌参数延迟的风险
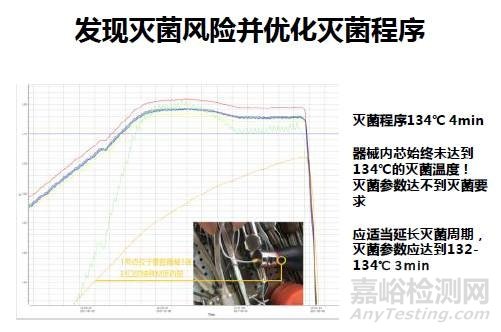
讲到外来器械首次灭菌对灭菌参数进行测试的时候,张教授举了一个案例:
一组器械,温度探头放置在最难灭菌部位,测试结果显示在灭菌阶段温度一直没有达到灭菌设定温度,灭菌时间自然也没到。这也是为什么要把温压仪探头放到最难灭菌部位检测的原因。
关于灭菌参数的检测要求:
1)谁来检测:
灭菌器定期检测:标准里面没有规定由谁来做。就是医院、官方和第三方实验室、生产厂家和设备供应商都可以检测,如果医院自己做,不需要CNAS认证,因为这就是医院自己本身生产活动的一部分。
外来器械灭菌参数检测:操作层面,只能医院自己做。
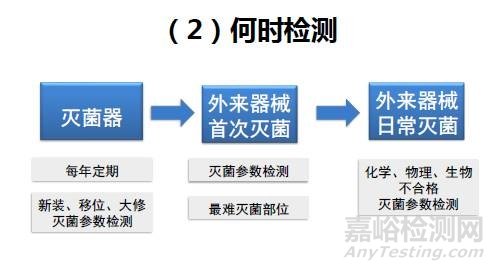
2)何时检测
对于灭菌器每年定期做,新装、移位、大修后也需要对灭菌参数进行检测。
外来器械首次灭菌时,对灭菌参数进行检测。温度探头放最难灭菌部位。
外来器械日常灭菌时主要是看化学指示物、物理打印条、生物指示物是否合格就行。
3)检测什么
温度、压力、时间;必要时进行化学指示物和生物指示物的监测。
4)如何检测
参照GB8599布点进行检测
检测仪探头放置于最难灭菌部位。
5)用什么检测
经过计量认证,符合国家标准,多点多因素无线测定仪
医疗器械灭菌参数检测的意义
从传统的监测手段到现代化的检测手段,学习欧洲,与欧洲的监测水平更接近了
不受预真空、升温和干燥阶段干扰
解决理论上的监测盲点(实现最难灭菌部位的监测)
灭菌保障水平“质”的提高,达到定量呈现数据的水平。医疗器械进行灭菌参数检测,代表着传统的定性监测技术发展到了现代化定量的检测技术。
降低手术感染风险




来源:AnyTesting


