新发布的医疗器械标准情况
您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2018-08-13 17:47
疗器械监管动态
2018年上半年国家食品药品监督管理局共发布医疗器械监管工作相关文件5项。

新发布的医疗器械标准情况
2018年上半年国家药品监督管理局批准发布医疗器械行业标准的公告3期,共有31个标准,其中与体外诊断行业有关的共22个,分别为:
(1)总局关于批准发布YY/T 0588—2017《流式细胞仪》等6项医疗器械行业标准的公告(2017年第151号),标准自2018年12月1日起实施,标准编号、名称如下:
1、YY/T 0588—2017 《流式细胞仪》;
2、YY/T 1585—2017 《25-羟基维生素D测定试剂盒(标记免疫分析法)》;
3、YY/T 1591—2017 《人类EGFR基因突变检测试剂盒》;
4、YY/T 1595—2017 《氯胺酮检测试剂盒(胶体金法)》;
5、YY/T 1596—2017 《甲型流感病毒核酸检测试剂盒(荧光PCR法)》;
6、YY/T 1597—2017 《新生儿苯丙氨酸测定试剂盒》。
(2)总局关于批准发布YY 0285.5-2018《血管内导管一次性使用无菌导管第5部分:套针外周导管》等16项医疗器械行业标准的公告(2018年第27号)。标准自2019年3月1日起实施,标准编号、名称如下:
1、YY 0285.5—2018《血管内导管一次性使用无菌导管第5部分:套针外周导管》;
2、YY/T 0528—2018《牙科学金属材料腐蚀试验方法》;
3、YY/T 1578—2018《糖化白蛋白测定试剂盒(酶法)》;
4、YY/T 1579—2018《体外诊断医疗器械体外诊断试剂稳定性评价》;
5、 YY/T 1580—2018《肌酸激酶MB同工酶测定试剂盒(免疫抑制法)》;
6、YY/T 1581—2018《过敏原特异性IgE抗体检测试剂盒》;
7、YY/T 1582—2018《胶体金免疫层析分析仪》;
8、YY/T 1583—2018《叶酸测定试剂盒(化学发光免疫分析法)》;
9、YY/T 1584—2018《视黄醇结合蛋白测定试剂盒(免疫比浊法)》;
10、YY/T 1586—2018《肿瘤个体化治疗相关基因突变检测试剂盒(荧光PCR法)》;
11、YY/T 1588—2018《降钙素原测定试剂盒》;
12、YY/T 1590—2018《心型脂肪酸结合蛋白测定试剂盒(免疫比浊法)》;
13、YY/T 1592—2018《ABO正定型和RhD血型定型检测卡(柱凝集法)》;
14、YY/T 1593—2018《 生长激素测定试剂盒》;
15、 YY/T 1599—2018《牙科学聚合物基修复材料聚合收缩测试方法激光测距法》;
16、YY/T 1605—2018《糖化血红蛋白测定试剂盒(胶乳免疫比浊法)》.
技术审评
新发布的二类医疗器械技术审查指导原则情况
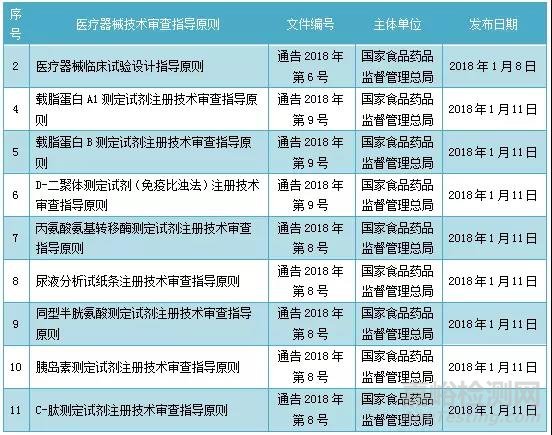
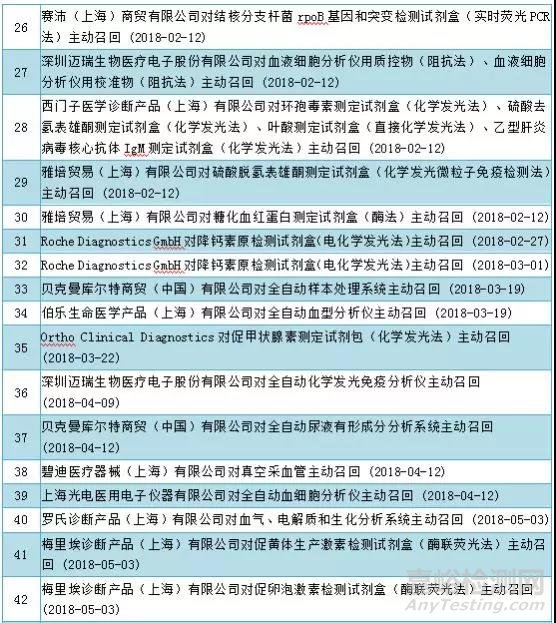
国家局发布的召回信息
2018年上半年,国家局共发布336个产品批次的召回信息。

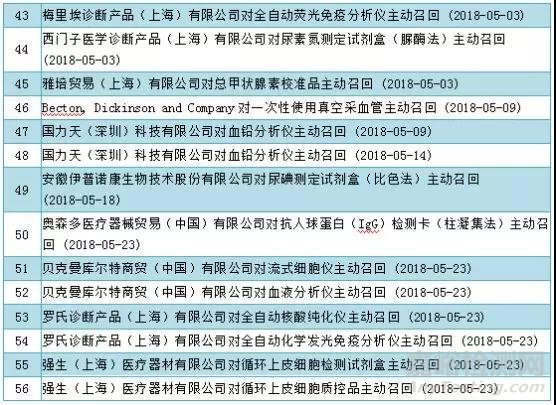

来源:AnyTesting


