您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-03-12 09:25
医疗器械产品设计开发控制和管理
引言:
医疗器械产品的设计开发过程是需要进行质量控制的重要环节,无论是标准还是法规都对产品的设计开发有要求,设计开发过程的各个阶段所进行的活动需要按要求进行。对设计开发过程进行有效的控制,可以减少工作的反复次数、提高研发效率、保证产品可行性。在进行产品注册的现场检查时,研发过程是重点关注的环节。
一、标准和法规依据
1)YY/T 0287-2017《医疗器械 质量管理体系 用于法规的要求》
7.3 设计和开发
2)ISO 13485:2016《Medical devices — Quality management systems — Requirements for regulatory purposes》
7.3 Design and development
3)国药局公告2014年第64号《生产质量管理规范》
第六章 设计开发
4)FDA Quality System Regulation
21 CFR Part 820.30 Design Controls
二、设计开发过程各阶段的活动
简述
设计开发过程应包括:设计开发策划、设计开发输入、设计开发输出、设计开发转换、设计开发验证、设计开发确认、设计开发评审、设计开发更改,应形成和保留设计开发文档。
研发过程各阶段的活动
注:1、在适宜阶段应进行相应的评审。
2、对设计更改应按要求进行控制。
三、设计开发过程控制和管理要点
对医疗器械设计开发过程的控制和管理有以下几个要点。
合规性
合规性是医疗器械产品设计开发活动的重中之重。要把产品所涉及的法规和标准要求考虑全面,如:医疗器械分类规则、医疗器械命名规则、注册申报资料要求、产品注册技术审查指导原则、技术要求编写指导原则、说明书和标签管理规定、质量管理体系要求、风险管理要求、生物学评价要求、确定产品性能指标所依据的资料、临床试验要求,等。
应及时收集法规和标准并进行分析,需要时,做相应的更新和调整,以使设计开发符合法规的要求。
统筹安排
在医疗器械产品设计开发活动中,有些项目需要的时间较长,有些项目需要的样品较多,有些样品可以流转以供几个项目使用,应提前列出清单,统筹进行安排,以减少样品量降低成本和缩短设计开发时间周期。尤其是生物学相容性试验、疲劳试验、磨损试验、特殊过程确认,等。
资源配置
资源配置也是医疗器械产品设计开发活动的要点,在设计开发策划阶段应对所需资源进行识别并进行配置,尤其是人员、生产设备和检验设备、生产环境等,以避免工作的反复或项目停滞、甚或半途而废。
进度控制
在医疗器械产品设计开发活动中,进度控制也比较重要,由于医疗器械产品设计开发周期较长,涉及到的内外部协作部门较多,可能出现的不确定因素和干扰因素就会多,制定计划时应考虑周全,实施时应不断进行跟踪和分析,采取有效措施使设计开发进度按预定计划进行。
人员能力
需重视对研发人员能力的培养和提升。在企业中,人是最重要的资源,研发人员的能力培养和提升是保障企业不断创新、产品研发续航的关键因素,进而能够使企业在市场上保持竞争优势。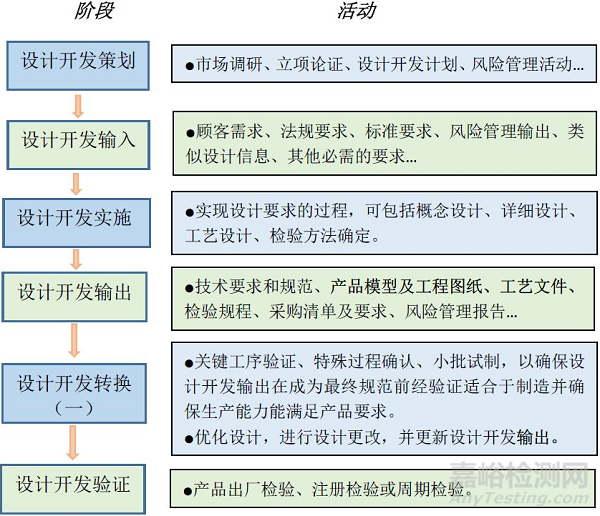


来源:索莉Not4Today


