您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-06-23 09:48
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:15条资讯,阅读时长约:3分钟 」
今日头条
安进骨质疏松症药物普罗力在华获批。安进普罗力®(地舒单抗,denosumab)获国家药监局批准,用于骨折高风险的绝经后妇女的骨质疏松症治疗。普罗力®是中国首个,也是目前唯一一个用于骨质疏松症治疗的抗RANKL单抗类药物。在一项III期临床中,绝经后骨质疏松症患者在为期3年的试验期及后续长达7年中持续使用普罗力®,腰椎和全髋的骨密度与基准线相比平均增加21.7%和9.2%,有效降低了椎体、非椎体和髋部骨折的风险。
国内药讯
1.海西新药创制枸橼酸莫沙必利片首家过评。福建海西新药创制4类仿制药枸橼酸莫沙必利片获国家药监局批准生产,视同通过一致性评价,为国内首家。枸橼酸莫沙必利属于高选择性5-HT4受体激动剂,临床上可用于功能性消化不良、食管反流、胃轻瘫、便秘、胶囊镜等。2019年中国公立医疗机构终端枸橼酸莫沙必利片销售额为7.04亿元,在胃动力药产品竞争格局中排位第一。
2.科兴生物四价流感病毒裂解疫苗获批。科兴生物四价流感病毒裂解疫苗获国家药监局批准上市,成为该品种国内第6家获批的产品。2018年6月8日以来,国家药监局陆续批准了长春长生、华兰生物、金迪克生物、长春生物、武汉生物制品共5家企业的四价流感病毒裂解疫苗上市。流感主要由甲(A)型和乙(B)型流感病毒引起,由于病毒经常发生抗原变异,传染性大,传播迅速,极易发生大范围流行。目前,接种流感疫苗仍是预防流感疾病及大爆发的最有效的措施。
3.罗氏TIGIT抑制剂新的临床申请获受理。罗氏在研TIGIT抑制剂tiragolumab的一项新的临床申请获CDE受理。值得一提的是,这是本月该新药在华递交的第四项临床申请。TIGIT是继CTLA-4、PD-1之后新兴的免疫检查点抑制剂之一,全球尚无针对该靶点的药物获批,罗氏的tiragolumab是全球研究进展最快的一款TIGIT抗体。在中国,信达生物旗下的IBI939是首个获批临床的TIGIT抗体,不久前其Ⅰ期临床研究完成首例患者给药。
4.中国又一款新冠病毒疫苗进入Ⅱ期临床。中国医学科学院医学生物学研究所自主研制的新型冠状病毒灭活疫苗于6月20日在云南省红河州进入Ⅱ期临床试验。该研究将在健康人群中评估疫苗接种的免疫原性和安全性,并确定免疫程序和免疫剂量。据科技部、国家卫健委6月19日通报,我国已在5条技术路线共布局了12项疫苗研发项目。目前,已对1个腺病毒载体疫苗和4个灭活疫苗开展了临床试验,占全世界开展临床试验疫苗总数的4成。
5.亚盛医药与阿斯利康达成研发合作。亚盛医药Bcl-2选择性抑制剂APG-2575与阿斯利康血液研发卓越中心的BTK抑制剂Calquence,拟联合开展一项Ⅰb/Ⅱ期剂量疗效探索研究,评估APG-2575单药或者联合Calquence治疗复发难治慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者的安全性、耐受性,并初步评估有效性。该试验计划在美国、欧洲、澳大利亚多地展开,目前已在美国完成首例患者给药。这是亚盛医药首次与全球性大药企开展临床合作。
国际药讯
1.法维拉韦治疗新冠肺炎在印度获批。印度药监机构加速批准Glenmark公司抗病毒药物法维拉韦(FabiFlu)上市,用于治疗轻中度COVID-19患者。这是印度批准的首个新冠肺炎治疗药物。FabiFlu的推荐剂量是第1天1800mg(每日2次),第2-14天800mg(每日2次)。2月16日,海正药业也发布公告,宣布收到国家药监局批准法维拉韦片用于治疗成人流感(仅限于其它抗流感病毒药物治疗无效或效果不佳时使用)的《药品注册批件》,以及法维拉韦片用于新冠病毒肺炎临床试验的《药物临床试验批件》。
2.瑞德西韦仿制药在印度获批。印度药物管理总局(DCGI)加速批准两家本土制药公司——西普拉(Cipla)和熙德隆(Hetero)开发的两款瑞德西韦仿制药,用于治疗疑似或实验室确诊为COVID-19、有严重疾病症状的住院成人和儿童患者。西普拉和熙德隆的产品均为100mg小瓶装注射剂,必须在医院由医疗保健医生监督通过静脉注射给药。其中,西普拉的产品商品名为Cipremi,定价每剂3000-4000卢比(约合39-52美元)。熙德隆的产品商品名为Covifor,定价每剂5000-6000卢比(约合65-78美元)。
3.罗氏Akt抑制剂治疗特定前列腺癌结果积极。罗氏PI3/Akt抑制剂ipatasertib治疗转移性去势抵抗性前列腺癌的Ⅲ期临床IPATential150达到共同主要终点中的一个主要终点。在携带PTEN抑癌基因缺失的患者中,ipatasertib与阿比特龙和prednisone/prednisolone联用,与活性对照相比,显著提高患者的放射学无进展生存期,总生存期数据尚未成熟。在治疗整体患者群时,ipatasertib组合疗法与活性对照组相比,未提供显著获益。目前试验正在进行中,详细数据将于医学会议上公布。
4.Finch微生物组疗法Ⅱ期临床结果积极。Finch Therapeutics公司开发的研究性口服微生物组药物CP101,在预防复发性艰难梭菌感染(CDI)的Ⅱ期临床PRISM3中达主要疗效终点。接受CP101单次给药的复发性CDI患者中74.5%在第8周达到了持续的临床治愈,与对照组患者的61.5%相比,改善具有统计学意义(p<0.05); CP101在研究中耐受性良好,无治疗相关严重不良事件。这是这类疗法首次在关键性临床试验中获得积极结果。
5.uniQure公布B型血友病基因疗法临床进展。uniQure公司在WFH2020年会上公布其基于AAV5载体递送表达凝血因子IX转基因的基因疗法etranacogene dezaparvovec,治疗B型血友病的ⅡB期临床积极结果。在这项试验中,中位凝血因子IX活性水平在接受治疗6周后达到正常水平的31%,在36周时达到正常水平的45%。接受治疗的患者没有出现出血事件,而且不需要接受凝血因子替代疗法。目前,该公司已完成这一基因疗法Ⅲ期临床的患者给药,试验结果预计今年年底之前获得。该公司计划于2021年递交其上市申请。
6.葛兰素史克与IDEAYA达成研发合作。IDEAYA Biosciences与葛兰素史克拟在“合成致死”创新靶点肿瘤研究领域达成战略合作协议。合作将包含IDEAYA公司的三个“合成致死”研发项目(靶向MAT2A、Polθ和Werner解旋酶)。其MAT2A和Polθ项目已在动物模型中获得了体内概念验证。根据协议,IDEAYA将主导MAT2A项目的早期临床开发,负责在GSK行使选择权之前MAT2A项目的所有费用。此后,IDEAYA将承担20%的全球开发成本。双方还将探索IDEAYA研发项目和GSK研发项目之间的组合。IDEAYA将获得1亿美元的前期现金付款,2000万美元的股权投资,以及潜在的临床前、临床期和销售里程碑付款。
医药热点
1.北京核酸检测能力达23万份/日。在21日下午召开的北京市新冠病毒肺炎疫情防控工作新闻发布会上,北京市卫健委新闻发言人高小俊表示,新发地批发市场发生疫情后,北京市迅速提升核酸检测能力,截至6月20日,核酸检测机构从98所扩至124所,日最大检测能力从10万份提升到23万份以上。124所机构中,疾病预防控制中心有20所,二、三级医院有73所,医学检验实验室有31个。如采用5:1混检,每日可检测近100万人。
2.北京协和医院建成新冠核酸采样方舱。开展大规模核酸检测是精准防控的前提和有效手段。为满足短期内集中完成大规模采样的应急需要,北京协和医院新冠核酸采样方舱项目经过三个昼夜的鏖战,于6月21日晚在协和医院急诊北广场东侧建成。6月22日,方舱正式投入使用。方舱内设有8间采样室、4间开单室和2间综合服务室,规范区分了患者人流,将提升医院的新冠核酸采样能力。
3.德国肉联厂新冠聚集性感染人数升至1331人。德国西部北莱茵-威斯特法伦州(北威州)居特斯洛县一家肉联厂近日发生新冠聚集性疫情,截至21日下午,6139名员工完成核酸检测,确诊感染人数上升至1331人,其中5人处于重症监护中。居特斯洛县20日要求肉联厂停产14天,以避免病毒进一步传播。德国疾控机构罗伯特·科赫研究所21日公布的疫情数据显示,截至当日零时,德国累计确诊病例为189822例,较前一日增加687例;累计死亡病例修正为8882例。
股市资讯
审评动向
2. FDA最新获批情况(北美06月19日)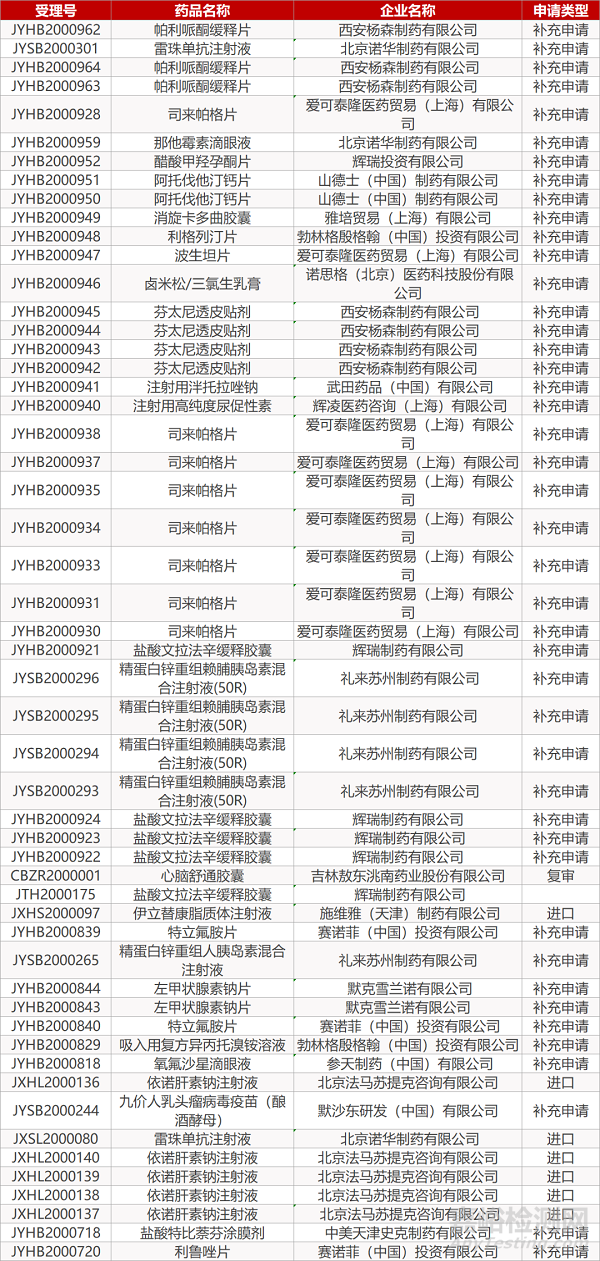
暂无
- The End -

来源:药研发


