您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-10-16 11:32
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
首款埃博拉疗法获FDA批准。FDA批准再生元(Regeneron)公司开发的中和抗体鸡尾酒疗法Inmazeb(atoltivimab、maftivimab和odesivimab-ebgn)上市,治疗成人和儿童埃博拉病毒感染。这是FDA批准的首个治疗埃博拉病毒感染的药物。在一项PALM试验中,Inmazeb治疗与对照治疗相比降低了患者的死亡率,治疗28天后两组的死亡率分别为33.8%和51%。再生元利用同样方法开发的新冠中和抗体鸡尾酒疗法REGN-COV2目前已向FDA递交了紧急使用授权申请。
国内药讯
1.百美特生物醋酸钙片首家通过一致性评价。百美特生物醋酸钙片获国家药监局批准通过一致性评价。醋酸钙片是一种磷结合剂,主要用于预防和治疗终末期肾病高磷血症。国内获批生产销售醋酸钙片的厂家有邦宇制药、赛立克药业、邦宇制药等6家,此前尚未有企业通过一致性评价。除百美特生物外,正在申请或视同申请该药一致性评价的厂家还有5家。
2.贝克生物恩曲他滨替诺福韦片即将获批。贝克生物4类仿制药恩曲他滨替诺福韦片进入行政审批阶段,即将于近期获批上市。恩曲他滨替诺福韦片(Truvada)原研厂家为吉利德,最早在2004年8月被FDA批准上市,联合其他抗逆转录病毒药物治疗HIV-1感染,2012年被FDA批准用于预防性传播导致的成人获得性HIV-1感染,是全球首个HIV预防药物。2019年Truvada全球销售额超过28亿美元。目前国内市场恩曲他滨替诺福韦片获批企业仅有吉利德和正大天晴。
3.百奥泰巴替非班注射液申报上市。百奥泰1类新药巴替非班注射液用于PCI围术期抗血栓的上市申请获CDE受理。巴替非班是一种人工合成的血小板糖蛋白IIb/IIIa(即GPIIb/IIIa)受体拮抗剂,可特异性地结合GPIIb/IIIa受体,能通过阻止纤维蛋白原、VonWillebrand因子和其它粘附配体与GPIIb/IIIa的结合来抑制血小板聚集。根据弗若斯特沙利文数据,2019年中国PCI手术85万台,国内已有替罗非班等IIb/IIIa受体拮抗剂上市,2018年替罗非班的市场规模约为2亿元。
4.康希诺新冠疫苗在墨西哥启动III期临床。陈薇院士团队与康希诺生物合作研发的重组新冠疫苗Ad5-nCoV国际III期临床在墨西哥取得进展。墨西哥公司EPIC RESERCH S de RL de CV将协助在当地开展新冠疫苗III期临床试验。同时,墨西哥与康希诺生物签署框架协议,向康希诺生物采购3500万剂新冠疫苗。目前Ad5-nCoV正在俄罗斯和巴基斯坦开展国际III期临床试验。这款新冠疫苗预计最早12月上市。
5.百利药业1类新药GNC-039申报临床。百利药业四特异性抗体GNC-039注射液的临床试验申请获CDE受理。这是百利药业申报临床的第二款四特异性抗体。今年9月,百利药业GNC-038四特异性抗体注射液在中国获得一项临床默示许可,拟用于治疗复发或难治性非霍奇金淋巴瘤(R/R NHL)、复发或难治性急性淋巴细胞白血病(R/R ALL)、难治性或转移性实体瘤。据悉,GNC-038是全球首个成功获批临床的四特异性抗体。
6.阿斯利康/安进“first-in-class”新药在华申报临床。阿斯利康与安进联合开发的tezepelumab注射液的临床试验申请获国家药监局受理。Tezepelumab是一款TSLP抑制剂,拟开发用于哮喘、特应性皮炎等疾病治疗。根据中国药物临床试验登记与信息公示平台, tezepelumab目前正在中国开展2项临床试验, tezepelumab用于治疗重度哮喘控制不佳受试者的国际多中心Ⅲ期临床;在健康受试者中单剂量皮下注射的药代动力学、安全性、耐受性和免疫原性研究。
国际药讯
1.发作性睡病治疗药物Wakix新适应症获FDA批准。FDA批准Harmony Biosciences公司神经系统疾病首创药物Wakix(pitolisant)新适应症,用于治疗发作性睡病成人患者的猝倒。值得一提的是,Wakix是FDA批准的首个也是唯一一个没有被美国禁毒局(DEA)列入管制分配的用于治疗与发作性睡病相关的白天过度嗜睡或猝倒的药物。在美国,Wakix已于2019年首次获批,用于治疗发作性睡病成人患者的白天过度嗜睡。
2.Biohaven偏头痛治疗药物在美申报新适应症。FDA受理Biohaven公司为Nurtec ODT提交的预防性治疗偏头痛的补充新药申请,预计在明年第2季度做出回复。Nurtec(rimegepant)是一款CGRP受体抑制剂,此前获FDA批准用于成人偏头痛的急性治疗。在一项针对偏头痛患者的关键性偏头痛预防治疗试验(研究305)中, Nurtec治疗显著减少患者每月偏头痛天数,Nurtec组患者每月偏头痛发作天数较基线减少4.3天,而安慰剂组减少3.5天(p<0.05)。
3.拜耳copanlisib组合疗法治疗NHL达Ⅲ期终点。拜耳PI3K抑制剂copanlisib联合利妥昔单抗(rituximab)治疗复发性无痛性非霍奇金淋巴瘤(NHL)的Ⅲ期临床CHRONOS-3获积极结果。该试验患者的组织学亚型包括滤泡性淋巴瘤(FL)、边缘区淋巴瘤(MZL)、小淋巴细胞淋巴瘤(SLL)和淋巴浆细胞样淋巴瘤/瓦尔登斯特伦巨球蛋白血症(LPL/WM)。分析结果显示,该组合疗法达到显著延长无进展生存期的主要终点;安全性结果与已知研究一致,没有发现新的安全信号。
4.创新细胞疗法获FDA再生医学高级疗法认定。Orca Bio公司细胞疗法Orca-T获FDA授予再生医学高级疗法认定(RMAT)。Orca-T是一种在研同种异体、高精度细胞疗法,适用于适合造血干细胞移植的血液癌症患者。此外,Orca-T还获得了FDA授予的孤儿药资格,用于增强造血干细胞移植手术的细胞定植。这款创新疗法正在进行的临床数据预计在今年第62届美国血液学会年会上公布。
5.罗氏与Dyno公司达成一项研发合作。Dyno Therapeutics将利用其基于AI技术设计新型衣壳的CapsidMap平台开发新一代腺相关病毒(AAV)载体,用于为罗氏和旗下Spark 公司的研发管线开发治疗中枢神经系统(CNS)疾病的基因疗法和肝脏定向递送的疗法。根据协议,Dyno将负责设计能够改善基因疗法功能特征的新型AAV衣壳,而罗氏和Spark Therapeutics将负责使用新型衣壳开展候选基因疗法的临床前/临床研究和推广活动。Dyno将获得的未来里程碑付款总计可能超过18亿美元。
医药热点
1.世行提供120亿美元为发展中国家抗“疫”。据彭博消息,世界银行批准120亿美元,用于资助发展中国家购买和分发新冠疫苗,以及为其公民安排检测和治疗。今年4月,鉴于新冠疫情带来的空前挑战,世界银行预计将在未来15个月调配1600亿美元的资金,帮助各国保护贫困弱势群体,支持企业,促进经济复苏。上述120亿美元是其中的一部分,将为世界银行的紧急卫生响应项目增加资金,该项目现已覆盖111个国家。
2.疫苗责任强制险管理办法公开征求意见。国家药监局网站消息,近日,国家药监局会同国家卫健委、银保监会组织起草了《疫苗责任强制保险管理办法(征求意见稿)》,现向社会公开征求意见。《征求意见稿》指出, 免疫规划疫苗和非免疫规划疫苗责任强制保险在全国范围内实行统一最低责任限额。死亡赔偿金每人不低于50万元,伤残赔偿金根据伤残鉴定机构出具的伤残程度鉴定书确定。
3.北京市对入境进京人员实行3次核酸检测。北京市新冠病毒肺炎疫情防控工作领导小组10月14日下午召开新闻发布会。疫情防控工作组成员田涛介绍,目前北京市对入境进京人员实行3次核酸检测。一是在境外远端实施核酸检测等健康筛查措施,持5天内核酸检测阴性证明才可以登机;二是在入境通关时海关进行健康申报和核酸检测;三是集中观察期满再进行一次核酸检测,结果为阴性的方可按程序解除集中观察。
股市资讯
【欧普康视】公司在研产品“硬性接触镜润滑液”通过伦理会审查,并完成在安徽省药监局备案,已可开展临床试验。具体为:评价硬性接触镜润滑液有效性和安全性的随机、平行对照临床试验。本产品适用于对硬性接触镜的湿润处理,配戴硬性接触镜时滴入眼内起润滑作用。
【天坛生物】公司所属成都蓉生收到蒙古国卫生部签发的规格为1ml 100IU/瓶和2ml 200IU/瓶的乙型肝炎人免疫球蛋白注册证书,本品主要用于乙型肝炎预防。
【中源协和】公司与中国科学院大学签署协议,继续沿用“中源协和生命医学奖”冠名承办该奖项,并出资每年不超过人民币400万元支持。
审评动向
1. CDE最新受理情况(10月15日)
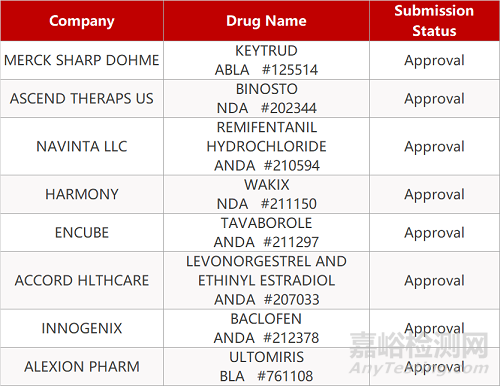
2. FDA最新获批情况(北美10月14日)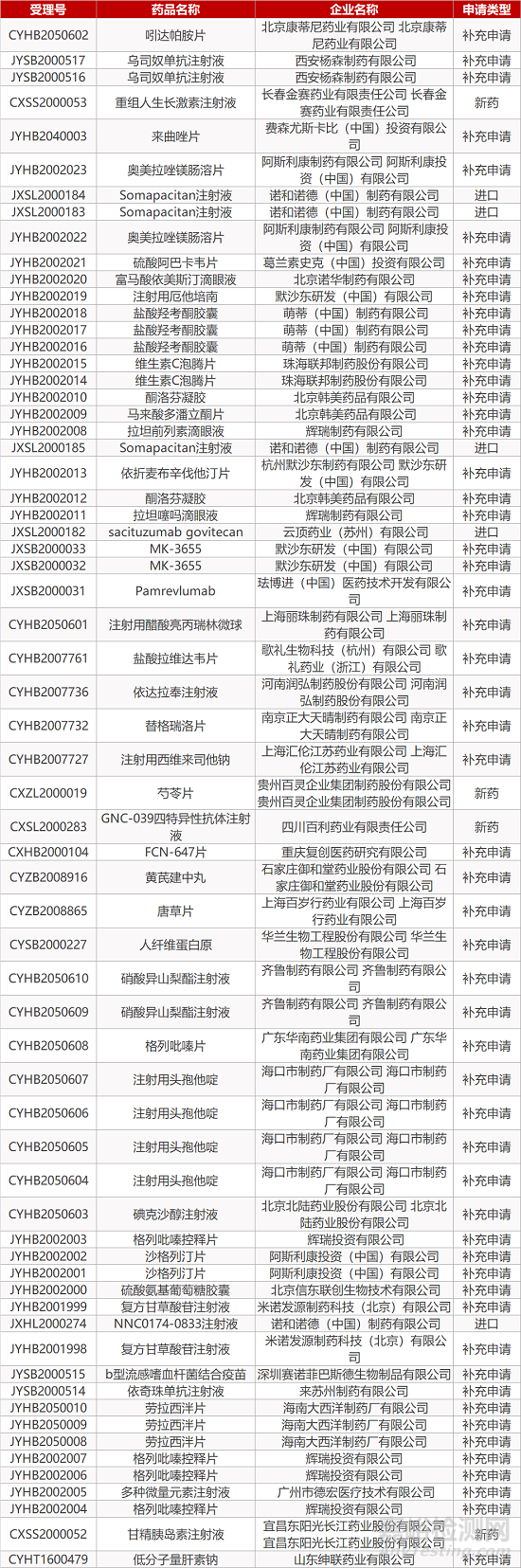
- The End -

来源:药研发


