您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-25 11:24
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
石药DPP-4抑制剂糖尿病Ⅲ期临床积极。石药集团中奇制药DPP-4抑制剂普卢格列汀片治疗2型糖尿病的两项关键Ⅲ期临床均达到主要终点。单药试验结果显示,DBPR108治疗较安慰剂,显著改善患者第24周末糖化血红蛋白(HbA1c)较基线变化,同时非劣于阳性药磷酸西格列汀片组。联合试验结果显示,DBPR108联合二甲双胍对比安慰剂组联合二甲双胍,显著改善患者24周末HbA1c较基线变化。药物的安全性数据与西格列汀和安慰剂相似。石药集团计划向NMPA提交上市前沟通交流的申请。
国内药讯
1.百济神州PD-1单抗新适应症报产。百济神州PD-1替雷利珠单抗(百泽安)新适应症上市申请获国家药监局受理,推测该项适应症为:联合化疗一线治疗晚期或转移性食管鳞状细胞癌(ESCC)患者。在国际Ⅲ期临床RATIONALE 306中,替雷利珠单抗联合化疗使患者死亡风险降低34%,中位OS达到17.2个月(vs10.6个月),无论患者PD-L1表达如何,均观察到联合治疗的OS获益。这也是该产品在国内申报上市的第11项适应症。
2.齐鲁中美双报双抗启动宫颈癌III期临床。齐鲁制药PD-1/CTLA-4双抗QL1706注射液登记启动一项III期临床,评估联合紫杉醇-顺铂/卡铂加或不加贝伐珠单抗用于一线治疗复发或转移性宫颈癌(登记号:CTR20222087)的有效性和安全性,目标入组人数为498人。齐鲁制药目前正在中美两国同步临床开发QL1706,涉及的适应症还包括广泛期小细胞肺癌、结直肠癌和晚期肝细胞癌等。
3.百奥泰Trop2靶向ADC获批临床。百奥泰Trop2靶向抗体药物偶联物(ADC)注射用BAT8008获国家药监局临床试验默示许可,拟用于实体肿瘤的治疗。Trop2通常高表达在多种肿瘤组织(包括乳腺癌、宫颈癌、结直肠癌、食管癌、胃癌、肺癌等),与肿瘤的侵袭和预后相关。肿瘤组织和正常组织中表达水平的差异使得Trop2成为ADC药物的热门靶点。BAT8008是百奥泰自主研发的第4个ADC产品获批进入临床。
4.艾滋病三合一复方拟纳入优先审评。晖致医药依非韦伦拉米夫定替诺福韦片的5.1类新药获CDE拟纳入优先审评,用于人类免疫缺陷病毒-1型(HIV-1)感染成人患者的治疗。这是Mylan公司开发的一款三联组合疗法,每片含有依非韦伦600mg、拉米夫定300mg及富马酸替诺福韦二吡呋酯300mg,已在海外获批上市,商品名为Symfi,用于治疗成人和儿童HIV-1感染者。
5.礼来PD-1激动剂在华报IND。礼来申报的peresolimab注射液的临床试验申请获CDE受理。peresolimab(LY3462817)是一款具“first-in-class”潜力的的单抗药物,可与人类PD-1结合并作为其激动剂,抑制淋巴细胞的激活和扩增。LY3462817与PD-1结合有望刺激生理免疫抑制通路,从而恢复免疫调节,有望成为一种治疗自身免疫性疾病或自身炎症性疾病患者的新方法。目前LY3462817用于治疗类风湿性关节炎正处于Ⅱ期临床开发阶段。
国际药讯
1.武田登革热疫苗获印度尼西亚批准。武田登革病毒(dengue)疫苗Qdenga(TAK-003)获印尼药监部门BPOM批准,用于6-45岁儿童和成人间隔3个月接种两剂预防任何血清型的登革热感染。Qdenga是一种减毒活疫苗,设计用以保护人体四种血清型的登革热。在Ⅲ期TIDES研究中,Qdenga对接种者的保护维持长达3年。此次为Qdenga的全球首批,目前该疫苗也正在接受欧盟的监管审查。
2.精神分裂症阴性症状治疗药物报NDA。Minerva Neurosciences公司在美国提交了5-HT2A/σ2受体拮抗剂roluperidone的新药申请(NDA),用于治疗精神分裂症患者的阴性症状。目前,美国尚无针对精神分裂症阴性症状的疗法获批。在两项III期临床(MIN-101C03和MIN-101C07)中,roluperidone较安慰剂显著改善患者的阴性症状因素评分(NSFS)。如果获批,这将是首款针对这一患者群体的治疗药物。
3.第一三共白血病新药在欧洲报产。欧洲药品管理局(EMA)受理第一三共FLT3抑制剂奎扎替尼(Quizartinib)的上市申请,用于治疗初诊FLT3-ITD阳性的急性髓系白血病(AML)成人患者,该药物可联合标准的阿糖胞苷+蒽环类药物的诱导缓解治疗和阿糖胞苷巩固治疗,以及单药用于巩固后的持续治疗。在中国,奎扎替尼正在III期临床中评估用于初诊FLT3-ITD阳性的AML患者作为维持治疗给药的有效性和安全性。
4.A3AR激动剂治疗肝癌获批同情用药。Can-Fite BioPharma公司口服A3AR激动剂候选药物namodenoson在罗马尼亚获批作为同情用药治疗晚期肝癌患者。一项针对肝细胞癌 (HCC)的II期扩展试验的5年治疗数据显示,有1例患者获得完全缓解并使所有转移肿瘤消失。此前,namodenoson已获得欧盟EMA与FDA的孤儿药资格,以及FDA的快速通道资格。Can-Fite计划启动namodenoson的国际Ⅲ期临床试验,评估namodenoson二线治疗晚期HCC的疗效和安全性。
5.爱尔康7.7亿美元收购多款眼科药物。爱尔康将斥资约7.7亿美元收购Aerie公司,并获得Aerie公司用于降低患者眼内压的已上市产品Rocklatan(奈他舒地尔和拉坦前列素滴眼液)和Rhopressa(奈他舒地尔滴眼液),和处于Ⅲ期临床的干眼病疗法AR-15512等眼科药物管线。AR-15512是一款小分子TRPM8离子通道激动剂,在使用1天或14天后,可显著提高患者的眼泪分泌水平,显著缓解患者的干眼病症状。
6.FDA暂停碱基编辑CAR-T疗法IND。碱基编辑公司Beam 开发的CAR-T疗法BEAM-201的IND申请被FDA暂停,FDA将在30天内提供相关更多详细信息。BEAM-201是一款基于胞嘧啶碱基编辑(CBE)的针对CD7靶点的四重碱基编辑CAR-T疗法,专为同种异体CAR-T细胞而设计。今年6月份,该疗法向FDA提交了治疗复发或难治性急性T淋巴细胞白血病(T-ALL)和其他CD7阳性恶性肿瘤的治疗数据,这也是首个同时编辑4个基因的CAR-T疗法。
医药热点
1.河北率先建设“三孩”优生优育指导门诊。为保障母婴安全,加快推进“三孩”生育政策落地见效,河北省在全国率先开展“三孩”优生优育指导门诊建设。门诊建设方案和评估标准围绕健全完善孕前、孕期、分娩、产后等各环节,以及全流程医疗保健及配套支持措施。“三孩”门诊不仅仅服务于“三孩”孕产妇,还将服务于包括一胎、二胎等在内的所有高危、高龄孕产妇。
2.我国疫苗监管体系通过WHO新一轮评估。北京时间23日晚,世卫组织宣布中国通过疫苗国家监管体系评估。中国的疫苗监管体系此次通过世卫组织升级评估标准后的新一轮全面评估,意味着中国拥有稳定的疫苗监管体系,能确保在中国生产、进口或流通的疫苗质量可控、安全、有效;中国疫苗有资格申请世卫组织疫苗产品预认证,有望被列入联合国等国际组织采购清单。
3.意大利一男子同时感染猴痘、新冠和HIV。英国传染病协会的刊物《感染杂志》(the Journal of Infection)上发布的报告显示,意大利一名男子的猴痘、新冠和HIV检测结果同时呈阳性。据悉,这名36岁的男子曾在西班牙短期旅行,结束旅行后9天左右出现发热、乏力、头痛、腹股沟发炎等症状。这些症状出现后3天,他的新冠病毒检测呈阳性。之后他的左臂上出现皮疹,随后水疱扩散到全身。在卡塔尼亚一家医院急诊时,通过检测发现他的猴痘、新冠和HIV均呈阳性。这是全球首例同时出现猴痘、新冠和HIV感染的病例。
评审动态
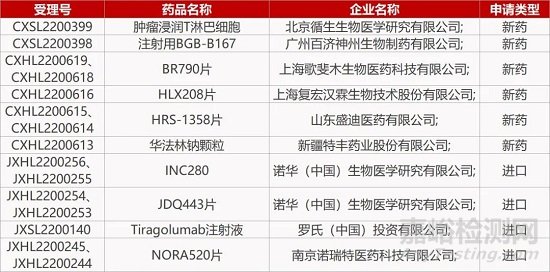
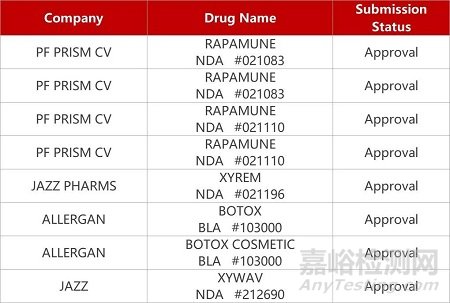

来源:药研发


