今日头条
天劢源和EpCAM-CD3双抗报IND。天劢源和生物1类生物制品“重组抗EpCAM-CD3抗体注射液”的临床试验申请获CDE受理。根据公开信息,推测这是该公司专有免疫治疗抗体技术平台 (iTAbTM)开发的EpCAM/CD3双特异性抗体A-337。A-319借助两个功能区分别与B细胞/B肿瘤细胞表面抗原CD19及T细胞CD3抗原结合,T细胞与肿瘤细胞之间能够形成免疫突触,从而激活T细胞导致肿瘤细胞溶胞而死亡。该新药拟开发用于多种实体瘤的治疗。
国内药讯
1.玛巴洛沙韦获批用于儿童流感。罗氏流感创新药玛巴洛沙韦(速福达)获国家药监局批准新适应症,用于治疗既往健康的成人和5岁及以上儿童单纯性甲型和乙型流感患者,或存在流感相关并发症高风险的成人和12岁及以上儿童流感患者。玛巴洛沙韦是一款创新的帽状结构依赖性核酸内切酶抑制剂,此前已在中国获批用于治疗12周岁及以上急性无并发症的流感患者。
2.康哲引进预充式甲氨蝶呤获批上市。康哲药业从medac公司引进的甲氨蝶呤注射液(预充式)获国家药监局批准上市,该产品允许患者自行皮下给药,治疗对常规疗法不敏感的严重、顽固、致残性银屑病。甲氨蝶呤注射液(预充式)是多种规格的小容量甲氨蝶呤产品,已在欧美获批用于治疗类风湿关节炎,和多关节型幼年特发性关节炎、银屑病、银屑病关节炎、克罗恩病等自身免疫性疾病。
3.卫材癫痫药物新适应症在华报产。卫材吡仑帕奈(perampanel)的5.1类进口上市申请获CDE受理,用于治疗癫痫全身强直-阵挛发作。吡仑帕奈是一款AMPA受体拮抗剂,已在国内获批用于辅助治疗12 岁及以上癫痫患者的伴或不伴继发全面性发作的癫痫局灶性发作,商品名为卫克泰。2021年8月,国家药监局又批准该药用于单药治疗部分发作性癫痫;以及作为辅助疗法/单药疗法,用于≥4岁儿科癫痫患者,治疗部分发作性癫痫。
4.赛诺菲NKp46/CD16/CD123三抗在华报IND。赛诺菲1类生物制品注射用SAR443579的临床试验申请获CDE受理。SAR443579是新型NK细胞接合剂(NKCE),通过Innate专有的多特异性抗体平台ANKET构建,靶向AML细胞上的 CD123,并共同接合NK细胞上的NKp46和CD16a,拟开发用于急性髓性白血病(AML)。在临床前研究中,CD123-NKCE能够显著促进NK细胞的激活,并对AML细胞系具有强效抗肿瘤活性,仅在AML靶细胞存在的情况下诱导细胞因子的分泌。
5.礼新与康方达成联合用药临床合作。礼新医药自研Claudin 18.2 ADC药物LM-302拟与康方生物PD-1/VEGF双抗新药依沃西(AK112)开展一系列临床研究,评估联合用药治疗实体肿瘤的安全性与有效性。在临床前研究中,LM-302显示出良好的安全性及体内外活性,尤其在Claudin 18.2低表达的肿瘤模型中显示出超过对照抗体Zolbetuximab的良好药效。此前,LM-302已获得FDA授予针对胰腺癌,胃癌及胃⻝管交界部癌和胆管癌的三项孤儿药资格。
国际药讯
1.眼科同种异体细胞疗法在日本获批上市。Aurion Biotech现货型、同种异体细胞疗法Vyznova获得日本医药品医疗器械综合机构(PMDA)批准上市,用于治疗大泡性角膜病变。Vyznova旨在利用来自捐赠者角膜的健康细胞通过Aurion专有的创新、多步骤培养,以产生完全分化的角膜内皮细胞。此过程不需经过基因编辑,来自单一捐赠者完全分化的角膜内皮细胞最终可用以治疗超过100只患者眼睛。这是全球首个获批用以治疗角膜内皮疾病的同种异体细胞疗法。
2.长效抗真菌新药「雷扎芬净」获批上市。Cidara公司新型棘白菌素rezafungin(雷扎芬净)获FDA批准上市,用于治疗念珠菌血症和侵袭性念珠菌病。rezafungin具有较长的半衰期,可每周给药1次。在Ⅲ期临床ReSTORE中,rezafungin治疗组在全因死亡率方面非劣效于caspofungin(每天注射)组,达到主要终点。此前,FDA已授予雷扎芬净合格传染病产品(QIDP)、孤儿药和快速通道资格。
3.全球首款自体TIL疗法在美报BLA。Iovance公司肿瘤浸润淋巴细胞(TIL)疗法lifileucel已完成向FDA滚动提交生物制品许可申请(BLA),用于治疗PD-1/L1治疗后进展的晚期黑色素瘤患者。lifileucel是美国国立卫生研究院(NIH)开发的一种自体细胞疗法。II期C-144-01研究数据显示,lifileucel在这类难治性患者中达到34.3%的总缓解率。Lifileucel有望成为首款获FDA批准用于这类患者的全新的治疗方法。
4.艾伯维IL-23抗体治疗UC的III期临床成功。艾伯维IL-23抑制剂risankizumab (Skyrizi)治疗中重度活动性溃疡性结肠炎的III期INSPIRE研究达到主要终点以及所有次要终点。与安慰剂相比,risankizumab治疗第12周时显著提高患者的临床缓解率(20.3%vs6.2%)和内镜改善的患者比例(24.5%vs7.7%)。药物的安全性与其他适应症以往研究中观察到的安全性一致,临床中没有新的安全性信号。
5.FIC抗焦虑鼻喷剂Ⅲ期临床积极。Vistagen公司潜在“first-in-class"鼻喷雾剂fasedienol(PH94B)治疗社交焦虑症(SAD)的Ⅲ期开放标签研究达到主要终点和次要终点。数据显示,fasedienol(3.2µg)能持续减少患者的Liebowitz社交焦虑量表(LSAS)评分,3个月时,患者的LSAS评分平均降低24分,55%的患者降低20分或以上,36%降低30分或以上;fasedienol多次按需鼻内给药的安全性和耐受性良好,未发现新的安全性问题。
6.降脂RNAi疗法获快速通道认定。Arrowhead公司靶向载脂蛋白C-III (APOC3)的RNAi疗法ARO-APOC3获FDA授予快速通道认证,用于降低家族性乳糜粒血症综合征(FCS)成人患者的甘油三酯。ApoC-III是甘油三酯代谢的关键调节剂。目前,该新药正在Ⅱ期临床中评估治疗严重高甘油三酯血症(SHTG)和治疗混合性血脂异常(MD)患者的潜力,以及在Ⅲ期临床中评估治疗FCS患者的疗效。
医药热点
1.儿童抗肿瘤药物临床指导原则发布。3月24日,国家药监局正式发布《儿童抗肿瘤药物临床研发技术指导原则》,旨在为儿童抗肿瘤新药的临床研发提供思路和技术建议,自发布之日起施行。《指导原则》明确,儿童抗肿瘤药物研发,首先需符合儿童药物研发的一般规律,同时还需体现对于恶性肿瘤这种危及生命的严重疾病的特殊考虑,符合抗肿瘤药物研发的一般原则。
2.上海龙华医院江西医院项目开工。3月26日上午,国家区域医疗中心建设项目上海中医药大学附属龙华医院江西医院正式开工。选址位于南昌市艾溪湖东岸地区,闵家路以东、鱼尾路以南、新力时代广场以北,雁行二路66号,项目规划编制床位1000张,总建筑面积18万平方米,总投资估算为16亿元,预计2025年底投入使用。
3.结核病报告发病率我国10年间下降25%。3月24日,中国防痨协会在京主办2023年世界防治结核病日结核病防治论坛,论坛的主题是“赋能基层,精准防控,终结结核”。据悉,我国结核病防治工作成效显著,结核病报告发病率下降25%,下降速度是全球平均水平的2倍;死亡率下降30%,保持在较低水平;结核病患者治愈率始终达到90%以上。
评审动态
1. CDE新药受理情况(03月27日)
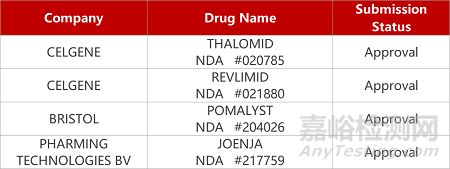
2. FDA新药获批情况(北美03月24日)