2023年截至到目前为止,美国食品药品监督管理局(FDA)已授予32项“突破性设备认定”。
历年FDA“突破性设备”分布
历年共计有760款医疗器械被纳入“突破性设备”名单。其中,8款由主管生物制品的CBER(生物制品评价与研究中心)通过,剩下752款均由主管医疗器械和数字医疗的CDRH通过申请。
以下为2023年部分获批突破性设备介绍。
1、美国医疗器械公司EndoTheia Inc.——柔性内窥镜机器人EndoTheia Robot
认定时间:2023年1月10日
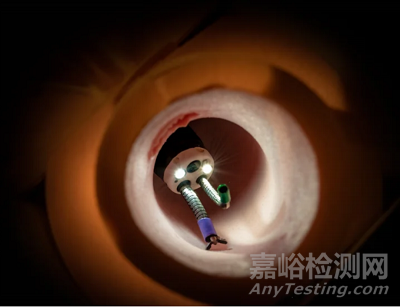
该技术大大改进了微创柔性内窥镜手术;以极薄的激光加工金属管为基础,能够创造出高度灵活、可转向的设备,这些设备可以通过标准的内窥镜,同时本身也携带有介入工具。
为内窥镜输送的工具提供的可操纵性,为柔性内窥镜的新诊断和治疗应用打开了大门。
2、Datar Cancer Genetics——诊断脑瘤的TriNetra-Glio液体活检
认定时间:2023年1月初
该设备利用了Datar公司的循环肿瘤细胞(CTC)富集和诊断技术,通过检测脑肿瘤血液中释放的细胞来诊断脑肿瘤。这些细胞“极为罕见,难以检测”。该测试加入了Datar公司的早期乳腺癌和前列腺癌检测测试。
3、芬兰公司Sooma Medical——家用抑郁症治疗刺激器
认定时间:2023年3月6日
工作原理是利用温和的电流刺激目标大脑区域,从而显着改善抑郁症状。它依赖于经颅直流电刺激(该疗法简称“tDCS”)。通过电极向大脑的特定区域发送电流,该设备可以辅助中断和恢复与抑郁症相关的神经信号,从而缓解症状。
系统是需要开具处方的,它安装于一个灵活的耳机中。用户预先设定后,将电极插入弹性帽,用水凝胶垫覆盖并用生理盐水清洗,之后便可以将帽子戴在头上并开始治疗。每次治疗持续 30 分钟,之后电极自动关闭。
4、大医集团——x/γ射线一体化放射治疗系统
认定时间:2023年3月7日
TAICHI是一款创新放射治疗产品,此前已经获中国国家药监局(NMPA)批准上市。将医用直线加速器、伽玛射线立体定向放射外科系统以及锥形束CT进行同机整合,既可用于多种适应症的单独放射治疗,也可组合起来完成复杂的放射治疗。
该产品通过对多种治疗模式的灵活应用,能够根据患者的个体化差异给每一位患者带来适合的、疗效较好的个性化放射治疗,确保患者利益的最大化。
5、Pixium Vision公司——仿生视觉系统Prima
认定时间:2023年3月31日
该仿生视觉系统,通过植入萎缩性干性老年性黄斑变性(干性AMD)患者体内,帮助部分患者恢复视力。
它是一款视网膜下微型光伏无线植入物,以光感知的形式诱导功能性人工或仿生视觉,部分取代自然中心视力的丧失。通过电刺激视网膜内部的神经细胞,将视觉信息通过视神经传递给大脑,部分取代眼睛感光细胞的正常生理功能。
6、美国神经技术公司Reach Neuro——Avantis系统
认定时间:2023年4月10日
Avantis神经刺激系统可应用于中风所致的长期功能障碍。通过微弱电流冲击脊髓神经,以帮助因长期中风而造成行动不便的病人恢复其对肩膀,胳膊和双手的控制。
它通过靶向电刺激激活脊髓环路,迅速提高中风中后偏瘫患者的自主活动能力。这个系统将一对8个通路的经皮硬膜外引线放在颈部的脊柱侧方,使其有选择地作用在支配上肢和双手的运动神经元胞的背根部。
7、脑际接机(BCI)和AR技术开发商Cognixion——BCI设备Cognixion ONE Axon
认定时间:2023年5月初
Cognixion成立于2014年,是一家在国际上屡获殊荣的神经科学和技术公司,是辅助现实领域的先驱。公司于2021年底获得了1200万美元的A轮融资,由Prime Movers Lab领投。(推荐相关阅读:一文带你了解脑机接口行业)
Cognixion ONE Axon是一款专门为支持患有神经退行性疾病的人而开发的辅助显示设备。其目标是成为第一个被美国FDA批准的、通过无创脑机接口帮助完全瘫痪或类似病人与他人交流的非侵入式脑机设备。
8、脊柱侧凸外科治疗医疗器械公司 Cresco Spine——Spring Distraction System 脊柱系统( SDS™ )
认定时间:2023年5月2日
SDS™脊柱系统能够为患有早发性脊柱侧凸的年轻患者提供更有效、负担更轻的治疗选择。它是一种专利的基于弹簧的动态牵引系统,与后路椎弓根螺钉固定的标准护理方式配合使用。
该系统减少了手术次数,且无需再进行临床延长干预。即使应对最极端的脊柱侧弯变形病例,也允许三维引导脊柱生长。这一系统将改善手术效果,同时最大限度为这一脆弱患者群体降低二次手术的概率以及手术和麻醉负担,而且更具成本效益。
9、鹍远生物——胰腺癌液体活检技术PDACatch
认定时间:2023年5月8日
PDACatch是一种新型的基于DNA甲基化、用于检测高风险人群中胰腺癌的液体活检检测技术。是首个辅助检测胰腺癌的液体活检工具;对于高危人群的早期检测和监测将对该人群生活质量产生重大影响。
自2014年成立以来,鹍远生物以攻克癌症早期筛查与诊断为目标,基于分子诊断技术开发了一系列肿瘤和遗传疾病的基因检测解决方案。公司在上海和美国圣地亚哥设有研发基地;在上海和扬州设有生产基地。
10、上海奕谱生物科技——尿路上皮癌检测产品“TAGMe DNA Methylation Detection Kit (qPCR) for Urothelial Cancer”(国内商标名:滂奕清®)
认定时间:2023年5月中旬
全球首个获得美国FDA突破性医疗器械认定的自主研发的基于全癌标志物的尿路上皮癌(膀胱癌、输尿管癌和肾盂癌)尿液同步检测产品。
采用全基因组 DNA 甲基化检测方法GPS (Guide Positioning Sequencing),即“导向定位测序”。基于GPS 技术对全基因组DNA高精度和高覆盖度的甲基化检测,找到了在肿瘤中共有的一类甲基化位点,并在全球首次提出“全癌标志物” (Universal Cancer Only Marker, UCOM) 概念,进而发现了一系列TAGMe®全癌肿瘤标志物,目前已发现57个全癌标志物检测靶标。
11、美国高速脑机接口(BCI)公司Paradromics——Connexus直接数据接口(DDI)
认定时间:2023年5月18日
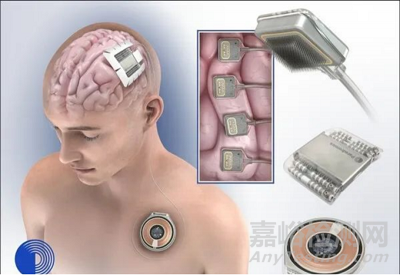
该产品可用于治疗因ALS、脊髓损伤和中风等疾病导致的严重运动障碍,并恢复患者的交流能力和操作能力。Connexus DDI是一种植入式的BCI设备,可以从大脑信号中提取语音和运动信息,并实时转换为可交流的输出。
可以帮助那些大脑功能正常但无法说话或使用电脑的患者,重新建立社会联系和独立生活。除了辅助交流之外,BCI设备还有可能应用于其他一系列目前难以治愈的医疗需求,如运动和感觉缺陷、慢性疼痛和情绪障碍等。
12、中国Pulse Medical公司——第四代 μFR ®系统
认定时间:2023 年 5 月 26 日
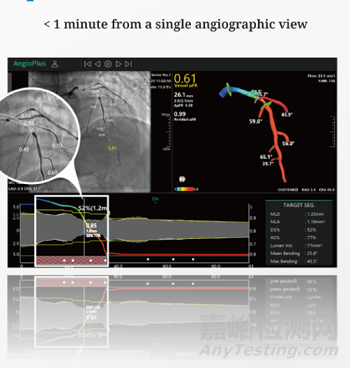
μFR 是一种基于血管的生理评估工具,无需压力线或充血剂。它的适应症范围更广,价格也更实惠。μFR® 可用于整个 PCI 过程,包括 PCI 前的精确生理评估、手术期间的策略优化、PCI 后的结果和微循环功能评估。
公司成立于2015年,位于中国上海,致力于开发用于泛血管疾病患者精准诊断和优化治疗的创新技术。开创并发明了 μFR® 的关键算法——一种从多个成像数据中快速计算血流储备分数 (FFR) 的方法。
13、美国QuantalX公司——Delphi-MD神经诊断设备
认定时间:2023年5月31日
Delphi-MD系统是一种创新的神经诊断工具,能够在任何护理点为医生提供大脑健康相关的诊断能力,从而有助于改善患者的治疗结果。该设备可用于诊断正常压力脑积水(NPH)患者,并预测他们接受脑室腹腔分流术(VPS)治疗后的反应。
14、中精普康——PrecogColo Dx 早期CRC血检
认定时间:2023年6月9日
基于血清代谢检测的结直肠癌及进展期腺瘤早筛检测(国内产品应用名:早长静®),是中精普康推出的首款用于结直肠癌早期发现的血检,已获得国际专利(专利序号:US11462305B2)、国内专利(国内专利序号ZL202080030060.1)。
从进展期腺瘤到I、II期结直肠癌,早长静®的敏感性和特异性均比肩国际标杆企业Freenome及Guardant health 同期发布的数据,其临床检测性能位于世界第一梯队,为国内首个自主研发的多组学结直肠早期肿瘤血检。