今日头条
荣昌MSLN-ADC获妇科肿瘤快速通道资格。荣昌生物靶向MSLN的ADC药物RC88获FDA授予快速通道资格,用于治疗铂耐药复发性上皮性卵巢癌、输卵管癌和原发性腹膜癌(PROC)患者。RC88通过靶向结合MSLN阳性的肿瘤细胞,介导抗体的内吞并将细胞毒素定向传递给癌细胞以杀灭肿瘤。荣昌生物计划在美国、中国、欧盟等国开展多中心国际Ⅱ期临床,评估单药治疗铂耐药复发性卵巢癌的潜力。
国内药讯
1.卫材/渤健Aβ抗体中国获批上市。卫材Aβ抗体仑卡奈单抗注射液(lecanemab)获国家药监局批准上市,用于治疗轻度阿尔茨海默症(AD)和AD引起的轻度认知障碍(MCI)疾病的改善治疗。在III期Clarity AD试验中,lecanemab较安慰剂使患者临床痴呆评分总和(量化痴呆症状的各种严重程度,CDR-SB)下降减少27%,患者大脑中淀粉样蛋白水平显著下降59.1centiloids。2023年7月,FDA已批准lecanemab的加速上市许可转变为完成批准。
2.礼来偏头痛新药中国获批上市。礼来CGRP受体拮抗剂加卡奈珠单抗注射液(galcanezumab)获国家药监局批准上市,用于预防性治疗成人发作性偏头痛。在Ⅲ期临床中,与安慰剂组相比,galcanezumab治疗组每月头痛天数显著减少;在四个评估偏头痛对功能影响的关键次要终点方面,治疗组也优于安慰剂组。蔼睦医疗拥有该新药在中国大陆的商业化授权。
3.阿斯利康PARP抑制剂中国报新适应症。阿斯利康PARP抑制剂奥拉帕利(olaparib)的新适应症上市申请获CDE受理,单药或与内分泌治疗联用,辅助治疗胚系BRCA1/2突变的HER2阴性早期高危乳腺癌。在Ⅲ期OlympiA临床中,奥拉帕利将患者疾病复发、出现新肿瘤或死亡的风险降低42%,并将死亡风险降低32%。
4.康宁杰瑞HER3/TROP2双抗ADC报IND。康宁杰瑞1类生物制品JSKN016注射液的临床试验申请获CDE受理,拟开发用于晚期恶性实体瘤治疗。JSKN016是一款靶向表皮生长因子受体3(HER3)和人滋养细胞表面抗原2(TROP2)的双抗偶联药物(ADC),通过与肿瘤细胞表面TROP2或者HER3结合后,介导抗体的内吞并将细胞毒素定向传递以杀灭肿瘤;它还可以通过旁观者效应,协同抑制肿瘤细胞的生长。
5.百奥赛图HER2/TROP2双抗ADC授权海外。百奥赛图宣布与Radiance Biopharma就其同类首创HER2/TROP2双抗偶联药物达成独家选择与授权协议,Radiance有权选择获得这款双抗ADC用于针对任何人类疾病在全球范围内的开发、生产和商业化许可。根据协议,Radiance如果行使选择权,百奥赛图将获得选择权行使费、许可费、开发和商业化里程碑付款,以及个位数净销售额分成;如果Radiance再授权给第三方,百奥赛图还将获得分许可费。
6.康华重组六价诺如病毒疫苗授权HilleVax。康华生物宣布与HilleVax公司签署独家许可协议,将其六价重组诺如病毒疫苗及其衍生物的大中华区外全球开发和商业化权益授予后者。根据协议,康华生物将获得1500万美元预付款,2.555亿美元里程碑后期付款,以及合作产品个位数百分比的销售分成。在临床试验中,该疫苗可以覆盖90%的诺如病毒感染病例。
国际药讯
1.诺华STAMP抑制剂白血病III期临床成功。诺华STAMP抑制剂Scemblix(asciminib)一线治疗费城染色体阳性慢性髓性白血病慢性期(Ph+ CML-CP)成年患者的III期ASC4FIRST研究达到双重主要终点。与研究者选择的TKIs(伊马替尼、尼洛替尼、达沙替尼和博舒替尼)相比,Scemblix治疗第48周时患者主要分子学反应(MMR)率显著更高;药物的安全性良好,没有观察到新的安全信号。
2.拜耳神经激肽拮抗剂更年期Ⅲ期临床积极。拜耳双神经激肽-1,3受体拮抗剂elinzanetant治疗更年期血管舒缩症状(潮热,VMS)的两项Ⅲ期临床(OASIS 1和OASIS2)达到主要终点与所有关键性次要终点。与安慰剂相比,elinzanetant治疗显著降低更年期女性中度至重度VMS的频率和严重程度;患者睡眠障碍和更年期相关生活质量也显著改善;药物的安全性与已知研究一致。详细结果将在科学大会上展示。
3.Oryzon公司LSD1抑制剂Ⅱb期临床失败。Oryzon Genomics公司口服赖氨酸特异性去甲基化酶1(LSD1)抑制剂Vafidemstat治疗边缘型人格障碍(BPD)的Ⅱb期PORTICO临床未达到主要终点。与安慰剂相比,vafidemstat治疗降低了8-12周时BPDCL评分和CGI-S A/A评分,但未达到统计学意义的改善(p=0.41, p= 0.25);不过vafidemstat治疗在总体疾病改善上具有统计学意义。Oryzon计划与FDA沟通后继续推进Ⅲ期临床。
4.强生约20亿美元收购ADC公司Ambrx。强生将斥资约20亿美元收购Ambrx公司,并获得该公司多款临床期ADC药物(ARX517,ARX788)。ARX517是一款靶向前列腺特异性膜抗原(PSMA)的ADC,已被获FDA授予快速通道资格,用于治疗接受雄激素受体通路抑制剂治疗后疾病进展的转移性去势抗性前列腺癌(mCRPC)。ARX788是一款靶向HER2的ADC,已在治疗HER2阳性乳腺癌的Ⅱ/Ⅲ期临床达到主要终点。新码生物拥有ARX788的中国权益。
5.默沙东近7亿美元收购Garpoon公司。默沙东宣布斥资约6.8亿美元收购Harpoon Therapeutics,并获得该公司一系列T细胞接合器候选疗法(HPN328、HPN217和HPN601等)。HPN328是一款靶向DLL3的T细胞接合器,目前正在Ⅰ/Ⅱ期临床中评估单药治疗携带DLL3表达的晚期癌症患者的潜力。HPN217靶向B细胞成熟抗原(BCMA),目前正在Ⅰ期临床用于治疗复发/难治性多发性骨髓瘤患者。
6.Isomorphic Labs与礼来和诺华达成研发合作。Isomorphic Labs宣布分别与礼来和诺华达成研发合作,利用其新一代AlphaFold技术,针对多个靶点开发小分子疗法。两项合作总额约30亿美元。新一代AlphaFold不仅可预测蛋白质结构,还扩展到小分子和核酸结构。诺华与Isomorphic Labs将针对3个未披露的靶点开发小分子候选药物;Isomorphic Labs将获得3750万美元前期付款,以及高达12亿美元的里程碑付款。
医药热点
1. 2022年度“国考”TOP100名单出炉。1月8日,国家卫健委公布2022年度三级公立医院绩效考核结果。全国共有2112家三级公立医院参加本次考核。其中,西医综合类TOP10名单分别为:北京协和医院、浙江大学医学院附一医院、四川大学华西医院、浙江大学医学院附属第二医院、山东大学齐鲁医院、上海交通大学医学院附属瑞金医院、南京鼓楼医院、北京大学第三医院、浙江大学医学院附属邵逸夫医院、复旦大学附属中山医院。
2.全国首家惰性淋巴瘤专科门诊成立。1月 5日,全国首家惰性淋巴瘤专科门诊在中国医学科学院血液病医院揭牌成立。惰性淋巴瘤一般临床进展缓慢,病程较长,患者通常需要定期随访。惰性淋巴瘤专科门诊旨在为惰性淋巴瘤患者提供标准化,规范化、优质化的诊断治疗和随访,助力惰性淋巴瘤优质的全程管理。
3.礼来中国换帅。1月9日,礼来中国宣布,Huzur Devletsah正式出任礼来中国总裁兼总经理。Huzur Devletsah拥有博斯普鲁斯海峡大学化学学士学位和土耳其马尔马拉大学商业管理研究生学位。她在1998年加入礼来公司,至今已经25年。此前,Huzur Devletsah担任礼来意大利总裁兼总经理,她还曾担任礼来中东欧、俄罗斯独联体国家以及以色列的总裁兼总经理。
评审动态
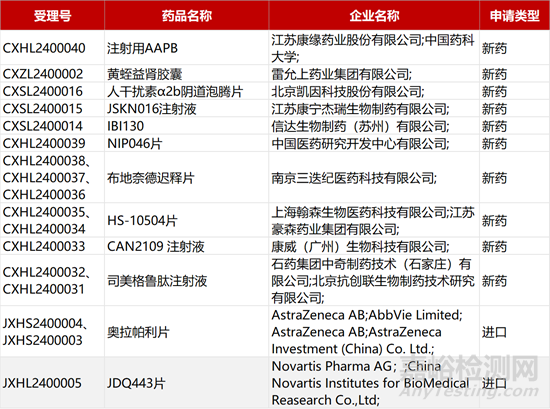
1. CDE新药受理情况(01月09日)
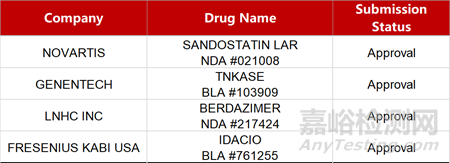
2. FDA新药获批情况(北美01月08日)