今日头条
诺诚健华BCL2抑制剂美国获批临床。诺诚健华自研BCL2抑制剂ICP-248获FDA批准开展Ⅰ期临床,评估用于治疗血液肿瘤患者的安全性、耐受性、药代动力学和初步疗效。ICP-248可激活内源性线粒体凋亡通路,从而导致癌细胞迅速凋亡,发挥抗肿瘤作用。该产品已在国内开展Ⅰ期剂量递增试验,初步数据已显示出良好的安全性和有效性。
国内药讯
1.齐鲁ALK/ROS1抑制剂获批新适应性。齐鲁制药新型口服间变性淋巴瘤激酶(ALK)/ROS1抑制剂伊鲁阿克(WX-0593)获国家药监局批准新适应症,用于一线治疗ALK阳性的非小细胞肺癌(NSCLC)。去年6月,该新药已获得NMPA批准上市,用于治疗既往接受过克唑替尼治疗但疾病仍有进展、或对克唑替尼不耐受的ALK阳性的局部晚期或转移性NSCLC患者。
2.药物牧场ALPK1抑制剂获儿科罕见病资格认定。FDA授予药物牧场(Drug Farm)潜在“First-in-class”新药ALPK1抑制剂DF-003儿科罕见病资格认定(RPDD),用于治疗ROSAH综合征(视网膜营养不良、视神经水肿、脾肿大、无汗症和头痛)患者。这是一种罕见、由ALPK1的遗传功能高活突变引起的常染色体显性遗传性自身炎症性疾病。DF-003可抑制ALPK1和ALPK1 T237M驱动突变。
3.圣因PCSK9靶向RNAi疗法国内启动临床。圣因生物靶向肝细胞PCSK9的siRNA-GalNAc药物SGB-3403登记启动一项I期临床,评价SGB-3403注射液在健康受试者及低密度脂蛋白胆固醇(LDL-C)升高受试者中的安全性、耐受性、药代动力学特征以及药效学特征。该项试验将由蚌埠医学院第一附属医院王洪巨教授和周焕教授牵头开展。去年5月,SGB-3403已在澳大利亚开展I期临床研究。
4.百吉TCR-T国内获批实体瘤临床。百吉生物基因修饰TCR-T细胞产品BRL03注射液获国家药监局临床许可,拟开发用于治疗EBV阳性晚期实体瘤患者,包括鼻咽癌、肺淋巴上皮瘤样癌和胃腺癌。该产品采用过继性免疫细胞治疗技术,通过采集患者血液中的免疫细胞,在体外进行基因工程化改造,增强T细胞对肿瘤细胞的特异性识别与杀伤效力。去年9月,FDA已批准BRL03在美国开展I/II期临床试验。
5.康方CD47单抗获批联合治疗AML临床。康方生物新一代CD47单抗AK117获国家药监局批准开展Ⅱ期临床试验,联合维奈克拉(VEN)和阿扎胞苷(AZA),治疗初治不适合标准诱导化疗的急性髓系白血病(AML)患者。AK117可与肿瘤细胞上表达的CD47结合,阻断CD47与其受体SIRPα的相互作用,增强吞噬细胞对肿瘤细胞的吞噬活性,从而抑制肿瘤生长。研究表明,CD47单抗联合AZA和VEN,在AML中具有协同抗肿瘤潜力。
国际药讯
1.罗氟司特乳膏皮炎两项Ⅲ期临床积极。Arcutis公司下一代4型磷酸双酯酶(PDE4)抑制剂疗法roflumilast(Zoryve)治疗特应性皮炎的两项Ⅲ期临床(INTEGUMENT-1和INTEGUMENT-2)汇总结果积极。治疗4周后,roflumilast组达到EASI评分减少50%(EASI-50)的患者比例较安慰剂组显著更高(69.2%vs44.4%,p<0.0001);两组安全性和耐受性相似。目前,Zoryve已获批用于治疗6-11岁儿童、≥12岁以上斑块状银屑病患者,以及脂溢性皮炎。
2.Mineralys公司ALDOS抑制剂启动高血压Ⅲ期临床。Mineralys公司选择性ALDOS抑制剂Lorundrostat针对高血压适应症启动Ⅲ期临床。在II期Target-HTN研究中,在意向性治疗群体中,不同剂量Lorundrostat队列患者,其经安慰剂调整的收缩压下降9.7mmHg(每天50mg,p=0.010)、7.9mmHg(每天100mg,p=0.037);当患者同时使用噻嗪类利尿剂(thiazide diuretic)作为背景治疗时,Lorundrostat(每天100mg)组收缩压降低了11.4mmHg。
3.创新PDC疗法膀胱癌Ⅱ期临床积极。Theralase公司光敏化合物(PDC)TLD-1433治疗非肌肉浸润性膀胱癌(NMIBC)的Ⅱ期临床结果积极。TLD-1433是一种钌基(ruthenium)分子,在被膀胱癌细胞优先吸收并被光激活后,可对癌细胞产生剧毒,在纳摩尔浓度下杀死>99.9%的癌细胞。中期数据显示,TLD-1433治疗90天时患者的总缓解达到63%,完全缓解率为56%。该公司计划向FDA递交TLD-1433的突破性疗法认定申请。
4.铅订书脂肽治疗新冠临床前研究积极。美国丹娜-法伯癌症研究院与波士顿大学等研究团队开发的铅订书脂肽(lead-stapled lipopeptide)鼻腔喷雾剂在治疗COVID-19感染的临床前研究积极结果发表于Nature Communications期刊上。仓鼠在鼻腔接种SARS-CoV-2之前和/或之后接受铅订书脂肽,结果显示每组接受铅订书脂肽的仓鼠都保持了体重,与未接受治疗的对照组相比,病毒滴度相对下降,严重肺炎方面也得到显著保护。
5.穿心莲内酯衍生物抗炎临床前研究积极。近期发表在Biomedicine & Pharmacotherapy杂志上一项最新研究显示,一种天然化合物穿心莲内酯(andrographolide)的衍生物AG5,能够通过抑制caspase-1作用于炎症小体,从而调节与细菌和病毒感染相关的炎症过程中的免疫反应。AG5有望在治疗各种炎症性疾病和预防/治疗CAR-T细胞疗法引起的细胞因子风暴方面提供新的治疗选择。研究人员计划在2024年向西班牙药监部门申请开展AG5用于脂肪肝的Ⅰ/Ⅱ期临床试验。
6.Orion公司收购ADC药物公司LegoChem股份。芬兰制药商Orion Group宣布旗下香港子公司Pan Orion Corp将以5500亿韩元(4.18亿美元)收购韩国生物技术公司LegoChem Biosciences 25.7%的股份。收购完成后,Orion将成为LegoChem的最大股东,而LegoChem Biosciences将保留现有的管理和运营。LegoChem公司专有ADC技术平台具有独特的连接分子和毒素,有望在未来五年内推出10个临床候选药物,应用于肿瘤学和自身免疫疾病领域。
医药热点
1.姜植铭出任万泰生物总经理。万泰生物发布公告,称其董事会近日收到董事长兼总经理邱子欣提交的书面辞职报告。邱子欣决定将主要精力集中在董事长工作职责和公司战略发展上,申请辞去公司总经理一职,辞职后仍继续担任公司董事长职务和董事会专门委员会委员相关职务。经公司董事长邱子欣提名、董事会提名委员会审核,董事会同意聘任姜植铭女士为公司总经理。
2.FDA前监管专家入职细胞疗法公司总裁。1月15日,专注于研发T细胞疗法的NeoImmuneTech(NIT)宣布,任命Luke Oh博士为总裁,立即生效。Luke Oh博士主要工作重点是加快长效人IL-7因子NT-I7的临床开发,并为其治疗急性辐射综合征(ARS)的潜在首次批准制定监管路径。此前,Luke Oh博士曾在FDA临床药理学III分部以及炎症和免疫药理学分部担任高级研究员。
3.我国推动生物技术与延缓老年病深度融合。近日,国务院办公厅印发《关于发展银发经济增进老年人福祉的意见》,提出26项举措,对老年人的医、食、住、行、文娱、购物等方面做出明确指导,其中与医疗医药产业息息相关的鼓励政策较多,包括推动基因检测、分子诊断等生物技术与延缓老年病深度融合,开发老年病早期筛查产品和服务等。
评审动态
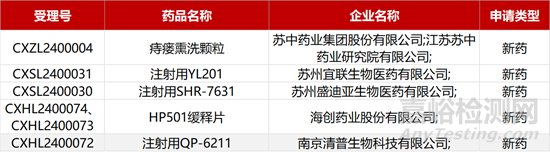
1. CDE新药受理情况(01月16日)
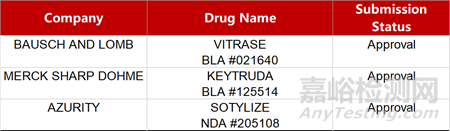
2. FDA新药获批情况(北美01月12日)