您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-04-20 20:22
摘要
作为医疗器械安全治理的制度安排,审评审批制度改革对于医疗器械创新发展具有重要意义。文章从确立核心价值理念、变革医疗器械上市准入规则、调整组织结构、完善技术审评流程、健全技术审评质量管理体系和发布技术指导原则等方面,总结医疗器械审评审批制度改革的实践做法,并实证评估了2017 至 2023 年期间第三类医疗器械注册审评用时与质量,观察到医疗器械注册质量体系核查提高了审评效率 ;医疗器械注册电子申报提高了技术审评信息化水平 ;补充资料通知单发放数量、第三类医疗器械审评用时在不断下降,确保了审评效率。同时,对重点省份的改革举措以及审评审批制度对企业的影响也做了分析。建议持续推进质量体系建设,提高创新能力、人才队伍建设水平与审评服务能力,以提升医疗器械创新水平。
2015 年 8 月,国务院印发《关于改革药品医疗器械审评审批制度的意见》,主要任务中包括改革医疗器械审批方式和全面公开药品医疗器械审评审批信息,以建立更加科学、高效的医疗器械审评审批体系,提高审评审批的质量和透明度。为了进一步促进药品医疗器械的技术创新,提高产业竞争力,2017 年 10 月,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,意在加快药品医疗器械上市审评审批,推动企业提高创新和研发能力。《“健康中国 2030”规划纲要》也明确指出,加快转变政府职能,继续深化药品、医疗机构等审批制度改革,推动创新药品医疗器械快速上市。国家药品监督管理局 (NMPA) 等 8 部门联合印发的《“十四五”国家药品安全及促进高质量发展规划》也提出,推进药品监管体系和监管能力现代化,保障药品安全,促进药品高质量发展。这一系列顶层文件的发布,均指明了药品医疗器械高质量发展与审评审批制度改革之间的密切关系。
在药品医疗器械审评审批制度改革中,如何提高审评效率、确保在法定时限内完成技术审评,如何提高审评质量、确保产品的安全性与有效性,如何科学审评以提升审评工作的科学性、前瞻性和适应性,如何平衡合规性和时效性,如何提升审评质量与效率,如何促进审评的科学与创新性,都是审评审批制度改革的重点。8 年来,我国进行了哪些制度性创新,如何建立相应的指标体系来衡量实施效果,成为药品医疗器械监管领域的重要课题。
2015 年以来,我国医疗器械审评审批制度改革主要集中在鼓励医疗器械研发创新、改革临床评价管理制度、优化审评审批机制等 11 个方面 。在优化程序提升审评审批效率、提升技术审评质量、开辟特批通道激发创新活力等方面,医疗器械审评审批制度改革取得了阶段性成果。NMPA 医疗器械技术审评检查中心 ( 简称“器审中心”) 在“创新、质量、效率、体系和能力”等五大方面得到提升。
1、 建立以技术审评为主导的医疗器械审评审批制度
医疗器械审评审批制度指注册申请人提出医疗器械注册申请,医疗器械技术审评部门进行技术审评,出具医疗器械技术审评报告,医疗器械许可审批部门据此作出许可决定的管理制度。审评审批的质量与效率在很大程度上影响着医疗器械上市速度和应用时机。器审中心积极做好改革的顶层设计,调整优化机构职能,建立健全审评制度,升级再造审评流程,全面实现电子申报,强化科学审评研究,加强新工具新方法开发应用,持续有效运行审评质量管理体系,各项改革举措相继落地并取得积极成效 。《医疗器械注册与备案管理办法》( 市场监督管理总局令 2021 年第 47 号 )首次在第二十一条明确规定,“药品监督管理部门持续推进审评审批制度改革,加强医疗器械监管科学研究,建立以技术审评为主导,核查、检验、监测与评价等为支撑的医疗器械注册管理技术体系,优化审评审批流程,提高审评审批能力,提升审评审批质量和效率。”审评审批制度改革的必要性和重要性在法律上得到了明确规定。
技术审评是针对质量管理体系有效运行过程中产生的证明产品安全性和有效性的验证、确认文件,从技术和风险2个层面进行产品安全性和有效性的综合评估,以提出产品是否可以上市的审评意见。医疗器械技术审评是医疗器械技术审评部门对医疗器械注册申请人申请的拟上市医疗器械的安全性和有效性研究及其结果进行系统评价,判定风险 / 收益比,并出具审评结论的过程。在遵循依法、科学、公开、公平、公正原则的基础上,应按照国家标准《质量管理体系要求 :GB/T 19001—2016》的要求,科学分配审评资源,主动识别审评业务风险。目前,器审中心制定实施了 15 项措施,建立了科学审评、审评质量体系和服务企业制度,形成以制度、技术指导原则、流程、沟通与质量体系为框架的科学高效的审评机制 ( 表 1,资料来源 :https://learn.cmde.org.cn)。

技术审评工作的质量和效率关系到医疗器械产品的安全性、有效性以及可及性,通过识别审评风险并采取有效措施保障审评质量和提升审评效率,显得尤为关键。鄢可书等以医疗器械领域为代表实证考察技术审评所面临的风险,针对其中第三方失灵的风险,应用治理理论探索技术审评的社会治理路径,设计治理格局。蓝翁驰等系统梳理了审评流程中各环节存在的风险,建议强化对审评全过程的质量控制,有效实现审评质量和效率的提升,保障医疗器械审评审批制度各项改革举措落地生效。特别在抗击新性冠状病毒感染疫情期间,医疗器械审评审批制度改革工作的快速推进以及技术审评体系和能力建设水平的不断提高,有力保障了应急产品技术审评工作能够及时、有序地开展。
以上文献从医疗器械审评审批制度的建设、完善医疗器械技术指导原则实施的质量控制与审评风险管理和沟通交流等方面,对医疗器械技术审评质量与效率进行了定性评价,但缺少实证检验。本文基于我国医疗器械审评审批制度改革的经验,对审评审批制度改革成效进行实证研究,并在此基础上,对医疗器械技术审评能力建设的提出建议。
2、 2017 至 2023 年我国医疗器械审评审批制度改革的实践经验
2.1 确立“以人民为中心,保护和促进公众健康”的核心价值理念
根据现代化国家治理体系理论,作为最内圈层的“文化价值体系”决定着国家治理体系的目标。我国医疗器械审评审批制度改革同样践行了这一价值理念,树立了“以人民为中心,保护和促进公众健康”的核心价值观,较好地平衡了满足临床需求和保证产品安全之间的关系,审慎推进审评审批制度改革,践行医疗器械“安全、有效、可用、可及”的价值观,不断推动医疗器械技术审评工作的发展。
2.2 突破传统的医疗器械上市准入规则,满足临床需求
传统的医疗器械上市准入路径是先对医疗器械进行技术审评,安全性和有效性得到肯定评价之后再进行上市审批,最后在医疗机构中使用,即严格遵循“先评价、后审批、再使用”的上市准入规则。近年来,随着医疗器械附条件审批、医疗器械临床试验拓展性应用、医疗机构对未上市的体外诊断试剂自研自用、医疗机构少量进口使用未上市医疗器械等制度在《医疗器械监督管理条例》中得以确立,“边评边用”和“先用后评再批”的医疗器械上市准入新规则已经初具雏形,这不仅意味着传统的医疗器械上市准入规则在一定程度上被突破,并且这些灵活的审评方式凸显了准入规则的审慎包容性,可满足不同形式的临床需求。
2.3 创新技术审评的组织结构与项目管理
按照管理学组织结构理论,器审中心建立了以专业为导向、兼顾效率的组织结构,并确保组织机构高效率运行。由表 2 可见,我国器审中心人员绩效远超欧美日,人均审评任务从 2017 年的 87件,上升到 2022 年的 97 件。
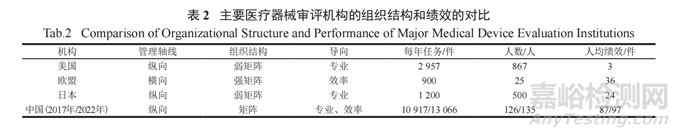
器审中心的项目管理部组织实施立卷审查、项目管理人和项目小组团队审评制度,督导审评进度,旨在提高审评质量和效率,对审评项目进行全面管理 ;增设临床与生物统计部门,完善以临床使用为导向的风险审评制度,强化医疗器械的临床评价。审评部和临床部分别进行非临床资料和临床资料的审评并专业审查,保证了审评审批决定的科学合理性。
2.4 完善技术审评流程以提高审评效率
器审中心基于对审评业务的风险识别,通过调整和优化使审评流程更加简单、科学,实现了审评流程的再造,进而提升了技术审评的效率。
第一,智能分配业务与项目分级分阶段审评。依据医疗器械产品特点,分配不同的审评人员进行“三分法”,即分级、分路径与分段审评。
第二,建立立卷审查、补正资料预审查与对外咨询服务制度。在注册申报受理前、审评、发补等各个阶段,设立多种沟通渠道,及时为生产企业提供技术指导。
2.5 建立健全技术审评质量管理体系以提升审评质量
器审中心建立了质量管理体系,明确管理职责、程序、审评的实现过程,保障了资源的有效配置,从而确保审评质量管理体系的有效运行。在审评质量体系建设中,项目管理人制度、对外咨询制度和信息公开制度可以保障审评质量体系的运行,实施《医疗器械注册审评质量管理规范》,确保符合法规要求。
2.6 发布技术审评指导原则以提高审评科学性
技术审评指导原则是医疗器械上市前审评的重要技术支撑文件。器审中心建立临床评价通用指导原则、各类产品临床评价指导原则、各类产品临床评价审评要点,涵盖有源、无源和诊断试剂三大类别的指导原则体系;基本实现了全面覆盖《医疗器械分类目录》三级目录下需要进行的临床评价产品,并逐渐建立起技术审评向产品研发阶段前移的工作机制。
器审中心也做好了前沿技术、创新产品指导原则的技术储备。对前沿技术和创新产品进行先期介入和研讨,保证技术审评紧跟最新发展。鼓励有候选产品的企业,尤其是处于研发阶段后期的,提前与医疗器械监管部门联系、做好备案,不断扩大监管部门的技术储备,应对可能的突发事件。
3、 2017 至 2023 年我国医疗器械审评审批制度改革效果的评析
3.1 医疗器械审评审批制度改革在国家层面取得的成效
审评审批制度改革于 2015 年启动后,NMPA 批准的医疗器械注册证为 2424 个,比 2014 年下降了54.3%,主要原因是首次进口医疗器械注册证的数量大幅下降 ;到 2023 年底,NMPA 批准的医疗器械注册证为 2732 项。从注册申请事项转入项目和转出审结项目看 :2015 年,注册申请转入 9 590 项,转出审结 7263 项 ( 占比 75.7% ) ;到 2023 年,转入项目为 16018 项,转出审结项目为 15012 项,占比93.7%。其中,2017 年、2022 年转出审结的项目超额完成。具体如表 3 所示 ( 其中,2011 至 2017 年 7月为注册品种转入和转出数据,自 2017 年 8 月起,数据为注册申请事项转入和转出审结数据 ;NMPA批准的医疗器械注册数包括三类医疗器械,进口三类医疗器械、二类医疗器械和港澳台医疗器械 )。

注册环节质量管理体系核查是对研发和生产过程的符合性考核,是对其质量管理能力进行审核,以决定产品的质量是否可控。2015 年以来,医疗器械注册质量管理体系核查工作整体开展顺利。2018 至 2023 年,注册质量体系核查完成率高于 80%,但是部分体系核查结果超期未返回,造成技术审评工作无法按时完成,具体如表 4 所示。

第三类医疗器械审评用时在不断下降。根据《医疗器械注册与备案管理办法》明确规定,第二类、第三类、医疗器械临床试验审批申请的技术审评时限分别为 60、90 和 60 个工作日,申请资料补正后的技术审评时限分别为 60、60 和 40 个工作日。而2020 至 2023 年注册总用时的具体情况如表 5 所示,单项和总用时有所减少,审评效率得到提升。
医疗器械注册电子申报提高了技术审评的信息化水平。自 2019 年医疗器械的注册电子申报系统( eRPS) 启动以来,企业使用电子申报的比例大幅增加。2019 年 6 月,线上电子申报占比为 42.5%,到 2021 年 10 月则提升到 96.6%。医疗器械 eRPS将申请资料按要求进行分类、归纳,资料更加全面、完整,可以有效提升申报质量。随着 eRPS 在国际医疗器械监管者论坛 ( IMDRF) 各成员国的推行,在向 IMDRF 中的其他成员国提交医疗器械注册申请时,无需再重新调整其相应申报资料,节约了注册成本,加快了产品上市进度。

3.2 重点省份医疗器械审评审批制度改革的举措与成效
审评审批制度出台后,各省反应迅速,积极出台了配套文件,由药品监管部门牵头,各部门通力合作,创造利好环境,对医疗器械创新产生深远影响。北京市药品监督管理局实施了《北京市药品监督管理局医疗器械创新服务提质增效行动方案 (2023—2025 年 )》,以发挥国家级创新服务站作用,开展精准服务和指导。上海市药监局通过实施《上海市加强集成创新持续优化营商环境行动方案》缩短了医疗器械审评审批平均时限,持续提升了审评审批的效能。江苏省、浙江省药监局也制定了第二类医疗器械优先审批、特别审查与应急审批程序。
2014 至 2023 年,NMPA 共批准了 250 个创新医疗器械,其中北京、上海、广东、江苏和浙江等五省市获批的创新医疗器械产品数量为 196 个,占比 78.4%,如表 6 所示。
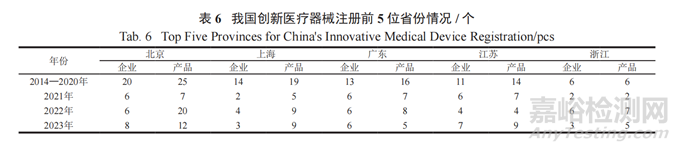
2020 年 12 月,NMPA 医疗器械技术审评检查长三角分中心 ( 以下简称“长三角分中心”) 与 NMPA医疗器械技术审评检查大湾区分中心 ( 以下简称“大湾区分中心”) 成立,这是高质量、一体化发展的实践平台,能以科学、高效、专业的区域性审评检查,推动长三角分中心与大湾区分中心医疗器械的成果转化、产业聚集和创新发展。截至 2023 年 11 月底,大湾区分中心实现了对区域内 46 个创新特别审批产品、5 个优先审批医疗器械产品相关企业的主动服务全覆盖。2023 年,大湾区分中心审结项目 3601 个,发出补正通知 1140 份,完成变更备案等其他事项548 项,受理前咨询预约申请 1160 项 ( 数据来源:大湾区分中心官网 www.gbacdei.org.cn)。
3.3 医疗器械审评审批制度改革对企业的积极影响
审评审批制度改革推动了医疗器械企业研发投入持续增加。2022 年,114 家 A 股上市医疗器械公司研发投入为 226.28 亿元,比 2021 年增加 45.52亿元,增幅 25.18% 。根据国家统计局数据显示,规模以上医药制造业工业企业的专利申请数从 2016年的 17785 件增加到 2022 年的 33128 件。
2017 和 2023 年,创新医疗器械申报分别为273 和 466 项,进入创新医疗器械特别审查程序的项目分别为 63 和 69 项。根据《2023 年度医疗器械注册工作报告》数据显示,2014 至 2023 年,NMPA 批准的 250 个创新医疗器械中,境内创新医疗器械涉及 16 个省的 167 家企业,进口产品则涉及 5 个国家的 18 个企业。
4、 继续推进医疗器械技术审评能力建设的研究建议
4.1 提高风险防范意识,推进质量管理能力建设
审评风险分析是实现审评质量和效率提升的重要基础,如何有效防范风险,实现科学审评,则是关键所在。对审评体制、机制、制度加以规范,统一科学审评理念,通过审评信息化手段加以规避和防范审评风险,从而不断提升科学审评能力和风险防范能力。继续实施好案卷评查、内部审核、管理评审等工作机制,秉持“科学、公正、创新、廉洁”的质量方针,建立面向审评全过程、全部门、分中心的质量管理体系,是未来强化技术审评能力建设的重中之重。
4.2 强化创新能力建设,提高审评服务能力
为了充分发挥产业聚集地区的创新发展优势,器审中心应当持续加强与浙江、广东、上海、江苏、四川、吉林、福建等省级药品监管部门的通力合作,强化省级创新服务站对技术审评工作的支撑作用 ;依托创新服务站、长三角分中心以及大湾区分中心,加大对医疗器械注册申请人的服务力度,提升创新产品沟通交流的质量与效率。
4.3 加快人才队伍建设,提高审评人员专业素养
医疗器械审评能力的提升对审评人员的专业素养提出了更高的要求。建议审评部门合理配置职业化审评队伍的规模,稳定业务骨干和高水平审评人员。建立良好的激励机制及考核方法,明确岗位职责,以审评工作需求为依据,以高层次人才培养为重点,加强培训与研究能力的提升。同时,强化外部咨询专家遴选与使用,弥补审评人员面对新技术所产生的审评能力不足。
4.4 加大网络培训平台建设,提高审评服务能力
充分发挥“器审云课堂”网络平台 ( https://learn.cmde.org.cn/) 的培训职能,做好注册申请人的审评咨询服务工作。针对医疗器械企业在产品研发、受理补正与审评补正阶段所遇到的问题,以现场咨询、视频咨询等形式进行服务,提升审评服务能力,实现对省域内医疗器械产品相关企业的主动服务全覆盖。

来源: 药械法苑


